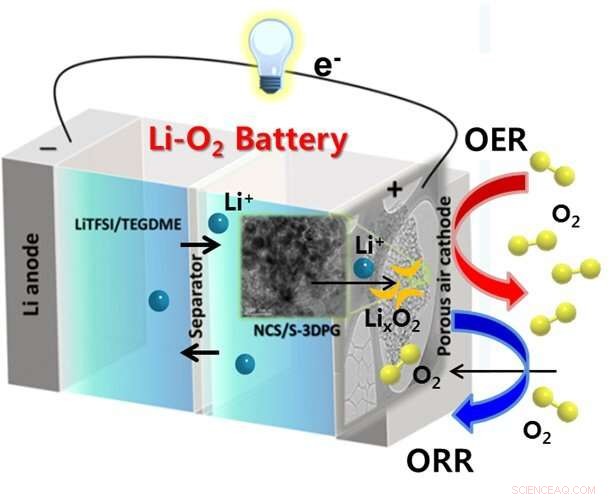
La cathode est conçue pour faciliter l'absorption et la libération d'oxygène, processus nécessaires pour décharger et charger une batterie lithium-air. Crédit :DGIST
Les chercheurs de la DGIST améliorent les performances des batteries lithium-air, nous rapprochant des voitures électriques qui peuvent utiliser l'oxygène pour fonctionner plus longtemps avant d'avoir besoin de se recharger. Dans leur dernière étude, publié dans la revue Catalyse appliquée B :Environnement , ils décrivent comment ils ont fabriqué une électrode en utilisant des nanoflocons de sulfure de nickel cobalt sur un graphène dopé au soufre, conduisant à une batterie longue durée avec une capacité de décharge élevée.
"La distance parcourue par les voitures électriques fonctionnant sur batteries lithium-ion est d'environ 300 kilomètres, ", explique le chimiste Sangaraju Shanmugam de l'Institut coréen des sciences et technologies Daegu Gyeongbuk (DGIST). " Cela signifie qu'il est difficile de faire un aller-retour entre Séoul et Busan avec ces batteries. Cela a conduit à des recherches sur les batteries lithium-air, en raison de leur capacité à stocker plus d'énergie et ainsi à fournir un kilométrage plus long."
Mais les batteries lithium-air sont confrontées à de nombreux défis avant de pouvoir être commercialisées. Par exemple, elles ne déchargent pas d'énergie aussi vite que les batteries lithium-ion, ce qui signifie qu'une voiture électrique avec une batterie lithium-air peut voyager plus loin sans avoir besoin de recharger, mais il faudrait conduire très lentement. Ces batteries sont également moins stables et devraient être remplacées plus souvent.
Shanmugam et ses collègues ont concentré leurs recherches sur l'amélioration de la capacité des batteries lithium-air à catalyser les réactions entre les ions lithium et l'oxygène, qui facilitent la libération d'énergie et le processus de recharge.
Les batteries ont deux électrodes, une anode et une cathode. Les réactions entre les ions lithium et l'oxygène se produisent à la cathode dans une batterie lithium-air. Shanmugam et son équipe ont développé une cathode à base de nanoflocons de sulfure de cobalt et de nickel placés sur un graphène poreux dopé au soufre.
Leur batterie a démontré une capacité de décharge élevée tout en maintenant ses performances de batterie pendant plus de deux mois sans que la capacité ne diminue.
Le succès de la batterie est dû à plusieurs facteurs. Les pores de différentes tailles dans le graphène ont fourni une grande quantité d'espace pour que les réactions chimiques se produisent. De la même manière, les paillettes de catalyseur de sulfure de nickel et de cobalt possèdent de nombreux sites actifs pour ces réactions. Les flocons forment également une couche protectrice qui rend l'électrode plus robuste. Finalement, le dopage du graphène avec du soufre et l'interconnectivité de ses pores améliorent le transport des charges électriques dans la batterie.
L'équipe prévoit ensuite de travailler sur l'amélioration d'autres aspects de la batterie lithium-air en menant des recherches sur la compréhension des comportements de décharge/charge des électrodes et de ses caractéristiques de surface. « Une fois que nous avons sécurisé les technologies de base de toutes les parties de la batterie et les avons combinées, il sera possible de commencer à fabriquer des prototypes, " dit Shanmugam.