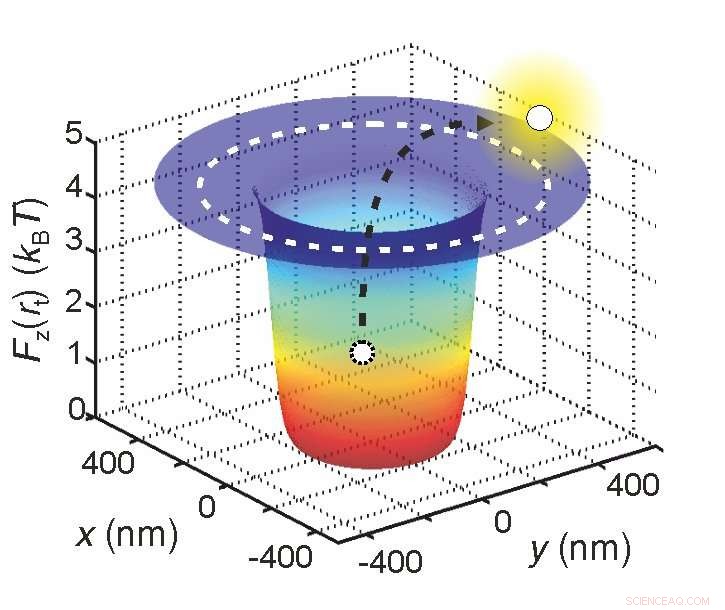
Les scientifiques peuvent déterminer la charge électrique effective d'une molécule en la piégeant dans un puits de potentiel en mesurant combien de temps elle reste à l'intérieur. Crédit :Madhavi Krishnan / Université de Zurich
Pour la première fois, les scientifiques ont mesuré avec précision la charge électrique effective d'une seule molécule en solution. Cette connaissance fondamentale d'un professeur du FNS pourrait également ouvrir la voie à de futurs diagnostics médicaux.
La charge électrique est l'une des propriétés clés qui permet aux molécules d'interagir. La vie elle-même dépend de ce phénomène :de nombreux processus biologiques impliquent des interactions entre des molécules comme des protéines, où leur charge joue un rôle essentiel. Encore, la charge d'une protéine dans un environnement aqueux – son contexte naturel dans un organisme vivant – est difficile à déterminer avec précision en utilisant les approches traditionnelles.
Madhavi Krishnan, titulaire d'une chaire FNS à l'Université de Zurich, a développé une méthode pour mesurer avec précision la charge d'une seule molécule en solution. Son avancée a été décrite dans une série d'articles dans Nature Nanotechnologie , Examen physique E et le Journal de physique chimique . Cette découverte pourrait ouvrir la voie à de nouveaux outils de diagnostic puisque, au niveau chimique, de nombreuses maladies sont liées à un changement de charge électrique d'une protéine, qui empêche la molécule d'agir comme elle le devrait.
La charge électrique d'une molécule peut être très différente en phase gazeuse et en solution. La raison de cette différence réside dans les interactions complexes entre l'objet et le liquide environnant. D'où, les mesures standard en phase gazeuse ne renseignent pas directement sur le comportement de la molécule dans son contexte biologique.
"Comme des enfants qui tapent dans un ballon"
Les molécules en solution sont en mouvement constant, se donner des coups de pied au hasard. Krishnan et Ph.D. l'étudiante Francesca Ruggeri a profité de ce phénomène bien connu, appelé mouvement brownien, afin de mesurer la charge effective d'une molécule directement en solution.
D'abord, ils ont piégé la molécule dans un "puits de potentiel". Plutôt qu'un puits réel, c'est une situation où l'énergie potentielle de la molécule est à son minimum. Dans une telle situation, les molécules d'eau rebondissantes tentent continuellement d'expulser la molécule du puits.
"C'est comme des enfants qui jouent avec une balle au fond d'une fosse, " explique Krishnan. " La balle est la molécule qui nous intéresse, et les enfants sont les molécules d'eau. Le ballon devrait recevoir un coup de pied assez dur pour s'envoler hors de la fosse."
Plus la charge effective de la molécule est élevée, plus la profondeur du puits de potentiel est grande et, par conséquent, plus la probabilité que la molécule soit éjectée du puits est faible. En pratique, cela signifie que le temps nécessaire pour que la molécule soit expulsée du puits est directement lié à sa charge effective.
"En fin de compte, cela se résume à un principe statistique, " explique Krishnan. " Si nous savons combien de temps une molécule reste piégée dans le puits, nous connaissons précisément la profondeur du puits. Et comme cette profondeur dépend directement de la charge effective de la molécule, nous pouvons également en déduire cette valeur très précisément."
Deux plaques de verre
Afin de créer un puits de potentiel, les scientifiques ont comprimé une solution contenant les protéines entre deux plaques de verre, l'un d'eux étant couvert de trous microscopiques. Les molécules piégées dans les puits potentiels ont été marquées avec des agents fluorescents, ce qui a permis de les suivre au microscope optique.
Bien que la découverte ait des implications fondamentales importantes, cela pourrait également ouvrir la voie à de nouveaux outils de diagnostic pour de nombreuses maladies causées par des protéines mal formées, comme la maladie d'Alzheimer et les cancers. "Nous savons que la conformation 3-D d'une protéine influence sa charge effective, et notre travail pourrait présenter une nouvelle voie pour détecter des protéines défectueuses. »