Depuis la révélation des inhibiteurs de la poly(ADP-ribose) polymérase (PARP) et leurs résultats remarquables dans le traitement des cancers mutants BRCA1/2, la létalité synthétique (SL) dans la thérapie antitumorale a attiré une attention croissante. SL est un phénomène dans lequel un seul événement génétique est insuffisant pour induire la mort cellulaire, mais plusieurs événements génétiques conduisent à la mort cellulaire.
La caractérisation des interactions génétiques SL avec des mutations spécifiques à une tumeur peut être utilisée pour développer un cadre conceptuel permettant de s'attaquer à des cibles « non médicamentables » telles que le gène suppresseur de tumeur p53. Le cancer de la vésicule biliaire (GBC) est la tumeur maligne du système biliaire la plus répandue et est généralement mortelle en raison de l'efficacité limitée des traitements existants.
Il a été rapporté que p53 est l'un des gènes les plus fréquemment mutés et un marqueur de mauvais pronostic dans la GBC. Par conséquent, une stratégie basée sur SL pour cibler les GBC mutés par p53 est une approche prometteuse.
Une nouvelle étude sur ce sujet dirigée par le professeur Mingyu Chen, le professeur Xiujun Cai, le Dr Shjie Li, le Dr Sarun Juengpanich et le Dr Win Topatana, tous de l'hôpital Sir Run-Run Shaw, de l'Université du Zhejiang, et le professeur Jicheng Yu du Collège des sciences pharmaceutiques de l'Université du Zhejiang apparaît dans le Science Bulletin .
Des études antérieures ont montré que la réparation des dommages à l'ADN réalisée par WEE1 via la régulation du point de contrôle G2 du cycle cellulaire est essentielle à la survie des cellules mutées par p53. Par conséquent, l’adavosertib (ADA), un inhibiteur de WEE1, a un effet létal synthétique significatif sur les cancers mutés par p53. Cependant, la résistance aux médicaments due aux voies de compensation de la réponse aux dommages de l'ADN (DDR) et à la toxicité élevée limite d'autres applications.
Des études récentes ont indiqué que l'utilisation de facteurs physiques tels que la thérapie photodynamique (PDT), la thérapie sonodynamique (SDT) et la gazothérapie dans le traitement des tumeurs ont des effets supérieurs et une gamme d'applications plus large que les médicaments chimiques conventionnels. Les facteurs physiques fournissent des conditions irréversibles pour renforcer l'effet mortel synthétique de la destruction des tumeurs et s'avéreront être une stratégie efficace.
Ainsi, sur la base de la capacité de la structure MOF à réaliser diverses conditions supplémentaires lors de l'administration de médicaments, cette nouvelle étude a sélectionné MOF comme outil en conjonction avec SDT pour améliorer l'effet létal synthétique entre WEE1 et p53 dans GBC et a obtenu un résultat prometteur. P>
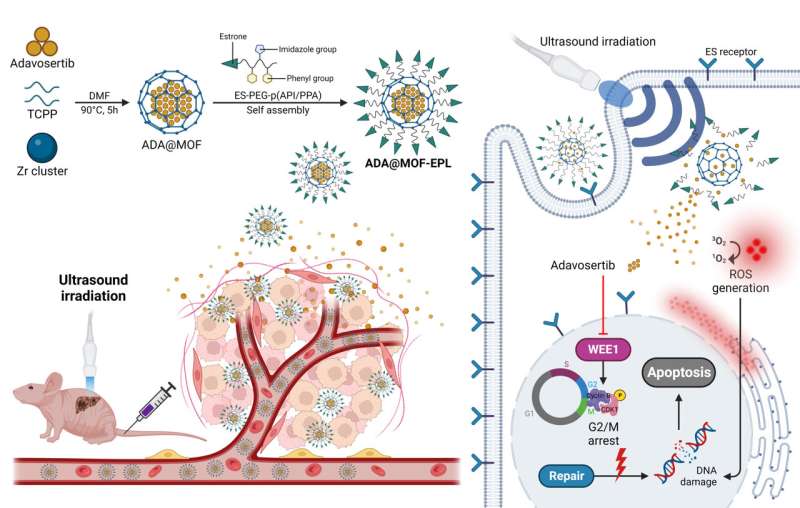
Plus précisément, une porphyrine sonosensible (tétrakis (4-carboxyphényl) porphyrine, TCPP) contenant du Zr-MOF a été utilisée comme squelette organique pour la thérapie sonodynamique (SDT), suivie d'une encapsulation d'ADA pendant la synthèse de MOF en un seul pot pour augmenter la charge d'ADA. des MOF (ADA@MOF). De plus, la surface de ADA@MOF a été recouverte de ligands polymères (EPL) ciblés sur l'estrone sensibles au pH pour conférer aux nanoparticules une capacité de ciblage des tumeurs (ADA@MOF-EPL).
En raison de l’expression élevée du récepteur des œstrogènes (ER) dans les GBC, l’estrone fonctionne comme un ligand ciblant les tumeurs, permettant aux nanoparticules d’entrer et de s’accumuler rapidement et précisément à proximité du noyau cellulaire. En entrant dans le microenvironnement acide de la tumeur (TME), les interactions ioniques affaiblies entre ADA@MOF et EPL relâcheront sa structure, conduisant à la libération initiale d'ADA.
Par la suite, l'irradiation par ultrasons (US) pour stimuler le MOF sonosensible contenant de la porphyrine entraînera la libération accélérée d'ADA et générera des ROS pour endommager l'ADN. Cela entraînera une plus grande sensibilité des cellules cancéreuses mutées par p53 à l'ADA et évitera la résistance aux médicaments due aux voies de compensation DDR à la source.
Ainsi, l’effet létal synthétique amélioré entre l’ADA et p53 grâce à une condition supplémentaire de SDT aurait une forte capacité de destruction des tumeurs. De plus, les nanoparticules réduisent également considérablement la réaction toxique du médicament. Plus important encore, cette nouvelle étude offre une nouvelle perspective sur l'utilisation de systèmes d'administration de médicaments basés sur MOF dans le traitement de divers cancers réfractaires via une SL améliorée.
Plus d'informations : Shijie Li et al, Cadres métallo-organiques encapsulés dans l'adavosertib pour le traitement du cancer de la vésicule biliaire muté par p53 via une létalité synthétique, Science Bulletin (2024). DOI :10.1016/j.scib.2024.02.039
Fourni par Science China Press