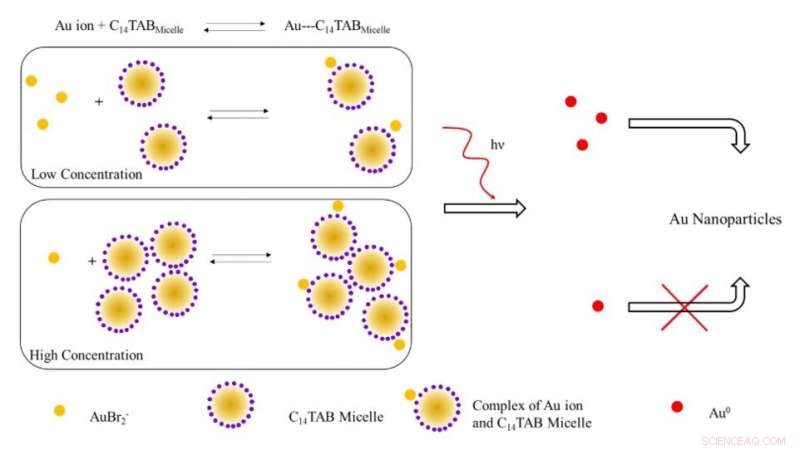
Illustration schématique du mécanisme proposé pour la formation de nanoparticules d'or lors d'une irradiation avec des rayonnements ionisants. A de faibles concentrations de tensioactifs, la plupart des ions or (AuBr2- /Au1+) sont probablement libres en solution (non liés aux micelles). Avec l'augmentation de la concentration en tensioactif, l'équilibre se déplace vers la droite avec une diminution des ions d'or libres. Lors de l'irradiation, le nombre d'atomes Au^0 formés en raison de la réduction à faible concentration en tensioactif est plus élevé en raison de la présence d'un nombre plus élevé d'ions d'or libres contrairement au système à forte concentration en tensioactif. Le nombre plus élevé d'atomes d'or libres conduit à un rendement accru de nanoparticules d'or en raison de la réduction assistée par la surface avec des ions d'or n'ayant pas réagi. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aaw8704.
La mesure de routine des doses de rayonnement peut être difficile sur le plan clinique en raison des limites des dosimètres conventionnels utilisés pour mesurer l'absorption de dose de rayonnement ionisant externe. Dans une nouvelle étude, Karthik Pushpavanam et une équipe interdisciplinaire de chercheurs dans les départements de génie chimique, Sciences moléculaires, Banner MD Anderson Cancer Center et Arizona Veterinary Oncology aux États-Unis ont décrit un nouveau nanocapteur à base de gel. La technologie permet la détection colorimétrique et la quantification des profils topographiques de dose de rayonnement pendant la radiothérapie.
Lors de l'exposition aux rayonnements ionisants, les scientifiques ont converti les ions d'or du gel en nanoparticules d'or (AuNP) accompagnées d'un changement visuel de la couleur du gel en raison des propriétés plasmoniques. Ils ont utilisé l'intensité de la couleur formée dans le gel en tant que rapporteur quantitatif pour les rayonnements ionisants et ont d'abord utilisé le nanocapteur de gel pour détecter des schémas de dose topographiques complexes après administration à des modèles fantômes anthropomorphes, suivi d'applications avec des patients canins vivants subissant une radiothérapie clinique. La facilité de fabrication, opération, lecture rapide, la détection colorimétrique et le coût relativement faible de la technologie impliquaient un potentiel translationnel pour la cartographie topographique de la dose lors des applications de radiothérapie clinique. Les travaux de recherche sont maintenant publiés sur Avancées scientifiques .
Les progrès de la radiothérapie ont conduit à une sophistication notable et à un logiciel de planification de pointe pour fournir aux patients des doses de rayonnement conformes élevées pour une meilleure qualité de vie après le traitement. Pendant la radiothérapie, une dose élevée est généralement délivrée à une tumeur cible tout en minimisant la dose de rayonnement délivrée aux tissus environnants. Pendant les soins palliatifs, les patients reçoivent des doses fractionnées plus importantes afin de terminer le traitement dans un court laps de temps. Cependant, des erreurs logicielles au cours de telles procédures peuvent entraîner un surdosage et une morbidité ultérieure.
Pour minimiser la surexposition accidentelle, les chercheurs cherchent à vérifier de manière indépendante la dose de rayonnement délivrée au niveau ou à proximité du tissu cible pour une sécurité avancée des patients. Techniquement, les capteurs moléculaires et les nanocapteurs peuvent surmonter les limites présentes dans les systèmes conventionnels pour former des alternatives pratiques en tant que capteurs faciles. Cependant, leurs limites existantes devraient être abordées et atténuées pour développer des capteurs robustes et efficaces qui déterminent quantitativement et qualitativement les profils de dose topographiques pendant la radiothérapie clinique.

Images numériques et spectres UV-visible de différentes formulations de nanocapteurs de gel exposés à des doses thérapeutiques de rayons X (A) Images de nanocapteurs de gel fabriqués dans des plaques de culture cellulaire à 24 puits et contenant différentes concentrations de C14TAB (24,5 à 73,5 mM) lors de l'exposition à diverses doses de rayonnement ionisant (rayons X de 0 à 10 Gy); Le temps d'attente du Na2S était de 5 min après l'irradiation, et le temps d'incubation était de 10 min. Les images ont été acquises 1 heure après l'irradiation. Une augmentation visible de l'intensité de la couleur marron est observée avec des doses croissantes de rayonnement ionisant pour la plupart des concentrations de C14TAB utilisées lors du développement du capteur de gel. (B à F) Spectres d'absorbance (300 à 990 nm) des mêmes nanocapteurs gel contenant (B) 24,5 mM, (C) 31 mM, (D) 37 mM, (E) 49 mM, et (F) 73,5 mM irradiés en utilisant différentes doses de rayonnement. Les pics d'absorbance caractéristiques entre les longueurs d'onde de 500 et 600 nm indiquent des nanoparticules d'or formées dans les gels. Les doses de rayonnement correspondantes sont mentionnées dans la légende avec une dose de rayonnement croissante (de haut en bas). A.U., unités arbitraires. Crédit photo :Sahil Inamdar, Université de l'État d'Arizona. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aaw8704
Étant donné que les nanoparticules d'or (AuNP) ont des caractéristiques physiques et chimiques uniques qui constituent une excellente plate-forme pour développer des capteurs. Pushpavanam et al. a conçu un capteur colorimétrique où le rayonnement ionisant a provoqué la formation d'AuNP à partir de précurseurs de sel incolore. La formation d'un nanocapteur à base de gel peut permettre une manipulation et des applications faciles pendant la radiothérapie clinique.
Dans le travail present, l'équipe a démontré la détection colorimétrique et la quantification des profils de distribution de dose à l'aide d'un nanocapteur à gel pour cartographier topographiquement les doses de rayonnement le long des surfaces des tissus. Lors des évaluations précliniques, l'équipe a administré la technologie de nanocapteur sur gel à des patients canins vivants subissant une radiothérapie. Au total, les résultats ont indiqué la portée de la technologie pour la traduction clinique chez les patients humains et la capacité de déterminer les doses topographiques pour planifier les traitements et vérifier les dosages pendant la radiothérapie du cancer.
Lors des expérimentations, la conversion des ions d'or en nanoparticules s'est accompagnée d'un développement de couleur marron dans la région irradiée du nanocapteur de gel. Alors que l'or existe dans un état trivalent en général (AuCl
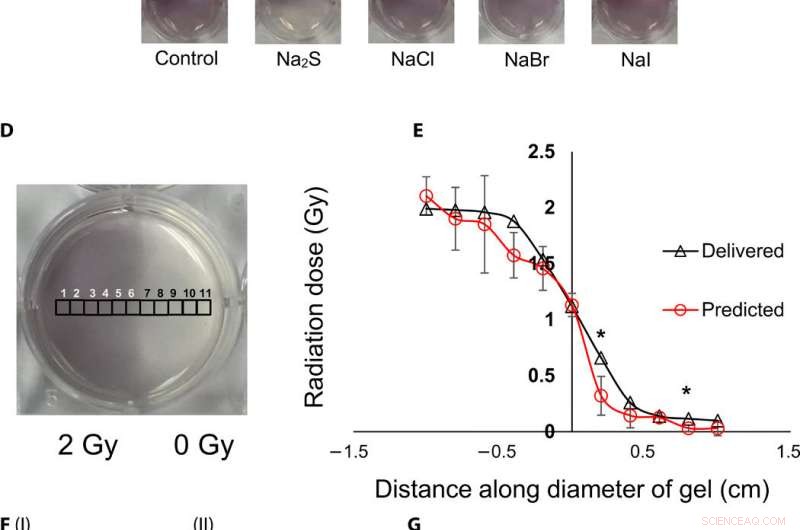
Visualisation topographique et quantification des doses de rayonnement à l'aide de nanocapteurs à gel. (A) Gel nanocapteur (à gauche) avant irradiation, (milieu) moitié supérieure irradiée avec 4 Gy et image acquise 2 min après irradiation, et (à droite) image acquise 1 heure après irradiation. Une augmentation visible de l'intensité de la couleur dans la moitié inférieure non irradiée indique une perte de couleur et une perte d'informations topographiques. (B) I :1,5 % (p/v) de gel d'agarose (à gauche) 2 min après l'irradiation et (à droite) 1 heure après l'irradiation ; II:2% (w/v) agarose gel (left) 2 min after irradiation and (right) 1 hour after irradiation indicates that the increase in agarose weight percentage does not preserve topographical dose information. (C) Gel nanosensor incubated with 5 mM sodium sulfide (Na2S) and various sodium halides with a wait time of 10 min and incubation time of 10 min; images were acquired after 1 hour. No loss of topographical information is observed upon incubation with sodium sulfide. All gels were fabricated in 24-well plates. (D) Colorimetric response of the gel nanosenor irradiated on one-half with a 2-Gy x-ray dose. A visible appearance of maroon color in the irradiated region illustrates the ability of the gel nanosensor to visualize topographical dose profiles. Each black square box (labeled 1 to 11) on the gel nanosensor corresponds to a grid of size ≈2 × 2 mm, whose absorbance at 540 nm is determined. Grids starting from 1 to 5 are regions exposed to ionizing radiation, 6 is the grid at the edge of the irradiation field, and grids from 7 to 11 are regions outside the field of irradiation. (E) Dose fall-off profile for the gel nanosensor irradiated by 2 Gy on one-half. The delivered and predicted radiation doses are comparable, which indicates the efficacy of the gel nanosensor in visualizing and retaining topographical information. In all cases, Na2S was added for 10-min incubation time after a wait time of 30 min. Radiation doses predicted by the gel nanosensor as compared with the delivered radiation dose as obtained from the treatment planning system. Asterisks indicate statistically significant differences (P <0.05) between the delivered dose and the dose predicted by the gel nanosensor (n =3 independent experiments). (F) Representative image of a petri dish containing the gel nanosensor formulation (≈3 mm thick and ≈10 cm diameter) irradiated with a 1 cm × 1 cm square field of x-ray radiation. À partir de la gauche, each square indicates increasing radiation dose from (I) 0.5 Gy (red box), 1 Gy, and 1.5 Gy; (II) 2, 2.5, 3, and 3.5 Gy; and (III) 4, 4.5, and 5 Gy; the black box in image (II) shows 0 Gy. (G) Visualization of a complex topographical dose pattern (ASU letters) generated using a 2-Gy x-ray dose. The petri dish has a diameter of ≈10 cm. In (F) and (G), the gel nanosensors contain 24.5 mM C14TAB, and Na2S was added after a wait time of 30 min and incubation time of 10 min; a representative image from three independent experiments is shown. Photo credit:Sahil Inamdar, Université de l'État d'Arizona. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aaw8704.
To determine intensity of the color and dose delivered within gels after irradiation, the researchers used absorbance spectroscopy and observed a decrease in the spectral profile width, with increasing radiation dose for decreased polydispersity (ratio of the percentage of the standard deviation to the average value) of the nanoparticles. The peak absorbance intensity increased with increasing radiation dose to corroborate the observed increase in color intensity.
To understand the gel nanosensor's ability to detect topographical distribution of the radiation dose, the scientists irradiated half of the gel nanosensor with a 4 gray (Gy) dose. The maroon-color only appeared in the irradiated area confirming AuNP formation, but after one hour of exposure, the color bled into the irradiated region showing loss of topographic information in the gel with time. The team observed the phenomenon to arise from reaction-controlled conditions and not based on the gel composition. By incubating the gel with sodium sulfide (Na
The research team then used the gel nanosensor to visualize diverse topographical radiation patterns, where the intensity of the color increased with increasing dose while preserving topographical integrity. Comme preuve de concept, they showed the gel nanosensor's ability to detect complex radiation patterns with a model dose patterned to form "ASU" (after Arizona State University). Then using transmission electron microscopy (TEM), the scientists characterized the generated gold nanoparticles as a function of dose to observe reduced average nanoparticle diameter and polydispersity at higher doses of radiation. They followed this with energy dispersive X-ray spectroscopy (EDS) to detect higher yields of AuNPs in the irradiated regions of the gel nanosensor as expected.

Gel nanosensor enabled topographical detection and quantification of clinical radiation doses in anthropomorphic head and neck phantoms. (A) Anthropomorphic head and neck phantom treated with an irregularly shaped x-ray radiation field below the left eye. (B) Image of the gel nanosensor positioned on the anthropomorphic phantom in the radiation field mimicking a conventional radiotherapy session. (C) Axial view of the treatment planning image along the central axis of the radiation beam representing an irregularly shaped radiation field used to deliver a complex radiation pattern under the eye of the phantom. The core of the crescent-shaped treatment region receives a radiation dose of 2.3 Gy (highlighted in red), and regions receiving lower doses are highlighted with different colors going outward (from green to light pink). (D) Visual image of the dose pattern on the gel nanosensor formed after delivery of 2.3 Gy. Only the irradiated region develops a maroon color, while the nonirradiated region remains colorless. (E) Expected topographical dose “heat map” profile of the radiation dose delivered to the gel placed in the phantom. The expected profile is generated from the treatment plan in the dose delivery system. In these figures, red and blue colors indicate higher and lower radiation doses, respectivement. (F) Topographical doses predicted by the irradiated gel nanosensor. Absorbance values of ≈2 mm × 2 mm grids were quantified using a calibration curve to generate the topographical dose profile. The anticipated dose received by the core of the crescent-shaped profile (2.3 Gy) is comparable to the dose profile predicted by the gel nanosensor (2.3 Gy), which demonstrates the capability of the gel nanosensor to qualitatively and quantitatively detect complex topographical dose profiles. Photo credit:Sahil Inamdar, Université de l'État d'Arizona. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aaw8704.
To investigate translational potential of the gel nanosensor and predict topographical profiles of radiation, Pushpavanam et al. first used a head and neck phantom model. They delivered an irregular crescent-shaped radiation dose near the eye to mimic clinically challenging administration modes of radiotherapy close to critical structures such as the eye during skin cancer treatment. The dose profile delivered using the treatment planning system was in excellent agreement with the predictions of the gel nanosensor. Indicating its capability to detect and predict complex radiation patterns similar to those used in clinical human radiotherapy.
During preclinical studies, the research team used two canine models undergoing radiotherapy to investigate the efficiency of gel nanosensors as independent, nanoscale radiation dosimeters for the first time and compared the efficiency with conventional clinical radiochromic films. On completion of the treatment, Pushpavanam et al. observed maroon color formation in one-half of the gel, whereas the non-irradiated region remained colorless. They showed predictions of the gel nanosensor in the irradiated region to agree excellently with the treatment planning system and the radiochromic film. The gel nanosensor also predicted for the region external to the irradiation to receive minimal radiation and their topographical dose profiles as well. The performance was comparable to clinical radiochromic films but with faster than conventional wait times (typically> 24 hours) to obtain the results. The scientists demonstrated the simplicity of fabrication, operation, readout time and cost effectiveness ($ 0.50 per gel material only) of the frugal invention. They maintained the response of the gel nanosensor for at least seven days to indicate long-term retrieval of dosing data unlike with fluorescence-based dosimeters with readouts that lasts mere minutes.
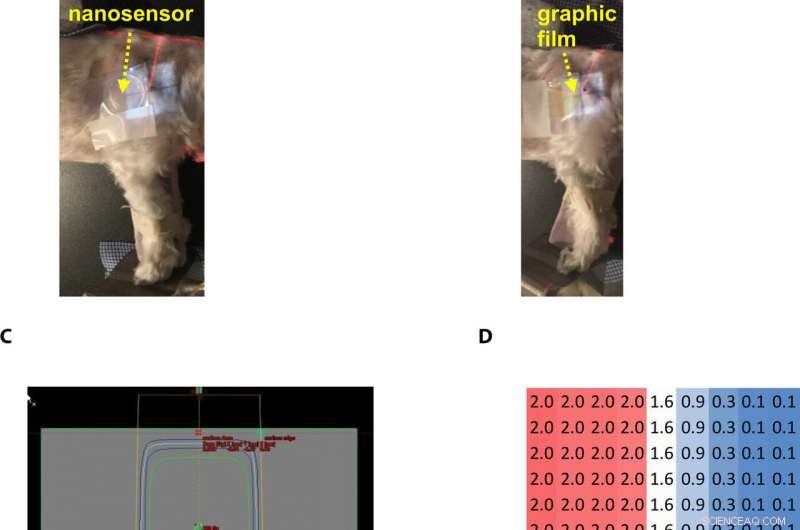
Gel nanosensor enabled topographical detection and quantification of radiation delivered to canine patient A undergoing clinical radiotherapy. Representative image of (A) half of the gel nanosensor and (B) half of the radiographic film positioned in the radiation field delivered to canine patient A. (C) Treatment planning software depicting the delivery of a 2-Gy dose delivered to the surface of patient A (neon green edge along the rectangular gray box indicates the region receiving the 2-Gy dose). (D) The irradiated region received a dose of 2 Gy (highlighted in red squares), with irradiation dose dropping to a minimal radiation 0.1 Gy (highlighted in blue squares) outside the field of irradiation. A color change is visible in both the (E) gel nanosensor whose color changes to maroon and (F) radiographic film whose color changes to dark green after irradiation. The predicted dose map in the gel nanosensor (Na2S addition wait time of 30 min and incubation time of 10 min) and radiographic film are shown below each corresponding sensor. Similarity in the dose profiles indicates the efficacy of the gel nanosensor for clinical dosimetry. The time for readout of the gel nanosensor was 1 hour after irradiation, while the radiochromic film required>24 hours of developing time before readout. All experiments were carried out three independent times. Photo credit:Sahil Inamdar, Université de l'État d'Arizona. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aaw8704.
De cette façon, Karthik Pushpavanam and colleagues developed the first colorimetric gel nanosensor as a nanoscale dosimeter to detect and distinguish regions exposed to irradiation. They optimized the platform with a chemical quenching agent (Na
© 2019 Réseau Science X