
Kristina Tschulik et Mathies Evers développent des méthodes qui permettent d'utiliser le moins possible les nanoparticules de métaux précieux rares et chères pour la catalyse. Crédit : RUB, Marquard
Des chercheurs de la Ruhr-Universität Bochum et du Fritz Haber Institute Berlin ont développé une nouvelle méthode pour conserver les catalyseurs rares et coûteux et les utiliser avec parcimonie. Ils ont enfermé un sel de métal précieux dans de minuscules micelles, et les a frappés contre une électrode de carbone, revêtant ainsi la surface de nanoparticules du métal précieux contenu dans les micelles. À la fois, l'équipe a analysé avec précision la quantité de métal déposée. Les chercheurs ont ensuite montré que l'électrode revêtue de cette manière pouvait catalyser efficacement la réduction de l'oxygène, qui est le processus chimique limitant dans les piles à combustible.
L'équipe, dirigé par le professeur Kristina Tschulik et Mathies Evers du groupe de recherche de Bochum pour l'électrochimie et les matériaux à l'échelle nanométrique décrit le processus dans le journal Angewandte Chemie , publié en ligne à l'avance le 11 avril 2019.
Produire des particules de même taille
Le groupe de recherche a produit les nanoparticules d'or à l'aide de micelles. Les particules étaient initialement constituées d'une substance précurseur, acide chloraurique, qui était enveloppé dans une coque extérieure en polymère. L'avantage :« Lorsque nous produisons des nanoparticules d'or à l'aide de micelles, les nanoparticules sont toutes de taille quasi identique, " dit Kristina Tschulik, chercheur principal du Cluster of Excellence Ruhr Explores Solvation (Resolv). Seule une certaine charge du matériau précurseur, à partir de laquelle une seule particule d'une certaine taille est produite, s'adapte à l'intérieur de la petite micelle. "Comme les particules de tailles différentes ont des propriétés catalytiques différentes, il est important de contrôler la granulométrie au moyen de la quantité de charge de la micelle, " ajoute Tschulik.
Revêtement uniforme, même sur des surfaces complexes
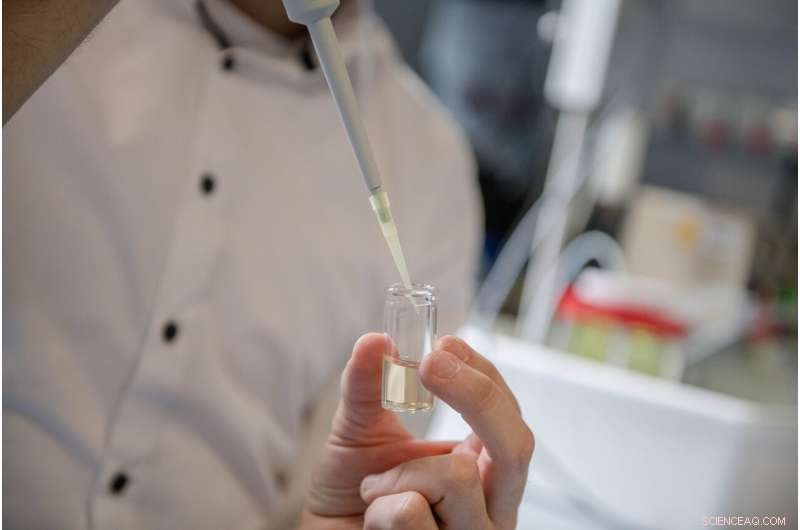
Cette solution contient le matériau précurseur qui est transformé en nanoparticules d'or dans les expériences électrochimiques. Crédit : RUB, Marquard
Pour enrober l'électrode cylindrique, les chercheurs l'ont plongé dans une solution contenant les micelles chargées et ont appliqué une tension à l'électrode. Le mouvement aléatoire des micelles dans la solution les a amenés à heurter la surface de l'électrode au fil du temps.
Là, l'enveloppe extérieure s'est ouverte et les ions d'or de l'acide chloroaurique ont réagi pour former de l'or élémentaire, qui adhère à la surface de l'électrode sous la forme d'une couche uniforme de nanoparticules. "Seuls les substrats plats peuvent être recouverts uniformément de nanoparticules en utilisant des méthodes standard, " explique Tschulik. "Notre procédé signifie que même des surfaces complexes peuvent être chargées uniformément avec un catalyseur."
Quantité séparée contrôlable avec précision
Alors que les ions d'or de l'acide chloroaurique réagissent pour former de l'or élémentaire, les électrons circulent. En mesurant le courant résultant, les chimistes peuvent déterminer exactement la quantité de matériau utilisée pour revêtir l'électrode. À la fois, la méthode enregistre l'impact de chaque particule individuelle et sa taille.
Les chercheurs ont testé avec succès la réaction de réduction de l'oxygène des électrodes revêtues à l'aide du nouveau procédé. Ils ont atteint une activité aussi élevée que celle des nanoparticules d'or nues sans enveloppe extérieure. En raison du revêtement uniforme de la surface, ils ont également observé une vitesse de réaction presque aussi élevée que celle d'électrodes entièrement recouvertes d'or et d'électrodes en or massif à seulement onze pour cent de couverture.