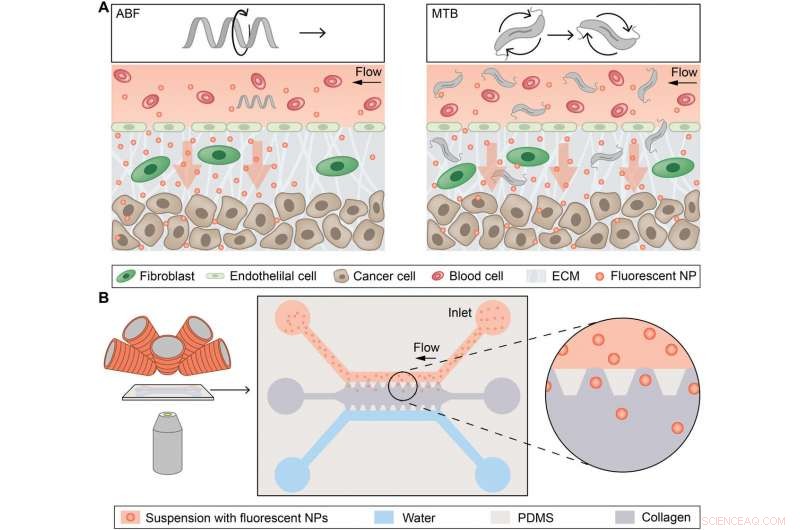
Aperçu conceptuel des microhélices à commande magnétique pour le transport de NP amélioré par convection. (A) Schéma conceptuel représentant un seul microrobot, le flagelle bactérien artificiel (ABF), l'amélioration du transport de masse des nanoparticules (NP) à l'interface vaisseau-tissu (à gauche), et des essaims de bactéries magnétotactiques (MTB) générant un écoulement convectif pour améliorer le transport de masse (à droite). ECM, matrice extracellulaire. (B) Schéma de la plate-forme magnétofluidique pour les études de transport de masse NP utilisant la convection induite magnétiquement. La puce microfluidique est placée entre l'objectif d'un microscope optique inversé et les électro-aimants (à gauche). Un schéma représente la puce, composé d'un canal supérieur rempli de NP (rouge) et d'un canal d'eau inférieur (bleu) qui bordent tous deux une matrice de collagène (gris) le long de montants trapézoïdaux restrictifs en PDMS. Les NP peuvent diffuser passivement dans la matrice de collagène le long de leur gradient de concentration vers le canal d'eau. Crédit: Avancées scientifiques , doi:10.1126/sciadv.aav4803
Les nanoparticules (NP) sont une plate-forme prometteuse pour l'administration de médicaments afin de traiter diverses maladies, notamment le cancer, maladies cardiovasculaires et inflammations. Pourtant, l'efficacité du transfert de NP vers le tissu malade d'intérêt est limitée en raison d'un assortiment de barrières physiologiques. Un obstacle important est le transport des NP pour atteindre précisément le tissu cible d'intérêt. Dans une étude récente, S. Schuerle et une équipe de chercheurs interdisciplinaires des départements de médecine translationnelle, Biophysique, Robotique d'ingénierie, Nanomédecine et électronique, en Suisse, le Royaume-Uni et les États-Unis ont développé deux micro-hélices distinctes basées sur des microrobots pour relever le défi.
Ils ont utilisé des champs magnétiques rotatifs (RMF) pour alimenter les appareils et créer une convection de fluide locale pour surmonter le transport limité par la diffusion des nanoparticules. Lors de la première approche expérimentale, ils ont utilisé un seul microrobot magnétique synthétique comme flagelle bactérien artificiel (ABF), puis ont utilisé des essaims d'une bactérie magnétotactique naturelle (MTB) pour créer un "ferrofluide vivant" en exploitant la ferrohydrodynamique. En utilisant les deux approches, les scientifiques ont amélioré le transport des NP dans un modèle microfluidique d'extravasation sanguine (mouvement d'un médicament des vaisseaux sanguins vers le tissu externe) et la pénétration des tissus dans des microcanaux entourés d'une matrice de collagène pour créer une interface biomimétique tissu-vaisseau dans le laboratoire. Les résultats de l'étude sont maintenant publiés dans Avancées scientifiques .
Les nanoparticules (NP) sont de plus en plus populaires en nanomédecine en raison du potentiel de recherche biomédicale en tant que vecteurs d'administration de médicaments qui dépassent les limites de la médecine conventionnelle. Alors que les NP sont conçues pour modifier la pharmacocinétique et la biodistribution des médicaments existants, ils sont entravés par des barrières physiologiques, qui empêchent une accumulation réussie sur les sites de la maladie, limitant leurs effets thérapeutiques in vivo. Au cours d'un traitement contre le cancer, par exemple, les porteurs de médicaments rencontrent des vaisseaux anormaux qui entourent l'architecture tumorale pour une libération de médicament intraveineuse inefficace.
Étant donné que l'apport de NP dans les tissus est fortement influencé par leurs propriétés physicochimiques, les scientifiques ont repensé les formes et les tailles des NP pour optimiser leur cinétique de transport à travers les parois des vaisseaux pour atteindre les tissus. Les chercheurs avaient déjà proposé des approches en plusieurs étapes pour une administration optimisée des médicaments, soit en rétrécissant les nanoparticules dans le temps, ou les fragmenter pour se disperser et atteindre un site d'intérêt uniquement après avoir rencontré des signaux microenvironnementaux de maladie in vivo.

Le flagelle bactérien artificiel (ABF) dans un dispositif à flux unique de type microvaisseau. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aav4803
Généralement, Le transport de NP est affecté par la charge de surface, hydrophobie et biochimie de surface; propriétés qui peuvent être activement optimisées dans les travaux de recherche pour un trafic in vivo plus efficace. Les scientifiques ont utilisé des sources d'énergie externes telles que les forces magnétiques et acoustiques pour créer des microrobots contrôlés sans fil et transférer les thérapies aux tissus malades pour un transport diffusif amélioré. Cependant, ces méthodes reposaient encore sur le transport diffusif après largage de leur cargaison embarquée, tandis que le besoin demeure de stratégies de transport plus distinctes vers un lieu défini.
Dans le travail present, Schuerle et al. a détaillé deux stratégies distinctes pour générer un flux convectif localisé sans fil afin d'empêcher le caractère invasif des nanoparticules implantées. Inspiré du domaine des microrobots (microbots), les scientifiques ont utilisé (1) un seul, synthétique, microrobot inspiré des bactéries, ou (2) de grands essaims de bactéries vivantes pour conduire le transport localisé de NP. Les microhélices artificielles et naturelles ont aidé le processus en favorisant la convection à entraînement magnétique dans un emplacement défini dans une configuration magnétofluidique avec un potentiel d'applications thérapeutiques.
Le microbot synthétique a imité la propulsion bactérienne à l'aide d'un flagelle bactérien artificiel (ABF), tandis que les essaims denses de bactéries magnétotactiques (MTB) exploités par Schuerle et al. se sont produits naturellement sous forme de procaryotes à Gram négatif ( Magnetospirillum magnetum ) avec des propriétés magnétiques. Les scientifiques s'attendent à ce que les résultats surmontent les barrières de transport existantes pour une pénétration améliorée des tissus NP via un contrôle sans fil et une convection locale spatio-temporelle précise à l'avenir.
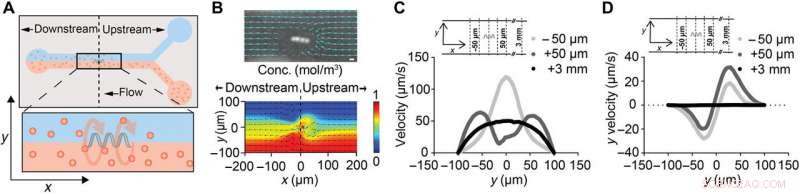
ABF perturbe localement l'écoulement du fluide. (A) Schéma d'un canal microfluidique de 200 µm de large avec ABF suspendu (36 µm de long, 10 m de diamètre) positionné au centre du canal (x, oui, z) =(0, 0, 0). Le canal supérieur contient de l'eau, tandis que le canal inférieur contient des NP fluorescentes à 200 nm. (B) Instantané d'ABF dans un canal de 200 um de large perturbant les chemins suivis des NP fluorescentes de 200 nm indiquant l'écoulement du fluide. Barre d'échelle (en haut), 10 µm. Une simulation numérique d'écoulement bifluide avec un ABF à l'interface, avec couleur indiquant la distribution de concentration (rouge, 1 mol/m3; bleu, 0 mol/m3) d'espèces moléculaires (en bas). (C) Profil de vitesse aux positions en amont et en aval de l'ABF. Pour le contrôle, à x =+3 mm, un profil laminaire non perturbé avec une vitesse maximale de 50 m/s a été simulé. A la fois x =+50 m (en amont) et x =-50 m (en aval), une augmentation des vitesses de pointe est prévue, avec le pic décalé plus près de la paroi du canal pour le cas en amont. (D) Résultats de simulation pour la composante de vitesse y uy (orthogonale vers et hors du canal) aux mêmes positions que (C). Aux abords de l'ABF, une poussée dirigée orthogonale à la direction d'écoulement vers la paroi du canal est prédite. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aav4803
Schuerle et al. conçu l'ABF magnétique en utilisant la lithographie tridimensionnelle (3-D) et le dépôt de métal, comme indiqué précédemment. Les microrobots bioinspirés ont imité les flagelles en rotation pour une locomotion efficace basée sur la propulsion à l'échelle microscopique, où les forces de traînée visqueuses dominent. Ils ont contrôlé le mouvement ABF avec des champs magnétiques uniformes en rotation 3D à l'aide d'une configuration de contrôle magnétique sans fil contenant des électro-aimants disposés autour d'un seul hémisphère.
Ensuite, ils ont monté la configuration sur un microscope inversé pour suivre les mouvements des microrobots contrôlés. Les champs magnétiques tournants (RMF) ont permis la propulsion vers l'avant et l'écoulement convectif dans le fluide environnant et lorsque les scientifiques ont immergé l'ABF dans une suspension de NP fluorescentes, ils ont observé un flux contrôlé pour le transport de masse des NP.
Dans l'expérience, ils ont construit la couche inférieure du canal microfluidique pour contenir les NP de 200 nm similaires à la taille utilisée dans les applications cliniques, tandis que sur la couche fluide supérieure, ils maintenaient une suspension de milieu aqueux pur. Les scientifiques ont placé l'ABF au centre de l'installation pour maintenir sa position à contre-courant en contrôlant le flux de fluide dans l'installation. Cet arrangement de l'ABF dans un canal microfluidique a perturbé le flux laminaire pour produire de la convection, qui a transporté les NP de la couche fluide du bas vers la couche supérieure pour atteindre la paroi du canal, c'est à dire., le lieu d'intérêt.
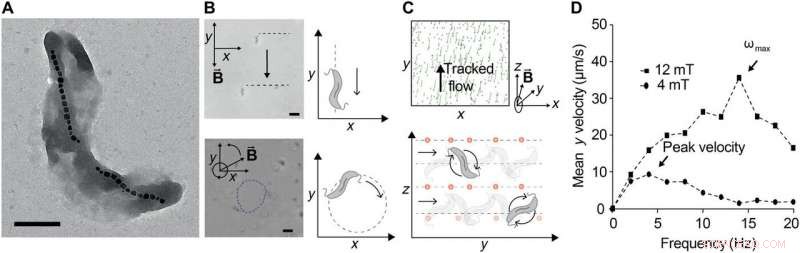
Pompage ferrohydrodynamique avec essaims contrôlés de VTT. (A) Micrographie électronique à transmission de la souche magnétique M. AMB-1. Barre d'échelle, 0,5 µm. Les magnétosomes sont bien visibles, ici formé en deux chaînes distinctes de cristaux d'oxyde de fer. (B) Contrôle d'AMB-1 sous des champs magnétiques statiques (en haut) et des champs magnétiques tournant dans le plan à 1 Hz. Barre d'échelle (en bas), 5 µm. (C) Images post-traitées de suivi, co-suspendu, non magnétique, NPs fluorescentes utilisées pour observer les champs d'écoulement générés par un essaim de VTT exposés à un champ magnétique de 12 mT tournant à 10 Hz dans le plan y-z. Les traces en vert correspondent aux trajectoires parcourues sur 12 images (~1 s). Les positions sont calculées à l'aide d'un filtre passe-bande d'un diamètre de 25 pixels, suivi de la recherche du pic (en haut). Le mouvement bactérien peut être dirigé en changeant la direction du vecteur du champ magnétique tournant, car le VTT translate dans le plan de rotation (en bas). Pour un vecteur RMF autour de l'axe x, les bactéries tournent le long de y, générer un flux qui transporte les NP le long de y. (D) La vitesse de translation est tracée en fonction de la fréquence de rotation appliquée à deux intensités de champ magnétique différentes. La vitesse de translation augmente avec la fréquence initialement, mais à des fréquences suffisamment élevées, il diminue car le couple de traînée fluidique surmonte le couple magnétique pour les empêcher de suivre la rotation du champ. La fréquence maximale synchronisée, correspondant également à la vitesse de translation maximale, est appelée fréquence de sortie ωmax. Lorsque l'intensité du champ magnétique est augmentée, la fréquence de sortie augmente, comme observé. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aav4803
Les scientifiques ont également développé un modèle d'écoulement de fluide unique dans un microcanal pour former un microvaisseau bioinspiré avec des échelles biomimétiques et des débits de fluide. Le modèle contenait du collagène concentré au centre qui imitait la matrice extracellulaire native. À l'aide de l'appareil, Schuerle et al. quantifié l'intensité de fluorescence dans la matrice biomimétique pour tester si l'ABF à commande magnétique pouvait améliorer le transport de masse des NP marquées par fluorescence dans la matrice imitant les tissus. Les résultats ont indiqué que les ABF étaient limités en tant que microhélice convective dans les petits navires, mais cela peut être modifié en adaptant la structure ABF à la taille du canal à l'avenir.
Les scientifiques ont ensuite examiné les effets de tout un essaim de petites hélices de microrobots. Pour ça, Schuerle et al. sélectionné la souche sauvage de MTB AMB-1 ( Magnetospirillum magnetum ) pour former des magnétosomes. Les micro-organismes produisaient naturellement des chaînes de particules d'oxyde de fer dans les bicouches lipidiques de la membrane plasmique pour un mouvement manipulé à l'aide de champs magnétiques externes. Alors que les chercheurs avaient utilisé des VTT dans des études précédentes comme véhicules potentiels d'administration de médicaments avec des champs magnétiques externes, Schuerle et al. utilisé des champs magnétiques rotationnels (RMF) dans le présent travail. Les RMF ont forcé le mouvement d'un essaim de VTT pour entraîner leur mouvement via un couple magnétique.
Contrôle du MTB marqué par fluorescence verte dans un dispositif microfluidique, lorsque RMF est activé/désactivé. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aav4803
Les scientifiques ont réduit la distance moyenne entre les bactéries en utilisant une forte concentration de VTT pour pousser les voisines cellulaires vers l'avant dans des essaims 3D dominés par les forces hydrodynamiques. Ils n'ont pas observé de regroupement ou d'agrégation des magnétosomes du VTT lorsqu'ils étaient exposés aux RMF, car les magnétosomes étaient intrinsèquement protégés par les membranes cellulaires bactériennes pour un flux de fluide contrôlé. Schuerle et al. répété les expériences de biomimétisme à l'aide d'un dispositif microfluidique contenant du collagène pour montrer que les essaims de VTT pouvaient pénétrer le collagène, lorsque des concentrations suffisamment élevées de VTT ont été utilisées.
De cette façon, en utilisant deux stratégies expérimentales Schuerle et al. amélioré le transport de masse des NPs, via un flux convectif généré par des microhélices à commande magnétique. Les expériences de microrobotique ont montré que l'ABF imitait un flagelle bactérien pour aider à l'accumulation et à la pénétration de NP dans une matrice de collagène dense - lorsqu'il était sollicité par les RMF. Schuerle et al. proposent d'inclure de tels ABF stationnaires dans les stents pour déclencher la libération du médicament et améliorer la pénétration sur un site d'intérêt pour contrer l'inflammation à la demande.
Avec la deuxième stratégie, ils se sont concentrés sur la génération de la même technique mais avec des souches bactériennes magnétotactiques (MTB). Sur la base du présent travail et des propriétés existantes de tumor-homing des VTT, les scientifiques envisagent des essaims contrôlés magnétiquement de VTT 3-D pour transporter les NP dans l'espace de liquide interstitiel des microenvironnements tumoraux. Les scientifiques optimiseront la densité des bactéries pour une dose compatible in vivo et les travaux ouvriront la voie à d'autres études sur les micro- et nanomatériaux pour le transport magnétiquement amélioré des NP en nanomédecine clinique.
© 2019 Réseau Science X