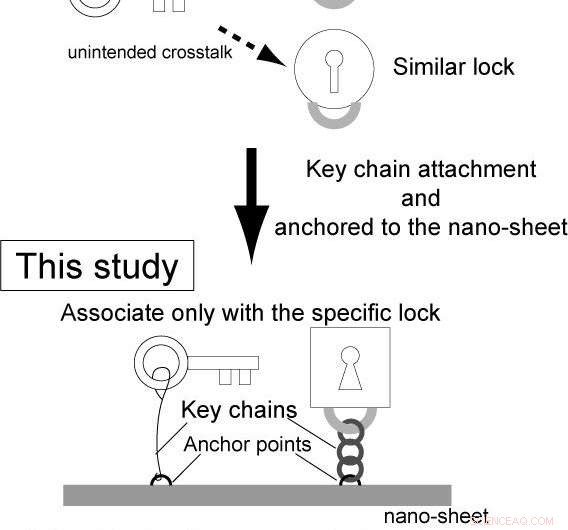
Fig. 1 Effet de l'approche d'intégration. Crédit :Hisasi Tadakuma / Université d'Osaka
L'expression des gènes est un élément fondamental de la vie, où chaque cellule active et désactive des gènes spécifiques. Ainsi, un dispositif autonome qui pourrait contrôler la commutation marche-arrêt aurait une grande valeur dans les soins médicaux.
Les circuits génétiques synthétiques sont une technologie permettant de contrôler l'expression des gènes et de programmer les cellules pour qu'elles remplissent les fonctions souhaitées. Par conséquent, l'augmentation de la complexité du circuit génétique nous permettra de contrôler plus précisément le destin des cellules.
Cependant, la complexité des circuits génétiques reste faible. Ceci est dû au fait, dans les systèmes classiques de réaction-diffusion, les enzymes et les substrats sont fournis séparément, et la liaison non spécifique des enzymes aux substrats provoque une diaphonie involontaire entre les différents circuits.
Chercheurs dirigés par l'Université d'Osaka, dans un projet de recherche conjoint avec l'Université de Tokyo, Université de Kyoto, et l'Université Waseda, construit des puces logiques génétiques intégrées appelées « nanopuces génétiques ». En utilisant des facteurs intégrés sur les nanopuces, ces nanopuces autonomes peuvent activer et désactiver des gènes au sein d'une seule puce, empêchant la diaphonie involontaire.
Les chercheurs ont montré les réponses autonomes des nanopuces dans des cellules artificielles :détection environnementale, calcul de l'information et sortie de produit au niveau de la puce unique. Les résultats de leurs recherches ont été publiés dans Nature Nanotechnologie .
La nanotechnologie de l'ADN est une méthode polyvalente utilisée pour construire des structures personnalisées et pour contrôler des dispositions moléculaires précises. Les chercheurs ont utilisé une feuille rectangulaire (90 nm de large, 60 nm de profondeur, 2 nm de haut), et enzyme intégrée, ARN polymérase (RNAP, une enzyme qui synthétise l'ARN à partir d'une matrice d'ADN), et de multiples substrats de gènes cibles.
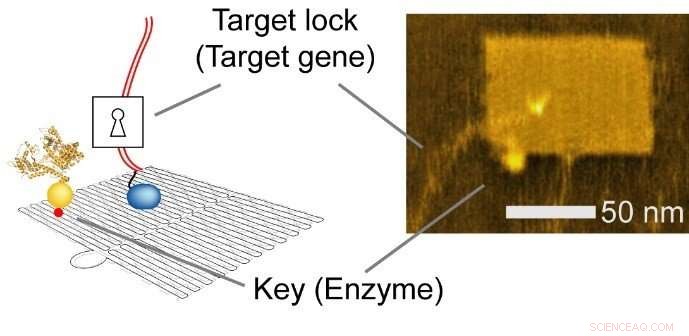
Fig. 2 Nanopuce intégrée. La gauche, Illustration schématique. Droit, image de microscopie à force atomique (AFM). Crédit :Hisashi Tadakuma / Université d'Osaka
La capacité de nano-disposition de la nanotechnologie de l'ADN permet au chercheur de concevoir rationnellement les niveaux d'expression des gènes en modifiant les distances intermoléculaires entre l'enzyme et les gènes cibles, affectant ainsi l'efficacité de la collision et la réaction ultérieure.
Les chercheurs ont en outre intégré des capteurs. Idéalement, un capteur capable de détecter tout type de signal doit avoir des limitations de conception minimales. Cependant, les méthodes conventionnelles ont souffert de plusieurs limitations (par exemple, matériaux). Ceci est dû au fait, dans les circuits génétiques conventionnels, le capteur fait partie du substrat de l'enzyme (par exemple, ADN en transcription; voir la note pour plus de détails).
Inversement, dans cette étude, la partie capteur était indépendante de la réaction enzymatique. Ainsi, les chercheurs peuvent utiliser n'importe quel matériau de capteur qui modifie la distance intermoléculaire effective lors de la reconnaissance du signal, permettant la construction de divers capteurs répondant à des signaux distincts (microARN, composants chimiques, protéines et lumière). De plus, en combinant et intégrant des capteurs répondant à des signaux distincts, les chercheurs ont réussi une photo-reprogrammation des circuits génétiques.
Finalement, la nanopuce a permis aux chercheurs de simplifier la construction d'un circuit génétique répondant à une cellule artificielle, une goutte d'eau dans l'huile, et ils pourraient calculer son profil de miARN, en mélangeant simplement les copeaux orthogonaux, étendre la puissance du circuit génétique.
L'auteur correspondant Hisashi Tadakuma dit :"Tous les facteurs nécessaires aux réactions de transcription sont sur cette nanopuce intégrée, donc la détection de l'environnement, calcul d'informations, et la sortie du produit peut être complétée au niveau de la puce unique. Dans le futur proche, les nanopuces autonomes seront utiles pour maintenir la cellule dans un état sain en contrôlant l'expression des gènes dans l'espace et dans le temps, qui incarnera l'idéal du dicton « la prévention est le meilleur remède ». "
Idéalement, un capteur capable de détecter tout type de signal doit avoir des limitations de conception minimales. Cependant, les méthodes conventionnelles ont souffert de plusieurs limitations (par exemple, matériaux). Ceci est dû au fait, dans les circuits génétiques conventionnels, l'efficacité de liaison entre une enzyme telle que RNAP (clé) et un gène cible (target lock), spécifiquement une séquence promotrice sur la molécule d'ADN, est contrôlé par des facteurs de transcription (régulateurs). Comme les régulateurs et les enzymes doivent se lier au capteur (région opérateur) près du verrou cible, le matériau du capteur doit être un substrat des régulateurs et des enzymes (par exemple, ADN en transcription), et le régulateur devrait être une protéine de liaison à l'ADN. Ainsi, le régulateur (signal) et le capteur ont des limitations matérielles.
Cependant, dans cette étude, la fréquence de liaison et la réaction ultérieure sont contrôlées par (1) la distance intermoléculaire entre une enzyme et un gène cible, et (2) les caractéristiques du porte-clés (par exemple, rigidité, longueur). Ainsi la partie capteur est indépendante de la réaction enzymatique, et le capteur et les régulateurs n'ont pas de limitations matérielles, permettant aux différents capteurs de répondre à des signaux distincts (composés chimiques, protéines et lumière).