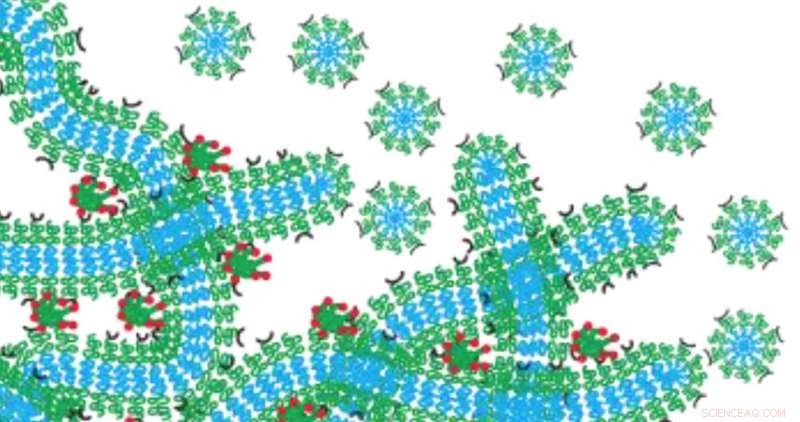
Le réseau d'hydrogel d'Evan Scott fonctionne comme un dépôt de médicament qui se dégrade lentement en se décomposant en micelles. Crédit :Université Northwestern
Parce qu'ils peuvent être programmés pour parcourir le corps et cibler sélectivement le cancer et d'autres sites de maladie, des véhicules à l'échelle nanométrique appelés nanocarriers peuvent administrer des concentrations plus élevées de médicaments pour bombarder des zones spécifiques du corps tout en minimisant les effets secondaires systémiques. Les nanotransporteurs peuvent également administrer des médicaments et des agents de diagnostic qui ne sont généralement pas solubles dans l'eau ou le sang, ainsi que réduire considérablement la dose efficace.
Bien que cette méthode puisse sembler idéale pour traiter les maladies, les nanotransporteurs ne sont pas sans défis.
"Contrôlé, l'accouchement prolongé est avantageux pour le traitement de nombreux troubles chroniques, mais cela est difficile à réaliser avec des nanomatériaux sans induire une inflammation locale indésirable, " a déclaré Evan Scott de l'Université Northwestern. " Au lieu de cela, les nanomatériaux sont généralement administrés sous forme d'injections séparées multiples ou sous forme de transfusion qui peut prendre plus d'une heure. Ce serait formidable si les médecins pouvaient faire une seule injection, qui a libéré en continu des nanomatériaux sur une période de temps contrôlée."
Maintenant Scott, professeur adjoint de génie biomédical à la McCormick School of Engineering de Northwestern, a développé un nouveau mécanisme qui permet de contrôler, livraison soutenue possible.
L'équipe de Scott a conçu une formulation de nanosupport qui, après s'être rapidement formée en un gel à l'intérieur du corps au site d'injection, peut libérer en continu des véhicules chargés de médicaments à l'échelle nanométrique pendant des mois. Le gel lui-même se réassemble dans les nanoporteurs, donc après que tout le médicament a été délivré, aucun matériau résiduel n'est laissé pour induire une inflammation ou la formation de tissu fibreux. Ce système pourrait, par exemple, permettre des vaccins à administration unique qui ne nécessitent pas de rappel ainsi qu'une nouvelle façon d'administrer la chimiothérapie, hormonothérapie, ou des médicaments qui facilitent la cicatrisation des plaies.
Soutenu par la National Science Foundation et les National Institutes of Health, la recherche a été publiée en ligne aujourd'hui, 12 février dans le journal Communication Nature . Nicolas Karabin, un étudiant diplômé du laboratoire de Scott, était le premier auteur de l'article. Kenneth Shull de Northwestern Engineering, professeur de science et génie des matériaux, également contribué aux travaux. Membre du Simpson Querrey Institute for BioNanotechnology and Chemistry of Life Processes Institute de Northwestern, Scott était l'auteur correspondant et a dirigé le développement des nanoparticules et la validation in vivo.
Actuellement, les systèmes d'administration de nanotransporteurs soutenus les plus courants contiennent des nanomatériaux dans des matrices polymères. Ces réseaux sont implantés dans le corps, où ils libèrent lentement les porteurs de drogue piégés sur une période de temps. Le problème se situe une fois l'accouchement terminé :les réseaux restent à l'intérieur du corps, provoquant souvent une réaction de corps étranger. Le réseau restant peut provoquer une gêne et une inflammation chronique chez le patient.
Pour contourner ce problème, Scott a développé un nanosupport en utilisant des nanomatériaux en forme de filament, qui sont chargés d'un médicament ou d'un agent d'imagerie. Lorsqu'ils sont réticulés ensemble, les filaments forment un réseau d'hydrogel semblable au tissu structurel du corps humain. Une fois les filaments injectés dans le corps, le réseau d'hydrogel résultant fonctionne comme un dépôt de médicament qui se dégrade lentement en se décomposant en nanomatériaux sphériques appelés micelles, qui sont programmés pour voyager vers des cibles spécifiques. Parce que le réseau se transforme en système de distribution de médicaments, rien n'est moins en retard pour provoquer une inflammation.
« Tout le matériel contient le médicament puis délivre le médicament, " expliqua Scott. " Il se dégrade de façon contrôlée, résultant en des nanomatériaux de forme et de taille égales. Si nous chargeons un médicament dans les filaments, les micelles prennent le médicament et repartent avec."
Après avoir testé le système à la fois in vitro et in vivo dans un modèle animal, L'équipe de Scott a démontré qu'elle pouvait administrer une injection sous-cutanée qui livrait lentement des nanomatériaux aux cellules des ganglions lymphatiques pendant plus d'un mois de manière contrôlée.
Scott a déclaré que le système peut être utilisé pour d'autres nanostructures en plus des micelles. Par exemple, le système pourrait inclure des nanoparticules en forme de vésicule, tels que les liposomes ou les polyersomes, qui ont de la drogue, protéines, ou des anticorps piégés à l'intérieur. Différentes vésicules pourraient transporter différents médicaments et les libérer à des vitesses différentes une fois à l'intérieur du corps.
« Ensuite, nous cherchons des moyens d'adapter le système aux besoins de maladies et de thérapies spécifiques, " a déclaré Scott. "Nous travaillons actuellement pour trouver des moyens de fournir des produits chimiothérapeutiques et des vaccins. La chimiothérapie nécessite généralement l'administration de plusieurs médicaments toxiques à des concentrations élevées, et nous pourrions livrer tous ces médicaments en une seule injection à des doses beaucoup plus faibles. Pour la vaccination, ces hydrogels injectables pourraient être administrés comme des vaccins standards, mais stimulent des cellules spécifiques du système immunitaire plus longtemps, des périodes de temps contrôlées et évitent potentiellement le besoin de boosters."