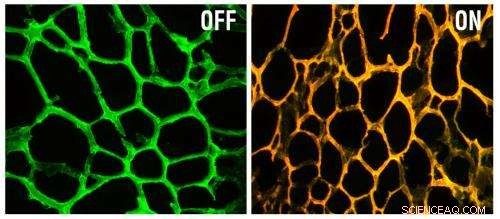
A gauche se trouve le nouveau nanodispositif, consistant en un hydrogel incrusté de nanoparticules d'or recouvertes d'ADN ciblant un gène appelé MRP-1. A droite, le dispositif émet une fluorescence après avoir rencontré la séquence du gène cible. Crédit :Avec l'aimable autorisation des chercheurs
La chimiothérapie rétrécit souvent les tumeurs au début, mais à mesure que les cellules cancéreuses deviennent résistantes au traitement médicamenteux, les tumeurs peuvent repousser. Un nouveau nanodispositif développé par des chercheurs du MIT peut aider à surmonter cela en bloquant d'abord le gène qui confère la résistance aux médicaments, puis lancer une nouvelle attaque de chimiothérapie contre les tumeurs désarmées.
Le dispositif, qui est constitué de nanoparticules d'or noyées dans un hydrogel pouvant être injecté ou implanté au niveau d'un site tumoral, pourrait également être utilisé plus largement pour perturber tout gène impliqué dans le cancer.
"Vous pouvez cibler n'importe quel marqueur génétique et délivrer un médicament, y compris ceux qui n'impliquent pas nécessairement des voies de résistance aux médicaments. C'est une plateforme universelle de bithérapie, " dit Nathalie Artzi, chercheur à l'Institute for Medical Engineering and Science (IMES) du MIT, professeur assistant à la Harvard Medical School, et auteur principal d'un article décrivant l'appareil dans le Actes de l'Académie nationale des sciences la semaine du 2 mars.
Pour démontrer l'efficacité de la nouvelle approche, Artzi et ses collègues l'ont testé sur des souris implantées avec un type de tumeur mammaire humaine connue sous le nom de tumeur triple négative. De telles tumeurs, qui manque l'un des trois marqueurs du cancer du sein les plus courants :le récepteur des œstrogènes, récepteur de progestérone, et Her2—sont généralement très difficiles à traiter. En utilisant le nouveau dispositif pour bloquer le gène de la protéine multirésistante 1 (MRP1), puis administrer le médicament chimiothérapeutique 5-fluorouracile, les chercheurs ont pu réduire les tumeurs de 90 pour cent en deux semaines.
Vaincre la résistance
MRP1 est l'un des nombreux gènes qui peuvent aider les cellules tumorales à devenir résistantes à la chimiothérapie. MRP1 code pour une protéine qui agit comme une pompe, éliminer les médicaments anticancéreux des cellules tumorales et les rendre inefficaces. Cette pompe agit sur plusieurs médicaments autres que le 5-fluorouracile, y compris la doxorubicine, un médicament anticancéreux couramment utilisé.
"La résistance aux médicaments est un énorme obstacle dans le traitement du cancer et la raison pour laquelle la chimiothérapie, dans de nombreux cas, n'est pas très efficace", dit João Conde, un post-doctorant IMES et auteur principal de l'article PNAS.
Pour surmonter cela, les chercheurs ont créé des nanoparticules d'or recouvertes de brins d'ADN complémentaires à la séquence d'ARN messager MRP1, l'extrait de matériel génétique qui transmet les instructions de l'ADN au reste de la cellule.
Ces brins d'ADN, que les chercheurs appellent des « nanobalises, " se replient sur eux-mêmes pour former une structure en épingle à cheveux fermée. Cependant, lorsque l'ADN rencontre la séquence d'ARNm correcte à l'intérieur d'une cellule cancéreuse, il se déplie et se lie à l'ARNm, l'empêchant de générer plus de molécules de la protéine MRP1. Au fur et à mesure que l'ADN se déploie, il libère également des molécules de 5-fluorouracile qui étaient incrustées dans le brin. Ce médicament attaque alors l'ADN de la cellule tumorale, puisque MRP1 n'est plus là pour le pomper hors de la cellule.
"Quand on fait taire le gène, la cellule n'est plus résistante à ce médicament, afin que nous puissions délivrer le médicament qui retrouve désormais son efficacité, " dit Condé.
Lorsque chacun de ces événements se produit - détection de la protéine MRP1 et libération de 5-fluorouracile - le dispositif émet une fluorescence de différentes longueurs d'onde, permettant aux chercheurs de visualiser ce qui se passe à l'intérieur des cellules. À cause de ce, les particules pourraient également être utilisées pour le diagnostic, en particulier, déterminer si un certain gène lié au cancer est activé dans les cellules tumorales.
Libération contrôlée de médicament
Les nanoparticules d'or recouvertes d'ADN sont intégrées dans un gel adhésif qui reste en place et recouvre la tumeur après son implantation. Cette administration locale des particules les protège de la dégradation qui pourrait se produire si elles étaient administrées dans tout l'organisme, et permet également une libération prolongée du médicament, dit Artzi.
Dans leurs études sur la souris, les chercheurs ont découvert que les particules pouvaient faire taire MRP1 jusqu'à deux semaines, avec une libération continue du médicament pendant cette période, rétrécissant efficacement les tumeurs.
Cette approche pourrait être adaptée pour délivrer tout type de médicament ou de thérapie génique ciblé sur un gène spécifique impliqué dans le cancer, disent les chercheurs. Ils travaillent maintenant à l'utiliser pour faire taire un gène qui stimule la métastase des tumeurs gastriques dans les poumons.