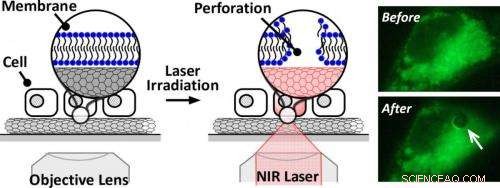
Les membranes cellulaires peuvent être manipulées en irradiant un film mince de nanotubes de carbone avec un laser proche infrarouge (NIR). Crédit :Science et technologie des matériaux avancés
Des chercheurs japonais ont mis au point un nouveau méthode ciblée de perforation des membranes cellulaires afin d'administrer des médicaments à, ou manipuler les gènes de, cellules individuelles. L'article est publié dans la revue Science et technologie des matériaux avancés .
La méthode implique l'irradiation laser proche infrarouge (NIR) d'un film mince de nanotubes de carbone, qui agissent comme un absorbeur de photons efficace ainsi qu'un générateur de stimulus.
Dans la recherche en génie cellulaire et en biologie tissulaire, l'utilisation de lasers pulsés pour stimuler les cellules est devenue une technique puissante pour permettre la transfection sélective de gènes, l'injection de drogue ou la régulation de l'expression des gènes. L'irradiation de cellules biologiques à l'aide de lasers pulsés provoque la perforation de leurs membranes, qui accélère considérablement la transfection de gènes ou l'administration ciblée de médicaments.
Parmi la large gamme d'énergies photoniques, la région proche infrarouge est moins nocive pour les cellules biologiques, qui absorbent très peu d'énergie dans ces longueurs d'onde. Les lasers NIR les plus performants sont les lasers femtosecondes en raison de leur résolution spatiale fine sans dommages thermiques ou mécaniques aux matériaux environnants. Mais les instruments laser femtoseconde sont chers et nécessitent un agencement optique très sophistiqué et beaucoup d'espace, l'équipe de recherche a donc opté pour un laser nanoseconde plus économique.
Dans l'étude, Naotoshi Nakashima et ses collègues de l'Université de Kyushu ont utilisé un plat recouvert de nanotubes de carbone à paroi unique (SWCNT), qui absorbent fortement le rayonnement dans la région NIR, comme antenne pour un laser à impulsions nanosecondes. L'équipe a découvert que les membranes cellulaires étaient perturbées de manière réversible ou irréversible à la suite d'une impulsion NIR, en fonction de l'énergie du laser. Lorsqu'un pouls dépassait 17,5 microjoules, la membrane a été irréversiblement rompue et la cellule est morte. Par contre, à environ 15 microJoules par impulsion, la membrane s'ouvrit et la cellule resta vivante.
Cela suggère qu'une source laser peu coûteuse pourrait être utilisée pour préparer une cible cellulaire unique pour la transfection sélective de gènes, injection de médicament ou régulation de l'expression des gènes, concluent les auteurs.