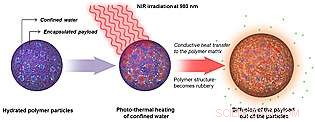
Dans cette représentation schématique, une nanoparticule polymère hydratée est exposée à une lumière proche infrarouge. Le NIR chauffe des poches d'eau à l'intérieur de la nanoparticule, provoquant le ramollissement du polymère et permettant aux molécules encapsulées de se diffuser dans le milieu environnant. Crédit:UC San Diego School of Medicine
Des chercheurs de l'Université de Californie, École de pharmacie et des sciences pharmaceutiques Skaggs de San Diego, en collaboration avec des scientifiques des matériaux, ingénieurs et neurobiologistes, ont découvert un nouveau mécanisme d'utilisation de la lumière pour activer des nanoparticules et d'autres substances thérapeutiques ciblées à l'intérieur du corps.
Cette découverte représente une innovation majeure, dit Adah Almutairi, Doctorat, professeur agrégé et directeur du centre d'excellence conjoint UC San Diego-KACST en nanomédecine. Jusqu'à maintenant, elle a dit, seule une poignée de stratégies utilisant la libération déclenchée par la lumière à partir de nanoparticules ont été rapportées.
Le mécanisme, décrit dans le 1er avril édition en ligne 2014 de ACS Nano , utilise la lumière proche infrarouge (NIR) d'un laser de faible puissance pour chauffer des poches d'eau piégées dans des nanoparticules polymères non photosensibles infusées de médicaments. Les poches d'eau absorbent l'énergie lumineuse sous forme de chaleur, qui ramollit le polymère d'encapsulation et permet au médicament d'être libéré dans le tissu environnant. Le processus peut être répété plusieurs fois, avec un contrôle précis de la quantité et de la dispersion du médicament.
"Un avantage clé de ce mécanisme est qu'il devrait être compatible avec presque tous les polymères, même ceux qui sont disponibles dans le commerce, " a déclaré Mathieu Viger, un boursier post-doctoral dans le laboratoire d'Almutairi et co-auteur principal de l'étude. "Nous avons observé le piégeage de l'eau dans des particules composées de tous les polymères biodégradables que nous avons testés jusqu'à présent."
La méthode, a noté Viger, pourrait ainsi être facilement adopté par de nombreux laboratoires de biologie.
L'utilisation combinée de polymères hydratés et de lumière proche infrarouge semble résoudre une multitude de barrières technologiques et sanitaires qui ont entravé les précédents, approches similaires. Les efforts antérieurs pour utiliser la libération déclenchée par NIR n'ont pas été largement exploités car ils nécessitaient des polymères de conception spéciaux, lasers de forte puissance coûteux et/ou la co-encapsulation de particules inorganiques dont la sécurité dans l'organisme reste sujette à caution.
La nouvelle méthode décrite par Almutairi et ses collègues des départements de génie mécanique et aérospatial, Neurosciences, et la chimie et la biochimie de l'UC San Diego utilisent le NIR à une longueur d'onde vibratoire pour exciter les molécules d'eau, qui absorbent l'énergie optique et la convertissent en chaleur. Le NIR est capable de pénétrer les tissus biologiques à des profondeurs plus importantes que la lumière visible ou ultraviolette.
Co-auteur principal Wangzhong Sheng, un étudiant diplômé au Département de génie mécanique et aérospatial, a expliqué la sélectivité du chauffage en comparant l'eau piégée dans les particules à un verre d'eau et l'eau environnante dans la solution ou le tissu à une baignoire. La plus petite quantité d'eau est chauffée beaucoup plus rapidement en raison de l'énorme différence de volume.
Une utilisation évidente de la méthode, dit Almutairi, est l'administration de médicaments déclenchée par la lumière, mais avec plus de recherche, elle anticipe que la nouvelle méthode pourrait fournir une variété de produits industriels, applications médicales et scientifiques, comprenant « toute application technologique nécessitant que la chimie soit maîtrisée dans le temps et dans l'espace, comme dans les matériaux de catalyse ou d'auto-réparation ou les écrans solaires activés par la lumière ou le dosage de pesticides."