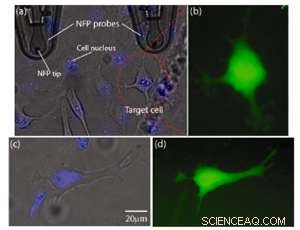
Transfection du colorant dextran Alexa Fluor 488 dans une cellule HeLa ciblée en utilisant l'électroporation de sonde Nanofountain. Réimprimé avec la permission de Nano Letters. Copyright 2013 Société chimique américaine.
(Phys.org) —Les chercheurs de l'Université Northwestern ont développé une nouvelle méthode pour livrer des molécules en un seul, cellules ciblées à travers des trous temporaires dans la surface cellulaire. La technique pourrait trouver des applications dans l'administration de médicaments, thérapie cellulaire, et les domaines biologiques connexes.
L'électroporation en vrac, une technique utilisée pour introduire des molécules dans les cellules à travers des nanopores réversibles dans la membrane cellulaire, provoqués par leur exposition à des impulsions électriques, est une méthode de transfection cellulaire de plus en plus populaire. (La transfection cellulaire est l'introduction de molécules, tels que les acides nucléiques ou les protéines, dans une cellule pour modifier ses propriétés.)
Cependant, parce que l'électroporation en vrac applique des impulsions électriques à une solution de cellule en vrac, il en résulte des populations cellulaires hétérogènes et souvent une faible viabilité cellulaire. Pour résoudre ces problèmes, Des chercheurs de la Northwestern University ont développé un nouvel outil pour la transfection unicellulaire.
La nouvelle méthode, appelée électroporation par sonde nanofontaine (NFP-E), permet aux chercheurs de délivrer des molécules dans des cellules ciblées à travers des nanopores temporaires dans la membrane cellulaire créés par un champ électrique localisé appliqué à une petite partie de la cellule. La méthode permet aux chercheurs de contrôler le dosage en faisant varier la durée des impulsions électriques, qui offre un contrôle sans précédent de la transfection cellulaire.
"C'est vraiment excitant, " dit Horacio Espinosa, James et Nancy Farley, professeur de fabrication et d'entrepreneuriat à la McCormick School of Engineering de Northwestern et l'un des auteurs de l'article. « La capacité de fournir avec précision des molécules dans des cellules individuelles est nécessaire pour que les chercheurs en biotechnologie fassent progresser l'état de l'art en matière de thérapie, Diagnostique, et l'administration de médicaments vers la promesse d'une médecine personnalisée."
Un article décrivant la recherche, "Électroporation par sonde nanofontaine (NFP-E) de cellules individuelles, " a été publié le 7 mai dans la revue Lettres nano .
NFP-E est basé sur la technologie de sonde nanofontaine (NFP) développée dans le laboratoire d'Espinosa. La puce NFP-E se compose d'un réseau de sondes en porte-à-faux microfabriquées avec des canaux microfluidiques intégrés. La sonde a déjà été utilisée pour la nanostructuration à grande vitesse de protéines et de nanoparticules pour des études d'administration de médicaments.
La nouvelle application de transfection unicellulaire couple la sonde avec une électrode et un système de contrôle des fluides qui peuvent être facilement connectés à un micromanipulateur ou à un microscope à force atomique pour le contrôle de la position. Ce système intégré permet de surveiller l'ensemble du processus de transfection et la réponse cellulaire post-transfection par un microscope optique.
Le système NFP-E est développé pour être commercialisé par iNfinitesimal LLC, une entreprise dérivée du Nord-Ouest fondée par Espinosa, et devrait être disponible fin 2013.
La technique s'avère extrêmement robuste et multifonctionnelle. Des chercheurs ont utilisé la puce NFP-E pour transfecter des cellules HeLa avec des polysaccharides, protéines, épingles à cheveux ADN, et de l'ADN plasmidique à sélectivité unicellulaire, haute efficacité de transfection (jusqu'à 95%), contrôle qualitatif du dosage, et une viabilité très élevée (jusqu'à 92%).