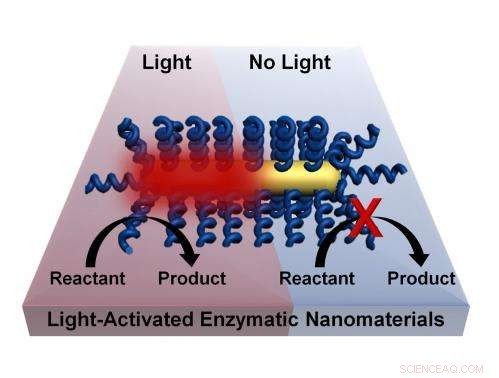
Les processus chimiques peuvent être activés par la lumière sans avoir besoin de chauffer en vrac un matériau grâce à un processus développé par des chercheurs de l'Université Rice. La technique consiste à revêtir des nanotiges d'enzymes thermophiles qui sont activées à haute température. L'éclairage de la nanotige en or plasmonique provoque un échauffement très localisé et active l'enzyme. Crédit :Lori Pretzer/Université Rice
(Phys.org)—Depuis la première ampoule d'Edison, la chaleur a été un sous-produit la plupart du temps indésirable de la lumière. Aujourd'hui, les chercheurs de l'Université Rice transforment la lumière en chaleur là où c'est nécessaire, à l'échelle nanométrique, pour déclencher des réactions biochimiques à distance à la demande.
La méthode créée par les Rice labs de Michael Wong, Ramon Gonzalez et Naomi Halas et rapportés aujourd'hui dans le journal de l'American Chemical Society ACS Nano utilise des matériaux dérivés de microbes uniques - thermophiles - qui se développent à des températures élevées mais s'arrêtent à température ambiante.
Le projet Rice dirigé par le boursier postdoctoral Matthew Blankschien et l'étudiante diplômée Lori Pretzer combine les enzymes de ces créatures avec des nanoparticules d'or plasmoniques qui chauffent lorsqu'elles sont exposées à la lumière proche infrarouge. Qui active les enzymes, qui sont alors en mesure d'exercer leurs fonctions.
Cela permet effectivement aux processus chimiques de se produire à des températures plus basses. Parce que le chauffage ne se produit que là où cela est nécessaire - à la surface de la nanoparticule, où il active l'enzyme - l'environnement reste plus frais.
Blankschien trouve cela fascinant.
"Essentiellement, nous bénéficions des avantages de la fabrication à haute température sans avoir besoin d'un environnement à haute température, " dit Blankschien, qui a remporté la bourse postdoctorale Peter et Ruth Nicholas il y a deux ans pour travailler sur ces idées. "Le défi était de maintenir la température plus élevée au niveau de la nanoparticule, où l'enzyme est activée, d'affecter l'environnement qui l'entoure."
La technique recèle un grand potentiel pour les procédés industriels qui nécessitent désormais de la chaleur ou bénéficient d'un déclenchement à distance avec la lumière.
"Les implications sont assez excitantes, " dit Wong, professeur de génie chimique et biomoléculaire et de chimie. « Dans l'industrie chimique, il y a toujours un besoin de meilleurs matériaux catalytiques afin qu'ils puissent exécuter des réactions à moindre coût, plus 'vert' et plus durable. Vous ne devriez pas utiliser des gallons de solvant pour faire un milligramme de produit, même s'il vous arrive de pouvoir le vendre pour beaucoup d'argent."
Pour l'industrie, les économies d'énergie potentielles à elles seules peuvent rendre le procédé Rice intéressant à étudier. "Ici, nous utilisons de l'énergie 'gratuite', " dit Wong. " Au lieu d'avoir besoin d'une grosse chaudière pour produire de la vapeur, vous allumez une ampoule économe en énergie, comme une LED. Ou ouvrez une fenêtre."
La particule au centre du processus est une nanotige d'or d'environ 10 nanomètres de large et 30 de long qui se réchauffe lorsqu'elle est touchée par la lumière proche infrarouge d'un laser. Les tiges ont juste la bonne taille et la bonne forme pour réagir à la lumière à environ 800 nanomètres. La lumière excite les plasmons de surface qui ondulent comme l'eau d'une piscine, dans ce cas émettant de l'énergie sous forme de chaleur.
Le laboratoire Rice de Halas est célèbre pour avoir été le pionnier de l'utilisation de nanocoquilles d'or (un matériau apparenté) pour traiter le cancer en ciblant les tumeurs avec des particules qui sont chauffées en masse pour tuer les tumeurs de l'intérieur. La thérapie est maintenant dans les essais humains.
La nouvelle recherche adopte une approche quelque peu différente en chauffant des nanoparticules drapées d'une enzyme thermophile modèle, glucokinase, de Aeropyrum pernix. A. pernix est un microbe découvert en 1996 qui prospérait près des évents sous-marins chauds au large des côtes du Japon. À environ 176 degrés Fahrenheit, A. pernix dégrade le glucose, un processus nécessaire à presque tous les êtres vivants. L'enzyme peut être chauffée et refroidie à plusieurs reprises.
Dans leurs expériences, Blankschien et Pretzer clonés, enzymes glucokinase purifiées et modifiées afin qu'elles se fixent aux nanoparticules d'or. Les complexes enzyme/nanoparticules ont ensuite été mis en suspension dans une solution et testés pour la dégradation du glucose. Lorsque la solution a été chauffée en vrac, ils ont découvert que les complexes devenaient très actifs à 176 degrés, comme prévu.
Ensuite, les complexes ont été encapsulés dans une bille de type gel d'alginate de calcium, ce qui aide à garder la chaleur mais est suffisamment poreux pour permettre aux enzymes de réagir avec les matériaux qui l'entourent. Sous chauffage en vrac, les performances des enzymes ont chuté de façon spectaculaire parce que les billes isolaient trop bien les enzymes.
Mais lorsque les complexes encapsulés étaient illuminés en continu, lumière laser proche infrarouge, ils ont fonctionné nettement mieux que sous chauffage en vrac tout en laissant la solution à température proche de la pièce. Les chercheurs ont trouvé les complexes suffisamment robustes pour des semaines de réutilisation.
"Aussi farfelu que cela puisse paraître, Je pense que les entreprises chimiques seront intéressées par l'idée d'utiliser la lumière pour fabriquer des produits chimiques, " a déclaré Wong. " Ils sont toujours intéressés par les nouvelles technologies qui peuvent aider à fabriquer des produits chimiques à moindre coût. "
Il voit d'autres utilisations possibles pour la nouvelle approche dans la production de carburants à partir de la dégradation de la biomasse comme la lignocellulose; pour la fabrication de médicaments à la demande – peut-être à partir de tatouages infusés de nanoparticules sur le corps ; ou même pour abaisser les concentrations de sucre dans le sang comme une façon différente de gérer le diabète.
« Que nous puissions maintenant fabriquer ces particules est formidable, " a déclaré Wong. " La prochaine partie passionnante est de réfléchir à la façon dont nous pouvons les déployer. "
Ryan Huschka, un co-auteur de l'article, est un ancien étudiant diplômé de Rice et maintenant professeur adjoint de chimie à l'Université Newman. Halas est le professeur Stanley C. Moore en génie électrique et informatique, professeur de génie biomédical, chimie, physique et astronomie et directeur du Laboratoire Rice pour la nanophotonique. Gonzales est professeur agrégé de génie chimique et biomoléculaire et également de bio-ingénierie
La recherche a été financée par le programme de bourses postdoctorales Peter et Ruth Nicholas administré par le Richard E. Smalley Institute for Nanoscale Science and Technology, le Rice University Institute of Biosciences and Bioengineering Hamill Innovations Award Program, le Fonds d'initiatives facultaires de l'Université Rice, la Fondation Robert A. Welch, la bourse de la faculté des sciences et de l'ingénierie de la sécurité nationale, l'Agence de réduction des menaces pour la défense, le Bureau de la recherche scientifique de l'Air Force et la National Science Foundation.