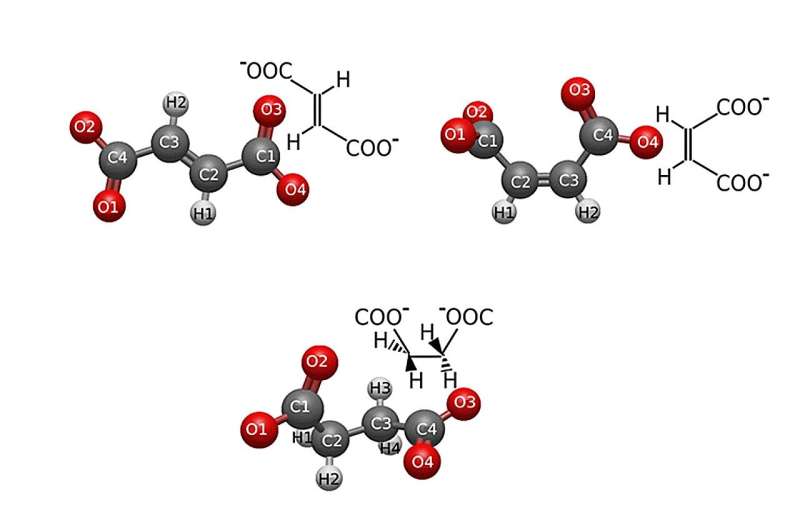
Les dianions de l'acide carboxylique (fumarate, maléate et succinate) jouent un rôle dans la chimie de coordination et, dans une certaine mesure, également dans la biochimie des cellules du corps. Une équipe HZB de BESSY II a maintenant analysé leurs structures électroniques à l'aide de RIXS en combinaison avec des simulations DFT. Les résultats fournissent des informations non seulement sur les structures électroniques, mais également sur la stabilité relative de ces molécules, qui peuvent influencer le choix d'une industrie en matière de dianions carboxylates, optimisant à la fois la stabilité et la géométrie des polymères de coordination.
Dianions d'acide carboxylique de type C4 H2 O4 ou C4 H4 O4 (fumarate, maléate et succinate) peuvent avoir différentes géométries (cis ou trans) et différentes propriétés. Certaines variantes sont essentielles à la chimie de coordination, incorporant des éléments métalliques dans des composés organiques ; d'autres jouent un rôle dans les processus biologiques.
Le fumarate et le succinate, par exemple, sont formés comme produits intermédiaires dans les mitochondries des cellules. Le maléate, en revanche, qui ne se forme généralement pas lors de processus naturels, est utilisé dans des applications industrielles nécessitant des matériaux durables. Cependant, pour des raisons environnementales, la question se pose de savoir si ces composés sont éternels ou s'ils sont biodégradables.
La stabilité des dianions fumarate, maléate et succinate est non seulement influencée par leurs géométries moléculaires, mais également par la structure électronique des molécules, en particulier l'orbitale moléculaire occupée la plus élevée (HOMO) et l'orbitale moléculaire inoccupée la plus basse (LUMO). Cependant, l'influence des orbitales moléculaires sur la stabilité de ces molécules n'a pas été étudiée.
Aujourd'hui, une équipe du HZB dirigée par le professeur Alexander Föhlisch a élucidé l'influence de la structure électronique sur la stabilité des dianions fumarate, maléate et succinate.
"Nous avons analysé ces composés à BESSY II avec deux méthodes différentes et très puissantes", explique le Dr Viktoriia Savchenko, premier auteur de l'étude. La spectroscopie d'absorption des rayons X (XAS) peut être utilisée pour étudier les états électroniques inoccupés d'un système, tandis que la diffusion inélastique résonante des rayons X (RIXS) fournit des informations sur les orbitales les plus élevées occupées et sur les interactions entre les orbitales HOMO-LUMO. Les résultats peuvent être liés aux propriétés macroscopiques, notamment à la stabilité.
L'analyse des données spectrales montre que le maléate est potentiellement moins stable que le fumarate et le succinate. De plus :l'analyse explique également pourquoi :la densité électronique dans l'orbitale HOMO au niveau de la liaison C=C entre les groupes carboxylates pourrait conduire à une liaison plus faible du maléate avec des molécules ou des ions. Le fumarate et le succinate, en revanche, pourraient être plus stables car leurs orbitales HOMO sont également délocalisées.
"Cela signifie qu'il est possible que le maléate soit dégradé par certaines substances", explique Savchenko.
Les travaux sont publiés dans la revue Physical Chemistry Chemical Physics .
Plus d'informations : Viktoriia Savchenko et al, Structure électronique, liaison et stabilité des dianions fumarate, maléate et succinate issus de la spectroscopie à rayons X, Physique Chimie Physique Chimique (2023). DOI :10.1039/D3CP04348G
Informations sur le journal : Physique Chimie Physique Chimique
Fourni par l'Association Helmholtz des centres de recherche allemands