2 , et permettent d'obtenir un stockage d'énergie avec une haute compatibilité environnementale.
Dans la réduction électrochimique du CO 2 , il est connu que l'acide formique peut être obtenu avec un rendement faradique d'environ 50 à 60 % en utilisant l'étain (Sn) comme catalyseur cathodique. Cependant, afin de développer cette technologie pour une utilisation pratique, une amélioration supplémentaire de l'efficacité faradique et une réduction de la surtension sont nécessaires. Il y a beaucoup d'intérêt actif dans la recherche pour comprendre les principes de conception des catalyseurs pour permettre d'atteindre ces objectifs.
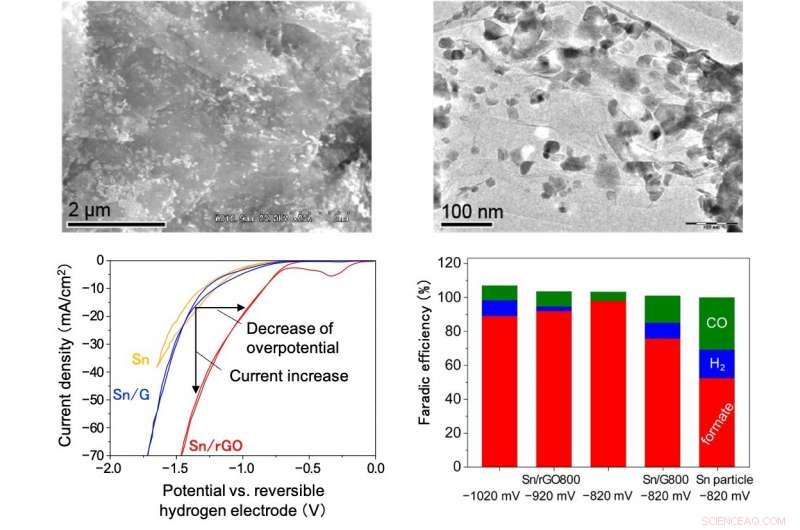
L'équipe de recherche actuelle dirigée par le professeur Tsujiguchi et ses collègues de l'Université de Kanazawa, en collaboration avec des scientifiques de l'Université de Tsukuba et de l'Université d'Osaka, a préparé un catalyseur à base d'oxyde de graphène réduit (Sn/rGO) dans lequel Sn était supporté sur de l'oxyde de graphite réduit par thermique. réduction du chlorure d'étain (SnCl 2 ) et de l'oxyde de graphène (GO) obtenu par oxydation de poudre de graphite selon la méthode améliorée de Hummers. Dans le catalyseur ainsi préparé, Sn est uniformément dispersé dans la couche rGO, et le composite est empilé pour former une morphologie 3-D, c'est-à-dire rGO/Sn/rGO.
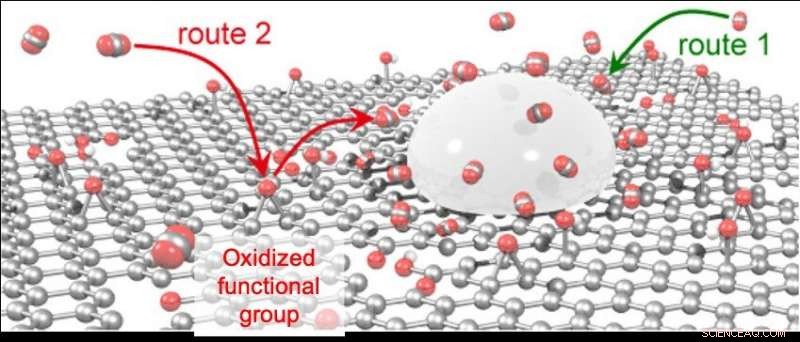
En plus de l'itinéraire conventionnel, c'est-à-dire le CO 2 directement adsorbé sur Sn (Route 1), CO 2 adsorbé sur les fonctions oxydées de rGO est fourni à Sn (Route 2). Crédit :Université de Kanazawa
Ce catalyseur est caractérisé comme un support avec un groupe fonctionnel contenant une quantité beaucoup plus importante d'oxygène que le catalyseur étain/graphite utilisé pour une comparaison. Lorsque nous avons effectué la réduction électrochimique du CO 2 en utilisant ces catalyseurs avec du CO 2 dissous dans une solution d'hydrogénocarbonate de potassium (KHCO 3 ), il a été constaté que le catalyseur Sn/rGO diminuait significativement la surtension et permettait d'obtenir une densité de courant élevée par rapport au catalyseur Sn. En outre, lorsque la réduction du CO 2 a été réalisée à potentiel constant, presque pas de produits autres que l'acide formique, comme H 2 et Cie, ont été détectés et nous avons réussi à obtenir de l'acide formique avec une efficacité faradique de 98 % (1,8 fois celle avec le catalyseur Sn seul).
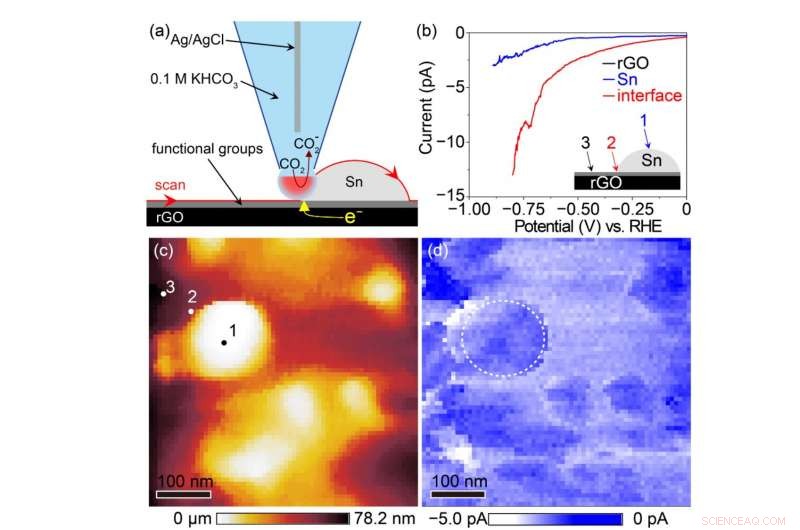
Schéma conceptuel de l'imagerie électrochimique Sn/rGO avec un microscope à cellule électrochimique à balayage (en haut à gauche), caractéristiques du CO 2 réduction sur la surface rGO, sur la surface Sn, et à l'interface entre Sn et rGO (en haut à droite), topographie au microscope électrochimique (en bas à gauche ; 1, sur la surface Sn; 2, à l'interface entre Sn et rGO; 3, sur la surface rGO) et cartographie du courant de réduction (en bas à droite). Cette figure montre que le CO 2 est efficacement réduit à l'interface entre Sn et rGO. Crédit :Université de Kanazawa
La raison de la production très efficace d'acide formique obtenue à l'aide du catalyseur Sn/rGO est sa teneur élevée en CO 2 capacité d'adsorption. Sn/rGO peut adsorber quatre fois plus de CO 2 comme catalyseur Sn seul. Plus loin, le taux de CO 2 l'adsorption est huit fois celle du catalyseur Sn seul. La chimie informatique a prédit que ce taux élevé de CO 2 la capacité d'adsorption serait due aux groupes fonctionnels oxydés de rGO et que la production d'hydrogène et de monoxyde de carbone serait supprimée puisque le CO 2 adsorbé par le groupe fonctionnel oxydé de rGO est fourni rapidement et efficacement à la surface adjacente de Sn.
Afin de confirmer expérimentalement ce mécanisme, notre équipe a tenté une imagerie électrochimique de l'activité catalytique avec un microscope à cellule électrochimique à balayage. Il a été révélé qu'une densité de courant de réduction significativement plus élevée a été observée à l'interface entre Sn et rGO que sur les surfaces Sn ou rGO (Fig. 3) suggérant qu'une grande quantité d'acide formique est synthétisée sur Sn adjacent à rGO, à l'appui de la prédiction ci-dessus par la chimie computationnelle. Il s'agit de la première démonstration expérimentale utilisant un microscope à cellule électrochimique à balayage que la synthèse d'acide formique se produit activement à l'interface entre le catalyseur et le support. Ainsi, une synthèse d'acide formique plus efficace serait possible en combinant un support à haute teneur en CO 2 capacité d'adsorption avec un catalyseur pour la réduction électrochimique du CO 2 . Cela fournit un cadre important qui pourrait être appliqué à tous les catalyseurs disponibles jusqu'à présent.
Les résultats de la présente étude fournissent de nouvelles informations sur le développement de catalyseurs pour la synthèse d'acide formique par la réduction de CO 2 , et des progrès spectaculaires sont attendus dans le développement de la technologie de synthèse de l'acide formique par la réduction électrochimique du CO 2 . En outre, nous avons démontré une amélioration de la sélectivité grâce à l'excellent CO 2 capacité d'adsorption du support ainsi que d'élucider son mécanisme de réaction. Cela devrait avoir un grand impact sur la technologie de réduction électrochimique liée au CO 2 , dont la synthèse de méthanol, méthane et oléfines. Par conséquent, il a le potentiel d'être une technologie de base utile dans la synthèse de produits chimiques à partir de CO 2 . À l'avenir, nous espérons que le développement de cellules de réduction électrochimique utilisant ce catalyseur sera encouragé, conduisant à la création de dispositifs de stockage d'énergie à haute compatibilité environnementale pouvant contribuer à la fixation du CO 2 et la promotion de l'utilisation efficace des énergies renouvelables.