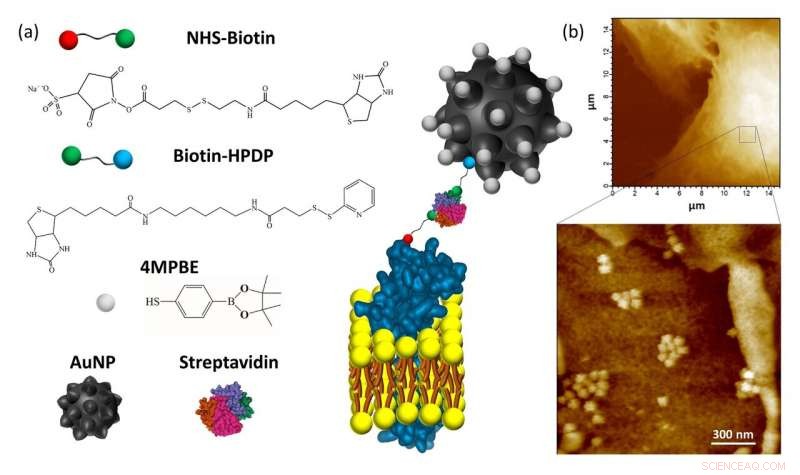
Figure 1 :(a) Schéma explicatif du nanocapteur ancré à la membrane plasmique. Les composés utilisés pour la conjugaison des nanoparticules d'or (AuNP) sont l'ester de pinacol 4-mercaptophénylboronique sensible au H2O2 (4MPBE) et la biotine-HPDP. La biotinylation des ectodomaines des protéines membranaires plasmiques est obtenue à l'aide de NHS-Biotine. L'ancrage de l'AuNP conjugué et de la NHS-Biotine est donné par la streptavidine réagissant avec les deux fragments de biotine. (b) L'analyse AFM a été réalisée sur des cellules de cancer du poumon A549 après ancrage et fixation du nanocapteur. Des images AFM haute résolution ont confirmé la présence du nanocapteur, qui est en contact avec la surface cellulaire et est capable de détecter le H2O2 endogène dans une région très peu profonde (c'est-à-dire, 90 nm) du liquide extracellulaire en contact avec la membrane plasmique. Crédit :Université de Kanazawa
Des chercheurs de l'Université de Kanazawa rapportent dans Biocapteurs et bioélectronique un test réussi d'un capteur pour mesurer les concentrations de peroxyde d'hydrogène à proximité des membranes cellulaires. Le capteur a le potentiel de devenir un outil pour de nouvelles thérapies contre le cancer.
Plusieurs processus dans le corps humain sont régulés par des réactions biochimiques impliquant le peroxyde d'hydrogène (H
Le biocapteur se compose d'une nanoparticule d'or avec des molécules organiques qui s'y rattachent. L'ensemble du cluster est conçu de manière à s'ancrer facilement à l'extérieur de la membrane d'une cellule, c'est exactement là que se trouvent les molécules de peroxyde d'hydrogène à détecter. En tant que molécules d'attachement, les scientifiques ont utilisé un composé appelé 4MPBE, connu pour avoir une forte réponse de diffusion Raman :lorsqu'il est irradié par un laser, les molécules consomment une partie de l'énergie de la lumière laser. En mesurant le changement de fréquence de la lumière laser, et tracer la force du signal en fonction de ce changement, un spectre unique est obtenu, une signature des molécules 4MPBE. Lorsqu'une molécule de 4MPBE réagit avec un H
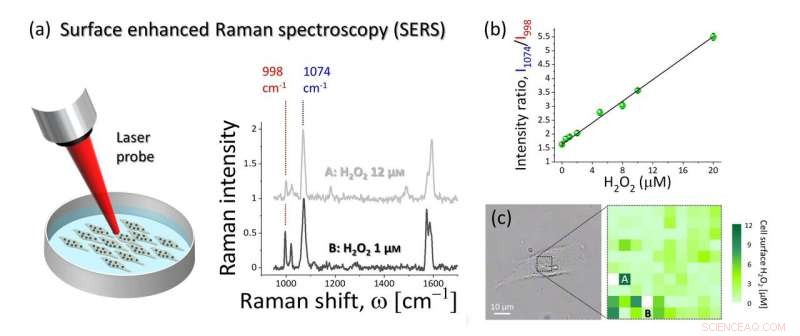
Figure 2 :(a) La spectroscopie Raman améliorée en surface a été utilisée pour détecter et quantifier la modification induite par H2O2 des molécules 4MPBE assemblées sur la surface en or du nanocapteur ancré aux cellules. L'intensité de la bande Raman à 998 cm-1 dépend de la concentration en H2O2, tandis que la bande à 1074 cm-1 n'a pas montré de modification et elle peut être utilisée pour la normalisation des raies spectrales. (b) Résultats de l'étalonnage du nanocapteur. Le rapport de l'intensité à 1074 cm-1 à l'intensité à 998 cm-1 a montré une dépendance linéaire par rapport à la concentration de H2O2. (c) Exemple de carte hyperspectrale SERS de H2O2 endogène extracellulaire collectée à la surface de la cellule A549 montrée dans image en fond clair. Les spectres SERS indiqués en (a) ont été collectés aux emplacements A et B. Crédit :Université de Kanazawa
Après avoir développé une procédure d'étalonnage pour leur nanocapteur-relatif à l'H
Puppulin et ses collègues concluent que leur "nouvelle approche peut être utile pour l'étude de la véritable H
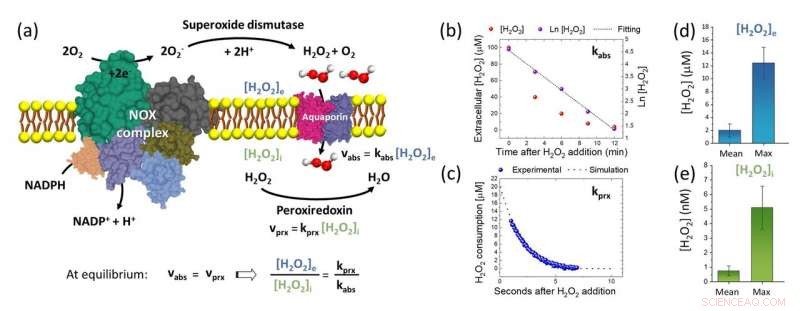
Figure 3 :(a) Schéma explicatif de la production extracellulaire de H2O2 par le complexe NOX, l'absorption conséquente par le canal Aquaporin et la réaction avec la peroxiredoxine intracellulaire. En régime permanent, le rapport de concentration de H2O2 extracellulaire à H2O2 intracellulaire peut être estimé par le rapport de la constante de vitesse de réduction de H2O2 par la peroxiredoxine (kprx) à la constante de vitesse d'absorption de H2O2 à travers la membrane plasmique (kabs). (b)-(c) Résultats typiques d'expériences de biologie redox avec des lignes d'ajustement à partir desquelles nous avons mesuré kabs et kprx, respectivement. (d) Surface extracellulaire moyenne [H2O2]e et le maximum typique de [H2O2]e mesurés sur des cellules A549 à l'aide du nanocapteur nouvellement conçu. (e) [H2O2]i intracellulaire moyen et le maximum typique de [H2O2]i estimés sur les cellules A549 selon le modèle rapporté en (a) et en utilisant les résultats de (b)-(d). Crédit :Université de Kanazawa
Le biocapteur développé par Leonardo Puppulin de l'Université de Kanazawa et ses collègues est basé sur une méthode appelée spectroscopie Raman améliorée en surface (SERS). Le principe dérive de la spectroscopie Raman, dans lequel les différences entre les fréquences entrantes et sortantes de la lumière laser irradiée sur un échantillon sont analysées. Le spectre obtenu en traçant l'intensité du signal en fonction de la différence de fréquence est caractéristique de l'échantillon, qui peut en principe être une seule molécule. Typiquement, cependant, le signal provenant d'une molécule est trop faible pour être détecté, mais l'effet peut être renforcé lorsque la molécule est absorbée sur une surface métallique rugueuse. Puppulin et ses collègues ont appliqué la technique pour détecter (indirectement) le peroxyde d'hydrogène; leur molécule sensible à Raman est un composé appelé 4MPBE, qui est modifié lorsqu'il est exposé au peroxyde d'hydrogène.