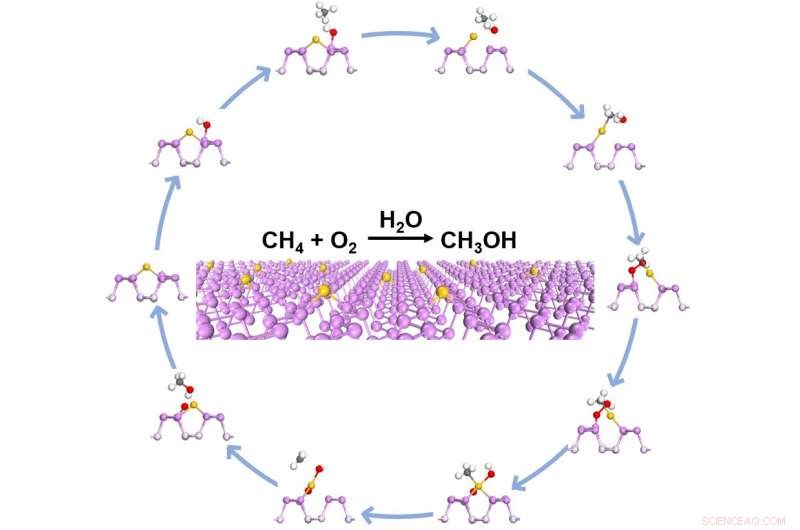
Diagramme schématique de la voie de réaction pour l'oxydation du méthane sur des nanofeuillets Au1/BP. Crédit :LUO Laihao
Les progrès de la technologie de fracturation hydraulique ont permis la découverte d'importantes réserves de gaz naturel qui contient principalement du méthane, et qui est principalement brûlé directement, potentiellement à l'origine du réchauffement climatique. La valorisation du méthane en énergie plus verte telle que le méthanol par oxydation aérobie est un moyen idéal de résoudre le problème.
Pourtant, les difficultés résident dans l'activation du méthane et la prévention de la suroxydation du méthanol. Le méthane prend une structure tétraédrique non polaire stable avec une énergie de dissociation élevée de la liaison C-H, qui nécessite une énergie élevée pour être activé. Pendant ce temps, le méthanol peut être facilement suroxydé en dioxyde de carbone pendant le processus. L'activation et la transformation directionnelle du méthane sont considérées comme le « Saint Graal » de la catalyse.
Un ouvrage récent publié dans Communication Nature par une équipe de recherche dirigée par le professeur Zeng Jie et LI Weixue du Laboratoire national des sciences physiques de Hefei à l'échelle microscopique marque de nouveaux progrès. Ils ont conçu et fabriqué des atomes simples d'Au sur du phosphore noir (Au
Au
Étant donné que l'eau est consommée pour former des groupes hydroxyle et produite par réaction de groupes hydroxyle avec du méthane, l'eau est ici complètement recyclée et peut donc également être considérée comme un catalyseur.
Cette étude donne un aperçu du mécanisme d'activation de l'oxygène et du méthane dans l'oxydation sélective du méthane, et offre une nouvelle compréhension du rôle de l'eau dans le processus de réaction.