Le Dr Ng et son équipe ont synthétisé un nouveau photocatalyseur en enveloppant de l'oxyde cuivreux avec des structures organo-métalliques à base de cuivre. Crédit :Université de la ville de Hong Kong
Dioxyde de carbone (CO
La recherche a été dirigée par le Dr Ng Yun-hau, Professeur agrégé à l'École de l'énergie et de l'environnement (SEE), en collaboration avec des chercheurs australiens, Malaisie et Royaume-Uni. Leurs découvertes ont été récemment publiées dans la revue scientifique Angewandte Chemie, intitulé "Cadres métalliques-organiques décorés de nanofils d'oxyde cuivreux pour des charges de longue durée appliquées dans le CO photocatalytique sélectif
Photocatalyse inspirée de la nature
"Inspiré par la photosynthèse dans la nature, le dioxyde de carbone peut désormais être converti efficacement en carburant méthane par notre catalyseur solaire nouvellement conçu, ce qui réduira les émissions de carbone. Par ailleurs, ce nouveau catalyseur est fabriqué à partir de matériaux à base de cuivre, qui est abondant et donc abordable, " a déclaré le Dr Ng.
Il a expliqué qu'il est thermodynamiquement difficile de convertir le dioxyde de carbone en méthane à l'aide d'un photocatalyseur, car le processus de réduction chimique implique un transfert simultané de huit électrons. Monoxyde de carbone, qui est nocif pour l'homme, est plus couramment produit dans le processus car il ne nécessite que le transfert de deux électrons.
Il a souligné que l'oxyde cuivreux (Cu
La figure a montre les images de fils de cuivre, nanofils d'oxyde cuivreux et oxyde cuivreux avec coque MOF. Chiffre b, c et d sont respectivement leurs images au microscope électronique à balayage. Crédit :DOI :10.1002/anie.202015735
Production sélective de méthane pur
Pour surmonter ces défis, Le Dr Ng et son équipe ont synthétisé un nouveau photocatalyseur en enveloppant de l'oxyde cuivreux avec des structures métallo-organiques (MOF) à base de cuivre. Grâce à ce nouveau catalyseur, l'équipe pourrait manipuler le transfert d'électrons et produire sélectivement du méthane pur.
Ils ont découvert que par rapport à l'oxyde cuivreux sans coque MOF, l'oxyde cuivreux avec coque MOF a réduit le dioxyde de carbone en méthane de manière stable sous irradiation à la lumière visible avec un rendement presque doublé. Aussi, l'oxyde cuivreux avec coque MOF était plus durable et l'absorption maximale de dioxyde de carbone était presque sept fois supérieure à celle de l'oxyde cuivreux nu.
Augmentation de l'absorption de dioxyde de carbone
L'équipe a encapsulé les nanofils d'oxyde cuivreux unidimensionnels (1-D) (d'un diamètre d'environ 400 nm) avec l'enveloppe extérieure MOF à base de cuivre d'environ 300 nm d'épaisseur. Ce revêtement conforme de MOF sur l'oxyde cuivreux ne bloquerait pas la récolte de lumière du catalyseur. Outre, MOF est un bon adsorbant de dioxyde de carbone. Il a fourni des surfaces considérables pour l'adsorption et la réduction du dioxyde de carbone. Comme il était étroitement attaché à l'oxyde cuivreux, il a apporté une concentration plus élevée de dioxyde de carbone adsorbé à des endroits proches des sites actifs catalytiques, renforcer l'interaction entre le dioxyde de carbone et le catalyseur.
De plus, l'équipe a découvert que l'oxyde cuivreux était stabilisé par le revêtement conforme de MOF. Les charges excitées dans l'oxyde cuivreux lors de l'illumination pourraient migrer efficacement vers le MOF. De cette façon, une accumulation excessive de charges excitées au sein du catalyseur pouvant conduire à une auto-corrosion a été évitée, donc prolongé la durée de vie du catalyseur.
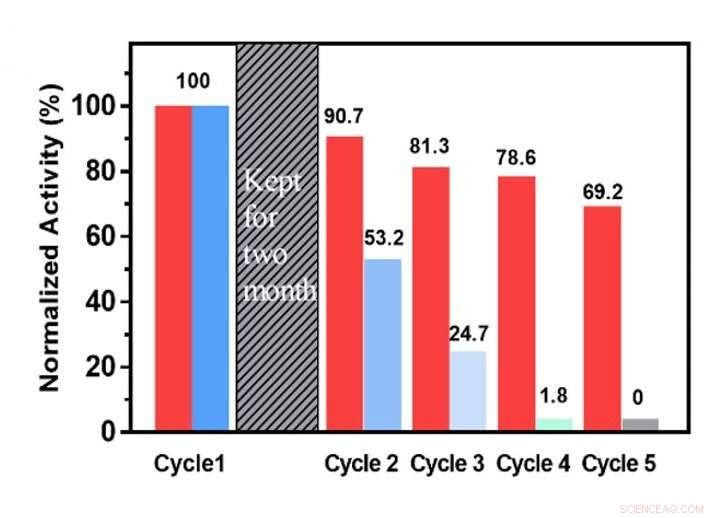
Contrairement à l'échantillon d'oxyde cuivreux nu, qui a perdu son activité intrinsèque au cinquième run, l'oxyde cuivreux avec coque MOF a conservé 69,2 % de son efficacité d'origine pour la production de méthane après cinq passages. Crédit :DOI :10.1002/anie.202015735
Les électrons sont restés dans le MOF avec plus de chances d'avoir des réactions chimiques
Dr Wu Hao, le premier auteur de l'article qui est également de SEE, a souligné l'un des points saillants de cette recherche et a déclaré :« En utilisant la spectroscopie de photoluminescence à résolution temporelle avancée, nous avons observé qu'une fois les électrons excités vers la bande de conduction de l'oxyde cuivreux, ils seraient directement transférés à l'orbitale moléculaire inoccupée la plus basse (LUMO) du MOF et y resteraient, mais ne sont pas revenus rapidement à leur bande de valence, qui est de plus faible énergie. Cela a créé un état séparé de charge de longue durée. Par conséquent, les électrons qui sont restés dans le MOF auraient plus de chances de subir des réactions chimiques. »
Étend la compréhension des relations entre les MOF et les oxydes métalliques
Précédemment, on croyait généralement que les activités photocatalytiques améliorées étaient simplement induites par l'effet de concentration de réactif du MOF et que le MOF n'a servi que d'adsorbant de réactif. Cependant, L'équipe du Dr Ng a dévoilé comment les charges excitées migrent entre l'oxyde cuivreux et le MOF dans cette recherche. "Il est prouvé que le MOF joue un rôle plus important dans la formation du mécanisme de réaction car il modifie la voie des électrons, ", a-t-il déclaré. Il a souligné que cette découverte a étendu la compréhension des relations entre les MOF et les oxydes métalliques au-delà de leurs interactions de type adsorption physique/chimique conventionnelle pour faciliter la séparation des charges.
L'équipe a passé plus de deux ans à développer cette stratégie efficace de conversion du dioxyde de carbone. Leur prochaine étape sera d'augmenter encore le taux de production de méthane et d'explorer des moyens d'augmenter à la fois la synthèse du catalyseur et les systèmes de réacteur. "Dans tout le processus de conversion du dioxyde de carbone en méthane, le seul apport d'énergie que nous avons utilisé était la lumière du soleil. Nous espérons qu'à l'avenir, le dioxyde de carbone émis par les usines et les transports peut être « recyclé » pour produire des carburants verts, " a conclu le Dr Ng.