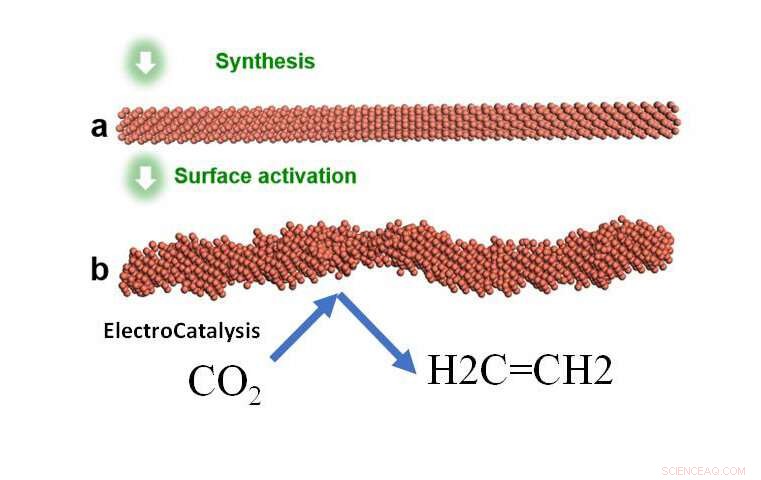
Illustration du système d'électrocatalyse qui a synthétisé le nanofil lisse puis l'a activé en appliquant une tension pour obtenir la surface rugueuse en gradins hautement sélective pour la réduction du CO2 en éthylène. Crédit :Yu Huang et William A. Goddard III
Une équipe de recherche de Caltech et de la UCLA Samueli School of Engineering a démontré un moyen prometteur de convertir efficacement le dioxyde de carbone en éthylène, un produit chimique important utilisé pour produire des plastiques, solvants, cosmétiques et autres produits importants dans le monde.
Les scientifiques ont développé des fils de cuivre à l'échelle nanométrique avec des surfaces spécialement formées pour catalyser une réaction chimique qui réduit les émissions de gaz à effet de serre tout en générant simultanément de l'éthylène, un produit chimique précieux. Des études informatiques de la réaction montrent que le catalyseur façonné favorise la production d'éthylène par rapport à l'hydrogène ou au méthane. Une étude détaillant l'avance a été publiée dans Catalyse naturelle .
"Nous sommes au bord de l'épuisement des combustibles fossiles, couplée aux défis mondiaux du changement climatique, " dit Yu Huang, le co-auteur de l'étude, et professeur de science et d'ingénierie des matériaux à l'UCLA. « Le développement de matériaux capables de transformer efficacement les gaz à effet de serre en carburants à valeur ajoutée et en matières premières chimiques est une étape cruciale pour atténuer le réchauffement climatique tout en se détournant de l'extraction de combustibles fossiles de plus en plus limités. Cette expérience intégrée et cette analyse théorique présentent une voie durable vers le recyclage du dioxyde de carbone et utilisation."
Actuellement, l'éthylène a une production annuelle mondiale de 158 millions de tonnes. Une grande partie est transformée en polyéthylène, qui est utilisé dans les emballages en plastique. L'éthylène est traité à partir d'hydrocarbures, comme le gaz naturel.
"L'idée d'utiliser du cuivre pour catalyser cette réaction existe depuis longtemps, mais la clé est d'accélérer le rythme pour qu'il soit assez rapide pour la production industrielle, " a déclaré William A. Goddard III, l'auteur co-correspondant de l'étude et le professeur de chimie Charles et Mary Ferkel de Caltech, La science des matériaux, et physique appliquée. "Cette étude montre une voie solide vers cette marque, avec le potentiel de transformer la production d'éthylène en une industrie plus verte utilisant le CO
L'utilisation de cuivre pour démarrer le dioxyde de carbone (CO
Pour surmonter ces deux obstacles, les chercheurs se sont concentrés sur la conception des nanofils de cuivre avec des « marches » hautement actives, semblables à un ensemble d'escaliers disposés à l'échelle atomique. Une découverte intrigante de cette étude collaborative est que ce modèle d'étape à travers les surfaces des nanofils est resté stable dans les conditions de réaction, contrairement à la croyance générale selon laquelle ces caractéristiques à haute énergie s'atténueraient. C'est la clé de la durabilité et de la sélectivité du système dans la production d'éthylène, au lieu d'autres produits finis.
L'équipe a démontré un taux de conversion du dioxyde de carbone en éthylène supérieur à 70 %, beaucoup plus efficace que les conceptions précédentes, qui a donné au moins 10 % de moins dans les mêmes conditions. Le nouveau système a fonctionné pendant 200 heures, avec peu de changement dans l'efficacité de conversion, une avancée majeure pour les catalyseurs à base de cuivre. En outre, la compréhension globale de la relation structure-fonction a illustré une nouvelle perspective pour concevoir du CO hautement actif et durable
Huang et Goddard sont de fréquents collaborateurs depuis de nombreuses années, avec le groupe de recherche de Goddard se concentrant sur les raisons théoriques qui sous-tendent les réactions chimiques, tandis que le groupe de Huang a créé de nouveaux matériaux et mené des expériences. L'auteur principal de l'article est Chungseok Choi, un étudiant diplômé en science et ingénierie des matériaux à l'UCLA Samueli et membre du laboratoire de Huang.