
La micrographie montre des nanoparticules uniformes de moins de 10 nm de diamètre. Crédit :Tony Z. Jia, ELSI
La plupart des efforts dans la recherche sur les origines de la vie se concentrent sur la compréhension de la formation prébiotique des blocs de construction biologiques. Cependant, il est possible que l'évolution biologique précoce repose sur différentes structures et processus chimiques, et ceux-ci ont été remplacés progressivement au fil du temps par des éons d'évolution. Récemment, les chimistes Irena Mamajanov, Melina Caudan et Tony Jia du Earth-Life Science Institute (ELSI) au Japon ont emprunté des idées à la science des polymères, l'administration de médicaments, et le biomimétisme pour explorer cette possibilité. Étonnamment, ils ont découvert que même de petits polymères hautement ramifiés pouvaient servir de catalyseurs efficaces, et ceux-ci ont peut-être aidé la vie à démarrer.
En biologie moderne, les enzymes protéiques codées font la plupart du travail catalytique dans les cellules. Ces enzymes sont constituées de polymères linéaires d'acides aminés, qui se replient et se replient sur elles-mêmes pour former des formes tridimensionnelles fixes. Ces formes préformées leur permettent d'interagir très spécifiquement avec les produits chimiques dont elles catalysent les réactions. Les catalyseurs aident les réactions à se produire beaucoup plus rapidement qu'elles ne le feraient autrement, mais ne soyez pas consumé par la réaction eux-mêmes, ainsi une seule molécule de catalyseur peut aider la même réaction à se produire plusieurs fois. Dans ces états pliés en trois dimensions, la plupart de la structure du catalyseur n'interagit pas directement avec les produits chimiques sur lesquels il agit, et aide simplement la structure enzymatique à garder sa forme.
Dans le travail present, Les chercheurs de l'ELSI ont étudié des polymères hyperramifiés - des structures arborescentes avec un degré et une densité de ramification élevés qui sont intrinsèquement globulaires sans avoir besoin d'un repliement informé - ce qui est requis pour les enzymes modernes. Polymères hyperbranchés, comme les enzymes, sont capables de positionner des catalyseurs et des réactifs, et moduler la chimie locale de manière précise.
La plupart des efforts dans la recherche sur les origines de la vie se concentrent sur la compréhension de la formation prébiotique des structures biologiques modernes et des blocs de construction. La logique est que ces composés existent maintenant, et ainsi comprendre comment ils pourraient être fabriqués dans l'environnement pourrait aider à expliquer comment ils sont apparus. Cependant, nous ne connaissons qu'un seul exemple de vie, et nous savons que la vie évolue constamment, ce qui signifie que seules les variantes les plus réussies des organismes survivent. Ainsi, il peut être raisonnable de supposer moderne les organismes peuvent ne pas être très similaires aux premier organismes, et il est possible que la chimie prébiotique et l'évolution biologique précoce se soient appuyées sur des structures et des processus chimiques différents de ceux de la biologie moderne pour se reproduire. Par analogie avec l'évolution technologique, les premiers téléviseurs à rayons cathodiques remplissaient plus ou moins la même fonction que les écrans haute définition modernes, mais ce sont des technologies fondamentalement différentes. Une technologie a conduit à la création de l'autre à certains égards, mais ce n'était pas nécessairement le précurseur logique et direct de l'autre.
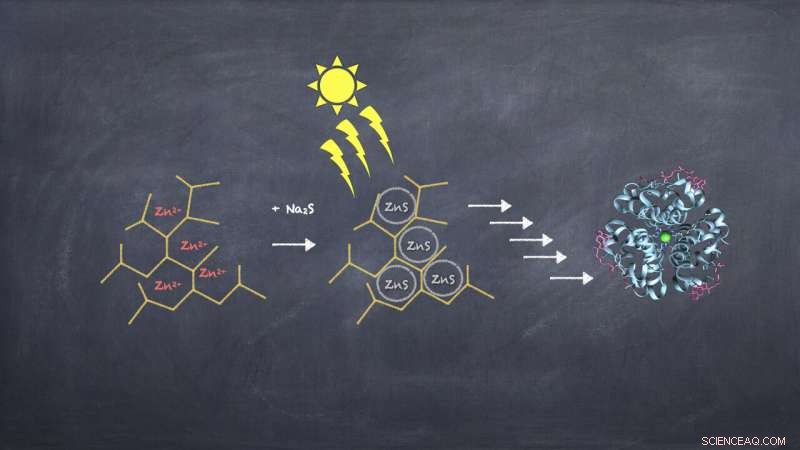
Les enzymes sulfures métalliques pourraient provenir de particules globulaires de sulfure métallique/polymère hyperramifié. Crédit :Irena Mamajanov, ELSI
Si ce type de modèle "d'échafaudage" pour l'évolution biochimique est vrai, la question devient quelle sorte de structures plus simples, outre ceux utilisés dans les systèmes biologiques contemporains, aurait-il pu aider à réaliser les mêmes types de fonctions catalytiques que la vie moderne ? Mamajanov et son équipe ont estimé que les polymères hyperramifiés pourraient être de bons candidats.
L'équipe a synthétisé certains des polymères hyperramifiés qu'ils ont étudiés à partir de produits chimiques dont on pouvait raisonnablement s'attendre à ce qu'ils soient présents sur la Terre primitive avant le début de la vie. L'équipe a ensuite montré que ces polymères pouvaient se lier à de petits amas inorganiques d'atomes naturels connus sous le nom de nanoparticules de sulfure de zinc. De telles nanoparticules sont connues pour être exceptionnellement catalytiques en elles-mêmes.
Comme le commente le scientifique principal Mamajanov, «Nous avons essayé deux types différents d'échafaudages polymères hyperramifiés dans cette étude. Pour les faire fonctionner, il suffisait de mélanger une solution de chlorure de zinc et une solution de polymère, puis ajouter du sulfure de sodium, et "voila, « nous avons obtenu un catalyseur à base de nanoparticules stable et efficace. »
Le prochain défi de l'équipe était de démontrer que ces hybrides polymère-nanoparticules hyperramifiés pouvaient réellement faire quelque chose d'intéressant et de catalytique. Ils ont découvert que ces polymères dopés au sulfure métallique qui dégradent les petites molécules étaient particulièrement actifs en présence de lumière, dans certains cas, ils ont catalysé la réaction jusqu'à un facteur 20. Comme le dit Mamajanov, «Jusqu'à présent, nous n'avons exploré que deux échafaudages possibles et un seul dopant. Il y en a sans doute beaucoup, de nombreux autres exemples restent à découvrir.
Les chercheurs ont en outre noté que cette chimie pourrait être pertinente pour un modèle des origines de la vie connu sous le nom de « monde du zinc ». Selon ce modèle, le premier métabolisme a été conduit par des réactions photochimiques catalysées par des minéraux de sulfure de zinc. Ils pensent qu'avec quelques modifications, ces échafaudages hyperramifiés pourraient être ajustés pour étudier des analogues d'enzymes protéiques contenant du fer ou du molybdène, y compris les plus importants impliqués dans la fixation biologique moderne de l'azote. Mamajanov dit, 'L'autre question que cela soulève est, en supposant que la vie ou la pré-vie a utilisé ce type de processus d'échafaudage, pourquoi la vie s'est-elle finalement installée sur des enzymes ? Y a-t-il un avantage à utiliser des polymères linéaires par rapport à des polymères ramifiés ? Comment, quand et pourquoi cette transition s'est-elle produite ?'