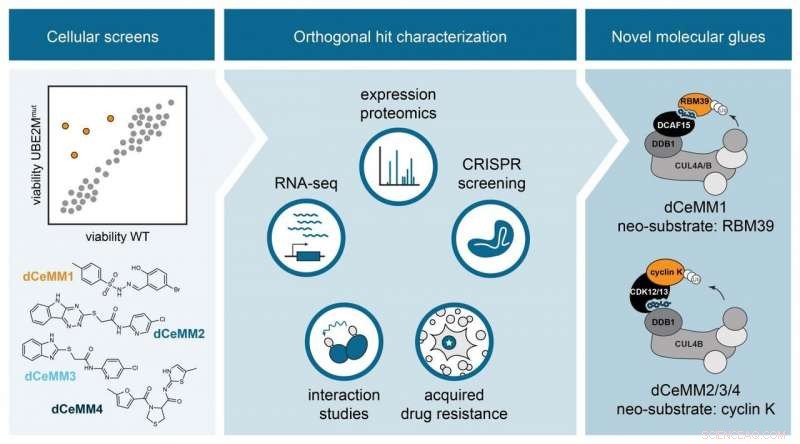
Les cribles de viabilité cellulaire ont désigné des colles moléculaires potentielles. L'étude orthogonale des principales molécules (dCeMM1/2/3/4) a permis de caractériser de nouveaux dégradeurs de colle moléculaire qui recrutent deux ligases E3 différentes pour induire la dégradation des protéines RBM39 et de la cycline K. Crédit :Cristina Mayor-Ruiz/CeMM
Malgré d'énormes efforts pour faire progresser les approches pharmacologiques traditionnelles, plus des trois quarts de toutes les protéines humaines restent hors de portée du développement thérapeutique. La dégradation ciblée des protéines (TPD) est une nouvelle approche qui pourrait surmonter cette limitation et d'autres, et représente ainsi une stratégie thérapeutique prometteuse. La TPD est basée sur de petites molécules, généralement appelés 'dégradants, ' qui peut éliminer les protéines pathogènes en provoquant leur déstabilisation. Mécaniquement, ces médicaments dégradants réutilisent le système de contrôle de qualité des protéines cellulaires, le peaufiner pour reconnaître et éliminer les protéines nocives. En détail, ils redirigent les membres de la famille des protéines des ubiquitine ligases E3 (E3) vers la protéine cible causant la maladie. Cela conduit à une « affectation moléculaire » de la protéine nocive via un processus appelé « ubiquitination ». Ensuite, la protéine ubiquitinée est reconnue et dégradée par la machine moléculaire appelée protéasome, qui sert de système cellulaire d'élimination des déchets.
Dans cette étude, Les chercheurs du CeMM se sont concentrés sur un sous-ensemble de dégradants appelés « dégradeurs de colle moléculaire ». Cette classe de petites molécules apparemment rares dont il a été démontré qu'elle induisait la dégradation de protéines cibles qui ne pouvaient pas être bloquées par les voies de la pharmacologie traditionnelle. Par conséquent, ces protéines avaient été qualifiées de « non médicamenteuses ». Les exemples les mieux caractérisés sont les analogues de la thalidomide cliniquement approuvés, efficace pour le traitement de différents cancers du sang. Malheureusement, la découverte des quelques dégradeurs de colle moléculaire décrits a toujours été un processus entièrement motivé par un heureux hasard, et aucune stratégie de découverte rationnelle n'existait.
Pour surmonter cette limite, Le groupe de Georg Winter au CeMM a entrepris d'innover une stratégie évolutive vers la découverte de nouveaux dégradeurs de colle moléculaire via un criblage chimique phénotypique. À cette fin, Cristina Mayor-Ruiz, premier auteur et boursière postdoctorale du CeMM, et ses collègues ont conçu des systèmes cellulaires largement altérés dans l'activité E3. La viabilité différentielle entre ces modèles et les cellules compétentes en E3 a été utilisée pour identifier les composés qui dépendent des E3 actifs, et donc, dégradants potentiels de la colle moléculaire. Les chercheurs ont intégré la génomique fonctionnelle à la protéomique et aux stratégies d'interaction médicamenteuse, caractériser les composés les plus prometteurs. Ils ont validé l'approche en découvrant un nouveau dégradeur de colle moléculaire RBM39, structurellement similaire à d'autres précédemment décrits. Surtout, ils ont découvert un ensemble de nouvelles colles moléculaires qui induisent la dégradation de la protéine cycline K, connu pour être essentiel dans de nombreux types de cancer. De façon intéressante, ces nouveaux dégradeurs de la cycline K fonctionnent via un mécanisme d'action moléculaire sans précédent qui implique le E3 CUL4B:DDB1 et qui n'a jamais été exploré thérapeutiquement auparavant.
Cette étude, réalisée en étroite collaboration avec CeMM PI Stefan Kubicek, fournit ainsi le premier cadre vers la découverte de dégradeurs de colle moléculaires qui peuvent être à grande échelle, mais aussi fortement diversifiée. "Je crois vraiment que nous ne faisons qu'effleurer la surface des possibilités. Cette étude est le premier chapitre des nombreux chapitres à suivre. Nous verrons une révolution dans la façon dont les chercheurs perçoivent et exécutent des stratégies thérapeutiques pour des maladies auparavant incurables en élaborant des stratégies de dégradation de la colle qui leur permettre d'éliminer des cibles thérapeutiques qui ne pourraient pas être explorées avec les approches pharmacologiques traditionnelles », dit CeMM PI et dernier auteur de l'étude Georg Winter.