Crédit :Daria Sokol/MIPT
Des chercheurs de l'Institut de physique générale Prokhorov de l'Académie des sciences de Russie et de l'Institut de physique et de technologie de Moscou ont mis au point une nouvelle méthode pour diagnostiquer et surveiller les maladies auto-immunes. En à peine 25 minutes, leur nouveau biocapteur mesure non seulement la concentration d'auto-anticorps dans le sérum sanguin humain avec une sensibilité extrêmement élevée, mais aussi — pour la première fois — quantifie leur activité. La combinaison de ces paramètres permet d'élaborer de nouveaux critères diagnostiques des maladies auto-immunes, ainsi que de nouvelles approches de leur traitement. Le document a été publié en Biocapteurs et bioélectronique , la revue scientifique la mieux classée dans le domaine de la technologie de biodétection et de la chimie analytique.
Les autoanticorps produits par le système immunitaire interprètent à tort les cellules et les organes de l'organisme comme cibles, provoquant des troubles auto-immuns. Les auto-anticorps sont associés à plus de 80 maladies auto-immunes graves allant de la polyarthrite rhumatoïde, psoriasis, et le lupus à la sclérose en plaques et au diabète de type 1. Beaucoup d'entre eux ont besoin de soins et de traitements à vie pour soulager leurs souffrances.
Les auto-anticorps sont présents dans le sang d'environ 10 % de la population. En raison d'une forte prévalence de maladies auto-immunes, l'impact économique est énorme et est estimé pour certains pays comme le double de celui du cancer. Les auto-anticorps apparaissent dans le sang bien avant l'apparition clinique, et leurs caractéristiques peuvent être utilisées pour prévoir l'activité et la gravité de la maladie.
Actuellement, le traitement des maladies auto-immunes est considérablement compliqué en raison des variations dramatiques dans les résultats des tests commerciaux par différents fabricants.
"Selon le laboratoire effectuant le test, et la méthode utilisée, la concentration d'auto-anticorps mesurée dans le même échantillon au même moment peut varier d'un facteur 10, " dit l'un des auteurs de l'article Alexey Orlov, un scientifique senior du Biophotonics Lab du GPI RAS et du Nanobiotechnology Lab du MIPT, un diplômé 2010 du MIPT. "En réalité, personne ne pouvait se fier à la concentration d'auto-anticorps comme paramètre quantitatif pour évaluer l'efficacité de la thérapie."
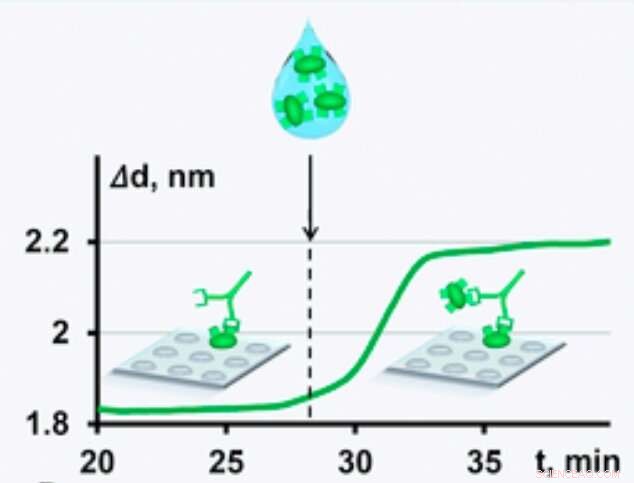
Un auto-anticorps a plusieurs « mains » – des fragments qui reconnaissent des cibles. Dans l'épreuve, l'anticorps saisit d'une main la cible immobilisée sur la surface du verre et de l'autre les cibles qui passent. Le processus reflète ce qui se passe dans l'environnement naturel et fournit des informations quantitatives sur l'activité réelle des anticorps dans l'organisme vivant. Crédit :Alexey Orlov et al./Biocapteurs et bioélectronique
De telles incohérences dans les résultats des tests proviennent de la nature complexe des auto-anticorps. Un auto-anticorps comprend un ensemble de nombreuses molécules hétérogènes qui interagissent les unes avec les autres et avec une cible de manières sensiblement différentes. Jusqu'à maintenant, aucune technique n'a permis de rendre compte de ce facteur.
Aussi, les méthodes existantes, largement utilisé dans la pratique clinique, n'offrent pas la possibilité de caractériser l'activité des anticorps - le paramètre qui montre à quel point les anticorps sont destructeurs pour les tissus cibles. Les auteurs ont développé un outil qui traite les deux problèmes à la fois :il effectue des mesures rapides à haute sensibilité de l'activité et de la concentration des auto-anticorps.
Une autre caractéristique innovante est la détermination simultanée dans un seul échantillon de la concentration et de l'activité d'auto-anticorps contre plusieurs cibles. Une telle approche augmente considérablement le mérite diagnostique de la solution car différents niveaux d'auto-anticorps dirigés contre des cibles différentes peuvent indiquer des maladies distinctes. Une analyse de corrélation des données obtenues simultanément sur plusieurs auto-anticorps peut considérablement améliorer la précision des diagnostics.
"C'est pourquoi nous appelons notre système multiplex, ou multiparamétrique, " mentionne le co-auteur de l'étude Averyan Pushkarev, un doctorant MIPT et un ancien élève 2018. « Un avantage fort réside dans les consommables utilisés dans notre technique :nous utilisons un verre de protection de microscope standard. Son faible coût est particulièrement important pour les diagnostics médicaux de masse, qui nécessite des consommables jetables."
Alors que l'étude démontre la caractérisation simultanée d'anticorps dirigés contre deux cibles, l'équipe travaille à augmenter ce nombre. Grâce à la technologie des puces électroniques, par exemple, des milliers de cibles de 100 microns peuvent être déposées sur une plaque de verre.
Dans la nouvelle technique, une goutte de sérum sanguin du patient est passée sur la surface de la lamelle de verre. Si des anticorps sont présents dans le sérum, ils trouvent leurs cibles déposées sur le verre et s'y attachent, augmenter l'épaisseur de la biocouche sur le verre. Sous la barquette de verre, il existe un système d'interférométrie développé au GPI RAS. Ce lecteur optique unique permet des mesures en temps réel de l'épaisseur de la couche moléculaire dans chaque point sur la surface du verre.
"Un détail fondamental :contrairement à une multitude d'autres méthodes, nous avons les autoanticorps qui interagissent avec des cibles en mouvement plutôt qu'avec celles immobilisées sur une surface, " Orlov ajoute. " Il s'agit de la toute première solution qui permet d'étudier l'interaction des auto-anticorps avec des cibles dans leur forme et leur environnement naturels, tels qu'ils sont présents dans un organisme vivant.
Ceci est réalisé comme suit :une fois qu'un auto-anticorps se lie à une cible sur le verre, les chercheurs pompent une solution de molécules cibles libres le long du verre. À ce moment, les auteurs mettent en œuvre une approche que personne n'a été en mesure de mettre en pratique pour la tâche importante mentionnée. Chaque autoanticorps possède un ou plusieurs fragments de reconnaissance, appelés fragments Fab ou « mains », ' qui peut reconnaître et saisir des cibles. Dans l'épreuve, un auto-anticorps saisit la cible immobilisée avec une « main » et utilise les autres pour attraper les cibles mobiles de l'échantillon de sérum. Ce processus fournit des données quantitatives sur l'activité réelle (native) des anticorps. De plus, cette configuration, d'un côté, assure l'immobilisation des auto-anticorps sur le verre sous leur forme naturelle ; et d'autre part, minimise la liaison des composants étrangers qui peuvent affecter les résultats.
"Nous avons développé non seulement un test de diagnostic efficace mais aussi un outil unique pour l'investigation des auto-anticorps, " commente l'auteur principal de l'article, Petr Nikitin, qui dirige le laboratoire de biophotonique du GPI RAS et est diplômé en 1979 du MIPT. « En utilisant des échantillons de sang de patients, nous avons démontré que le paramètre quantitatif de l'activité des autoanticorps est indépendant de leur concentration. Les cliniciens disposent désormais d'un outil de suivi quantitatif des deux paramètres clés au cours d'une maladie, et l'élaboration de nouvelles méthodes avancées pour le diagnostic et le traitement des maladies auto-immunes. »