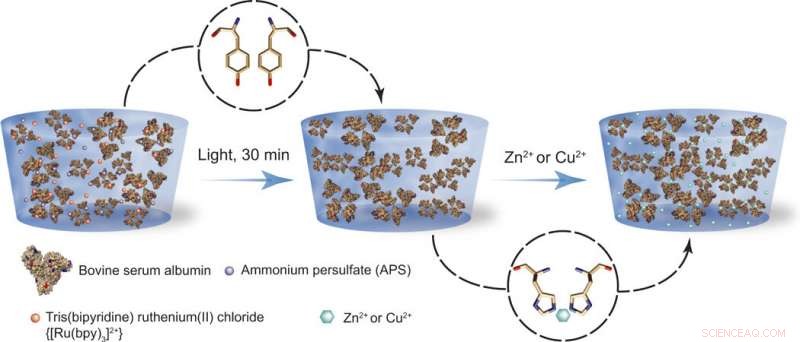
Schémas du processus de fixation. (À gauche) Les hydrogels de protéines à base de BSA sont fabriqués à l'aide d'une réaction activée par la lumière, en présence de persulfate d'ammonium (APS) et de chlorure de tris(bipyridine)ruthénium(II) [Ru(bpy)3]2+. (À droite) Après la synthèse, les hydrogels protéiques sont exposés à Zn2+ ou Cu2+, ce qui augmente de manière réversible leur rigidité jusqu'à 17 fois. Cet effet de raidissement peut être utilisé pour la programmation de formes. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aba6112
Les matériaux intelligents ou les matériaux avancés capables de mémoriser une forme temporaire et de se transformer en réponse à un stimulus peuvent révolutionner la médecine et la robotique. Dans une nouvelle étude maintenant sur Avancées scientifiques , Luai R. Khoury et une équipe de recherche du département de physique de l'Université du Wisconsin-Miluwaukee aux États-Unis ont introduit une approche innovante pour programmer des hydrogels de protéines et induire des changements de forme à température ambiante dans des solutions aqueuses. L'équipe a démontré son approche en utilisant des hydrogels à base d'albumine sérique, la protéine la plus abondante dans le plasma sanguin. Les scientifiques ont synthétisé la protéine sous la forme d'un cylindre ou d'une fleur et ont programmé les gels sous la forme d'un ressort ou d'un anneau. Ils ont effectué la programmation en modifiant la rigidité du matériau en induisant l'adsorption du Zinc (Zn 2+ ) ou Cuivre (Cu 2+ ) cations. Les biomatériaux programmés pourraient reprendre leur forme d'origine à mesure que les cations se diffusaient à l'extérieur du matériau hydrogel. La méthode est une stratégie innovante pour programmer des hydrogels à base de protéines pour potentiellement agir comme des actionneurs robotiques.
Les biomatériaux dynamiques avec des changements de conformation peuvent faciliter les structures de tissus artificiels pour la transformation morphologique et la robotique douce afin de réagir et de changer en réponse à leur environnement. Les matériaux de morphing de forme les plus courants sont basés sur des polymères qui nécessitent une commutation entre une phase rigide et molle. De tels matériaux reposent généralement sur deux squelettes de réseau ou plus qui partagent le même espace tridimensionnel (3D) ou maintiennent une réponse chimique aux petits ions. La programmation est définie comme la capacité de fixer une forme temporaire dans un matériau et le processus nécessite une augmentation réversible de la rigidité. La reprise de forme initiale peut passer d'une phase rigide à une phase molle, généralement réalisé en changeant la température, pH ou photo-commutation pour compromettre l'intégrité du réseau secondaire.
Khoury et al. a déjà introduit une méthode pour former une mémoire de forme dans des hydrogels à base de protéines, où les protéines formaient le réseau primaire dans un environnement riche en eau, en rigidifiant les hydrogels avec des polyélectrolytes adsorbés. Dans cette approche, l'équipe a produit des hydrogels protéiques à partir d'albumine de sérum bovin, qui est homologue à l'albumine sérique humaine, la protéine plasmatique la plus abondante. Ils ont programmé l'hydrogel par rigidification induite via un réseau secondaire constitué de polyélectrolytes chargés positivement, et a stimulé un changement de forme en initiant la réponse de dépliement des domaines protéiques dans les dénaturants chimiques.
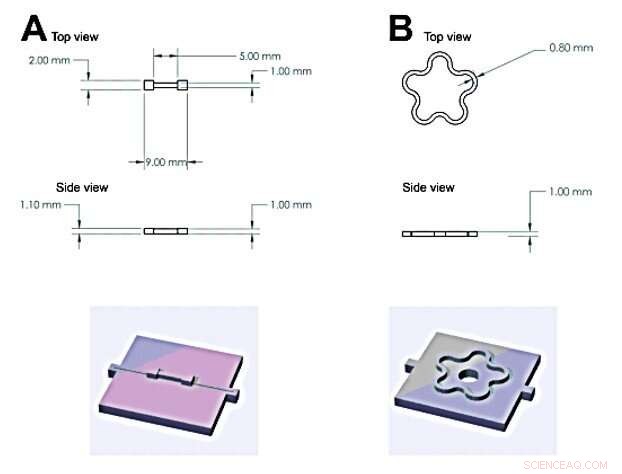
Schémas montrant les deux formes différentes utilisées dans cette étude pour synthétiser des hydrogels :(A) forme en forme d'os (B) forme en forme de fleur. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aba6112
La stratégie a permis une récupération complète lors de l'élimination du dénaturant et cette transition était hautement reproductible, mais l'adsorption des polyélectrolytes était irréversible et a entraîné un changement de rigidité. Dans ce travail, les scientifiques ont utilisé des cations divalents pour rigidifier les hydrogels à base de protéines et les ont programmés dans une variété de formes qui ont réussi à retrouver leur forme d'origine par simple diffusion. L'équipe de recherche a exploré le changement mécanique pour induire une rigidité accrue et programmer des biomatériaux à base de protéines dans une variété de formes. Les hydrogels à base de protéines nouvellement programmés avec de petits ions ont constitué une étape importante pour concevoir des biomatériaux biocompatibles avec des structures ajustables.
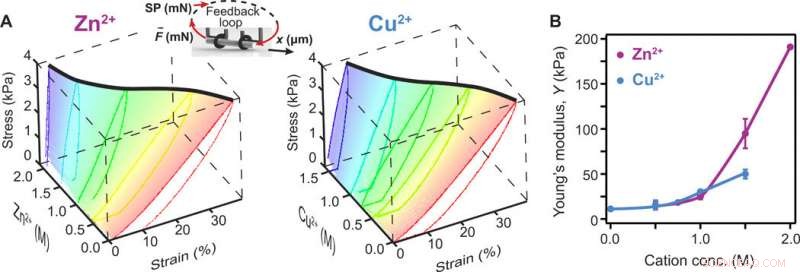
Raidissement à base de cations d'hydrogels à base de protéines. (A) Modifications chimio-mécaniques induites par l'adsorption de diverses concentrations de Zn2+ (à gauche) et Cu2+ (à droite) par des hydrogels de protéines fabriqués à partir de 2 mM de BSA. Le maillage met en évidence la partie sollicitant l'effort, utilisé pour évaluer le changement de rigidité, et l'épais, la courbe noire suit la déformation finale à une contrainte de 4 kPa. En médaillon :schémas d'un tube d'hydrogel tiré sous une force contrôlée par rétroaction, où le point de consigne (SP) a été augmenté et diminué linéairement avec 40 Pa/s. (B) Modification du module de Young mesuré en fonction des concentrations de cations. Le Zn2+ et le Cu2+ induisent tous deux un raidissement lors de l'adsorption sur des hydrogels à base de BSA. Les lignes entre les points sont des guides oculaires. Les barres d'erreur sont SD (n =3). Crédit :Avancées scientifiques, doi:10.1126/sciadv.aba6112
Une série de réactions peut produire des hydrogels à base de protéines, y compris des stratégies de réticulation basées sur des traitements avec du glutaraldéhyde, réactions enzymatiques, ou photoactivation. Khouri et al. utilisé la photoactivation pour former les hydrogels à base de protéines en BSA, la réaction a produit des liaisons covalentes carbone-carbone. Ils ont testé une gamme de concentrations d'ions chargés positivement pour augmenter la rigidité des hydrogels protéiques pour la programmation de forme, et mesuré le changement de rigidité à l'aide d'un appareil rhéométrique force-clamp. L'équipe a choisi 2 mM comme concentration de départ pour produire une réticulation complète pour la BSA et les hydrogels résultants ont montré un comportement réversible sans déformation plastique. Les hydrogels BSA ont montré une rigidité accrue jusqu'à 5 fois lorsqu'ils sont traités avec Cu 2+ et une rigidité de 17 fois en présence de Zn 2+ ; plusieurs ordres de grandeur supérieurs à ceux rapportés pour les gels traités aux polyélectrolytes, permettant des formes programmées plus complexes. L'effet de raidissement dépendait de la concentration de la solution, où Zn 2+ était plus soluble dans l'eau et donc plus avantageux que Cu 2+ . Les hydrogels à base de BSA avaient une ténacité et une contrainte de rupture accrues en raison de l'augmentation des concentrations de cations. La ténacité représentait la capacité du matériau à adsorber l'énergie et à se déformer sans fracture. Cependant, la rupture irréversible des liaisons covalentes était un facteur limitant pour les extensions et donc l'hydrogel nécessitait un raffinement supplémentaire.
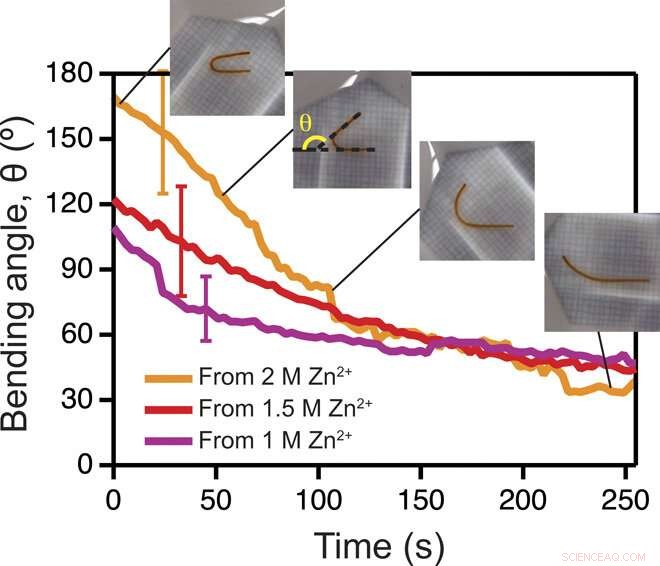
Modifications de la forme de l'hydrogel dues à la diffusion de cations à l'extérieur de l'hydrogel. Angle programmé mesuré d'un gel en forme de U, , en fonction du temps, lors de l'immersion de Zn2+ dans un tampon Tris ordinaire. Encart :images de l'hydrogel récupérant d'une forme en U à quatre moments différents. Le deuxième encart à partir de la gauche montre comment l'angle est mesuré. Les barres d'erreur représentent SD (n =3). (Crédit photo :Luai R. Khoury, UWM ; Marina Slawinski, UWM). Crédit :Avancées scientifiques, doi:10.1126/sciadv.aba6112
Puisque la dynamique de morphing de la forme programmée à la forme initiale dépendait directement de la diffusion des cations à l'extérieur du biomatériau, Khoury et al. suivi le phénomène à l'aide d'un hydrogel cylindrique en forme de U. La forme de l'hydrogel dépend de la quantité de raidissement induite par le dosage avec des cations. Les scientifiques ont obtenu une forme temporaire en combinant une réticulation ionique et des cations divalents stables dans le matériau. Ils ont ensuite programmé des biomatériaux moulés de manière cylindrique en forme de ressort et des matériaux moulés en fleurs en forme d'anneau. Les cations dans le milieu ont induit un raidissement suffisamment fort suivi d'un morphing d'un anneau à une forme de fleur.

Film montrant le morphing d'un hydrogel BSA coulé en anneau et programmé en fleur dans 2 M Zn2+ pendant 30 min et immergé dans du tampon PBS. Comme le Zn2+ diffuse à l'extérieur de l'hydrogel, la forme de la fleur se transforme en la forme initiale de l'anneau. Crédit :Avancées scientifiques, doi:10.1126/sciadv.aba6112
Les hydrogels à base de polymère ont à eux seuls une variété d'applications dans les applications de mémoire de forme et de morphing de forme, bien qu'elles ne soient pas aussi structurellement diverses que les protéines naturelles. Dans cette nouvelle approche, Luai R. Khoury et ses collègues ont développé des hydrogels à base de protéines pour faciliter le meilleur des deux mondes. L'approche reposait sur Zn 2+ et Cu 2+ cations pour induire un raidissement afin de programmer une forme permanente dans une nouvelle configuration temporaire. Ils ont également rendu les protocoles de l'étude largement accessibles via Bio-protocole. La diffusion des ions à l'extérieur du matériau a permis à l'équipe de retrouver la structure d'origine. Ils visent à utiliser Zn 2+ principalement dans les travaux futurs en raison d'une biocompatibilité plus élevée par rapport à Cu 2+ . L'approche a préservé la fonctionnalité des protéines en formant le squelette de l'hydrogel et a remarquablement combiné la biodiversité avec une capacité de programmation réversible.
© 2020 Réseau Science X