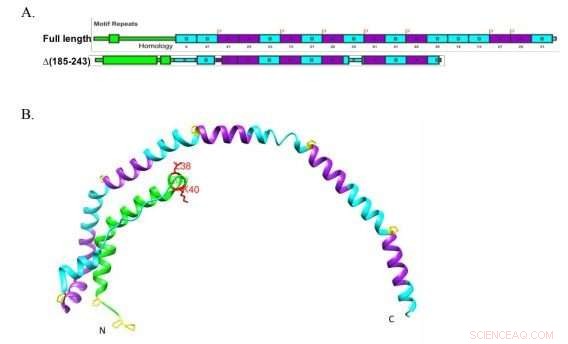
Des chercheurs de l'Université de Boston ont utilisé une version tronquée de l'apolipoprotéine A-I, montré ici, déterminer de manière concluante que la protéine doit se lier au transporteur de lipides ABCA1 pour commencer à former des lipoprotéines de haute densité, les particules de « bon cholestérol » qui transportent le cholestérol vers le foie pour élimination. Crédit :Liu et al. JLR 2018
L'huile et l'eau ne font pas bon ménage. Mais notre sang aqueux est plein de différents types de lipides hydrophobes, dont le cholestérol. Pour voyager par la circulation sanguine, ces lipides doivent faire du stop sur un porteur amphipathique. Dans un article récent du Journal de recherche sur les lipides , des scientifiques de l'Université de Boston rapportent une avancée dans notre compréhension mécaniste de la formation d'un tel porteur.
"Les lipoprotéines sont comme des bateaux qui livrent et enlèvent des cargaisons de corps gras vers et depuis nos cellules, " a déclaré David Atkinson, président du département de physiologie et de biophysique de la faculté de médecine de l'Université de Boston et auteur principal sur le JLR papier.
Le sous-ensemble de ces « bateaux » qui transportent le cholestérol et d'autres lipides vers le foie à partir d'autres parties du corps sont appelés lipoprotéines de haute densité (HDL, alias "bon cholestérol"). Le HDL peut éliminer le cholestérol des cellules distales, telles que les macrophages dans les parois des artères, où l'accumulation de cholestérol peut entraîner des crises cardiaques et le transmettre aux cellules du foie, un processus connu sous le nom de transport inverse du cholestérol. Le foie élimine l'excès de cholestérol en le convertissant en acides biliaires sécrétés dans l'intestin grêle.
Selon Atkinson, un biophysicien, la plupart de ce que l'on sait sur la formation de HDL provient d'expériences qui prennent une dimension biologique cellulaire. Dans ces types d'études, il a dit, "Vous pouvez voir (la formation HDL) se produire, et vous pouvez quantifier ce qui se passe, mais vous ne comprenez pas les interactions motrices qui le provoquent. C'est là que se concentrent mes recherches."
Les particules HDL sont construites sur une protéine d'échafaudage appelée apolipoprotéine A-I (apoA-I). On pense que l'ApoA-I collecte le cholestérol et les phospholipides de la membrane cellulaire. Atkinson et son équipe voulaient mieux comprendre le fonctionnement de ce processus.
ApoA-I dépend d'une protéine transporteur de lipides, appelé ABCA1, qui pompe le cholestérol de l'intérieur vers le feuillet extérieur de la membrane cellulaire. Parce que le cholestérol que l'ABCA1 transfère finit généralement par se lier à l'apoA-I, certains chercheurs soupçonnaient qu'il y avait une interaction physique entre l'apoA-I et l'ABCA1. Pendant ce temps, d'autres ont soutenu que le cholestérol et les phospholipides pouvaient tout aussi bien diffuser passivement et se lier à l'apoA-I. Et les expériences disponibles, dont la plupart étaient basés sur la réticulation, n'a pas tranché le débat.
"Même si vous démontrez que l'apoA-I se lie à la surface cellulaire, vous ne savez pas réellement qu'il est lié à ABCA1. C'est juste lié à la surface de la cellule, " Atkinson a expliqué. Il a donc demandé à son équipe de voir s'ils pouvaient "démontrer que l'interaction se produit réellement dans les composants isolés".
L'équipe, dirigé par l'étudiant diplômé Minjing Liu, et soutenu par le Dr Xiaohu Mei et le Dr Haya Herscovitz, utilisé isolé apoA-I et ABCA1 pour tester une interaction physique. Ils ont pu montrer une immunoprécipitation de l'apoA-I avec ABCA1 purifié.
Le laboratoire avait précédemment conçu un mutantapoA-I avec un petit mouvement supplémentaire dans une région charnière déjà flexible. Pour cette étude, ils ont utilisé le mutant pour montrer qu'une plus grande flexibilité augmentait la lipidation de l'apoA-I, ou la formation de HDL naissant. L'équipe n'a pas encore testé si le mutant extra-flexible se lie mieux à ABCA1 ou si la liaison de l'une ou l'autre forme d'apoA-I active ABCA1.
Mais à propos d'une chose, Atkinson est certain. "C'est l'interaction ApoA-I/ABCA1 qui permet ensuite à la formation de particules HDL naissantes de se produire lorsque les composants de la membrane sont transportés par ABCA1, " a déclaré Atkinson.
L'augmentation du transport inverse du cholestérol pourrait un jour être un moyen de réduire l'athérosclérose et les maladies cardiaques. Atkinson est optimiste quant à la promesse de mieux comprendre les processus physiologiques. « La recherche translationnelle est peut-être à la mode, mais n'oubliez pas que si vous ne faites pas de recherche fondamentale et fondamentale, tu n'auras rien à traduire, " il a dit.