
En utilisant la chimie computationnelle, étudiant diplômé Vindi M. Jayasinghe-Arachchige et Rajeev Prabhakar, professeur de chimie, conçu une nouvelle molécule qui pourrait faire avancer considérablement l'étude et les utilisations des enzymes. Crédit :Jenny Hudak/Université de Miami
Les enzymes sont les moteurs de la nature. Présent dans les cellules de tous les animaux, les plantes, et tout autre organisme vivant, ils accélèrent les réactions chimiques qui déclenchent des milliers de fonctions biologiques, de la formation de neurones à la digestion des aliments.
Ils effectuent leur travail de manière si sélective et si rapide - des millions de fois plus vite qu'un clin d'œil - que le domaine de la chimie biomimétique a émergé au cours des dernières décennies dans le but de concevoir des enzymes artificielles capables d'imiter les pouvoirs des enzymes naturelles dans milieux industriels. Les enzymes artificielles pourraient, par exemple, convertir le maïs en éthanol ou aider à créer de nouveaux médicaments plus rapidement, à bon marché, et efficacement.
Faire un pas de plus vers la réalisation de cet objectif, Rajeev Prabhakar, un chimiste informatique à l'Université de Miami, et ses collaborateurs à l'Université du Michigan ont créé un roman, synthétique, molécule à trois brins qui fonctionne comme une métalloenzyme naturelle, ou une enzyme qui contient des ions métalliques.
"Il n'était pas clair qu'ils pouvaient être fabriqués, mais nous les avons faits. Et, puis nous les avons utilisés pour catalyser avec succès des réactions, " dit Prabhakar, un professeur de chimie qui étudie les réactions enzymatiques dans l'espoir de concevoir leurs analogues artificiels. "Il s'agit d'une étape incrémentielle mais importante dans le développement d'enzymes artificielles, qui a longtemps été considéré comme le Saint Graal de la chimie. Malheureusement, aussi bien que les enzymes naturelles fonctionnent dans notre corps et d'autres formes de vie, ils ne tolèrent pas très bien les autres réglages. Ils sont également très chers et pas faciles à préparer et à purifier."
Pour leur étude révolutionnaire publiée dans Chimie de la nature cette semaine, Prabhakar et l'étudiant diplômé Vindi M. Jayasinghe-Arachchige se sont associés à Vincent L. Pecoraro, professeur de chimie à l'Université du Michigan, pour améliorer les performances des enzymes artificielles que le laboratoire de Pecoraro a mises au point au fil des ans. Les chercheurs du Michigan avaient auparavant créé des métalloenzymes synthétiques plus simples qui catalysaient avec succès un certain nombre de réactions chimiques. Mais ces macromolécules artificielles ont été conçues avec trois identiques, ou des brins "homotrimères" symétriques, lequel, Prabhakar a dit, limité leurs capacités catalytiques.
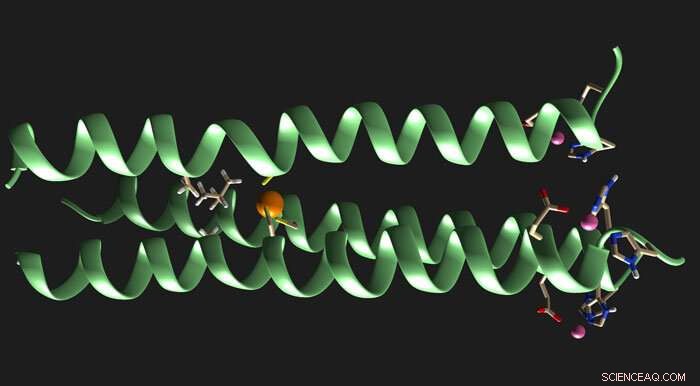
Crédit :Université de Miami
Dans la nouvelle molécule, que Jayasinghe-Arachchige a conçu sur le superordinateur de l'Université de Miami avec les conseils de Prabhakar, le troisième brin diffère par sa structure des deux autres brins. Ses calculs de mécanique quantique ont montré que les plus complexes, non symétrique, structure à trois brins, connu sous le nom de bobine « hétérotrimérique », a élargi les performances catalytiques des métalloenzymes artificielles homotrimériques, une découverte que Pecoraro et son équipe ont confirmée avec des expériences dans son laboratoire du Michigan.
« Nos techniques sont différentes, mais complémentaire, " a déclaré Prabhakar. " Ce que nous faisons, le groupe Pecoraro ne peut pas le faire, et ce qu'ils font, nous ne pouvons pas faire. Nous modélisons des molécules sur ordinateur afin de pouvoir prédire leurs propriétés structurelles et le mécanisme de leurs formations. Ils utilisent nos modèles pour construire la vraie chose, et dans ce cas, c'est le premier exemple d'une molécule hétérotrimérique naturelle."
La plupart des profanes trouveraient probablement l'étude aussi incompréhensible que son titre :« Les bobines enroulées à trois brins hétéromères conçues à l'aide d'une stratégie médiée par un modèle Pb(II)(Cys)3 ». Mais l'essentiel, Prabhakar a dit, est que la recherche collaborative menée à Miami et au Michigan ouvre la porte à une nouvelle stratégie pour parvenir à la création d'enzymes artificielles qui fonctionnent aussi bien que des enzymes naturelles.
En plus de Pecocaro, Prabhakar, et Jayasinghe-Arachchige, les autres co-auteurs de l'étude incluent l'ancien étudiant diplômé de Prabhakar, Thomas J. Paul, maintenant à l'Université du Michigan; Audrey E. Tolbert, Catherine S. Ervin, et Kosh P. Neupane, également de l'Université du Michigan; et Leela Ruckthong, de l'Université de technologie du roi Mongkut, en Thaïlande.
Maintenant dans sa dernière année d'études pour son doctorat en chimie, Jayasinghe-Arachchige a déclaré qu'elle restait fascinée par les progrès des techniques de chimie computationnelle qui lui ont permis de modéliser les structures chimiques et les réactions de la nouvelle molécule.
"Je suis ravi que nos découvertes créent de nouvelles voies vers le développement d'enzymes artificielles efficaces qui peuvent être utilisées pour améliorer la qualité de vie, '' dit Jayasinghe-Arachchige, "et en tant que femme dans un domaine où les femmes sont sous-représentées, J'espère que cette étude motivera les femmes à rejoindre le monde fascinant des domaines STEM."