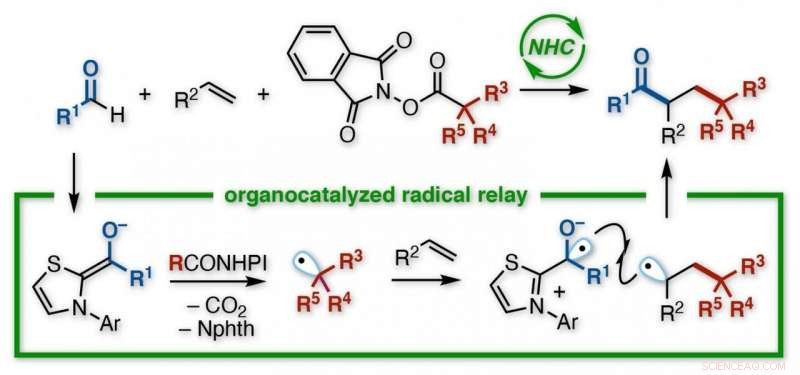
Une équipe de recherche japonaise de l'Université de Kanazawa a développé une réaction pour créer des cétones fonctionnalisées. En utilisant un organocatalyseur carbène N-hétérocyclique (NHC), sans besoin de métaux ni d'irradiation lumineuse, un acyle et un groupe alkyle sont ajoutés à travers la double liaison d'un alcène. Le NHC donne un contrôle régiosélectif sur un processus de relais impliquant un transfert d'électrons suivi de l'ajout successif de deux radicaux sur l'alcène. Les divers produits sont des blocs de construction utiles pour d'autres synthèses. Crédit :Université de Kanazawa
Les chimistes organiques sont des architectes moléculaires, concevoir des structures sophistiquées. Alors que les molécules utilisées en science et en médecine deviennent de plus en plus complexes, de nouveaux outils sont nécessaires pour reconstituer les blocs de construction. Maintenant, une équipe japonaise de l'université de Kanazawa a développé une réaction qui relie trois composants à la fois en utilisant la chimie des radicaux libres.
Doubles liaisons carbone-carbone, connu sous le nom d'alcènes, sont plus réactifs que les liaisons simples. Cela les rend utiles pour connecter différents groupes :si la double liaison est rompue, deux nouvelles molécules peuvent être ajoutées à chaque extrémité, reliés entre eux par l'ancien alcène maintenant à simple liaison.
L'équipe de Kanazawa a cherché des moyens de réaliser cette transformation à l'aide d'aldéhydes, qui contiennent une double liaison entre l'oxygène et le carbone, comme l'une des deux molécules greffées sur un alcène. Comme indiqué dans le Journal de l'American Chemical Society , le but était de créer des cétones hautement fonctionnalisées, une famille importante de composés en synthèse organique.
Leur méthode choisie était une réaction connue, assez évocateur, comme relais radical. Contenant un électron non apparié, et donc une orbitale à moitié vide, les radicaux (ou radicaux libres) ont tendance à être voracement réactifs. Tellement réactif, En effet, qu'ils ne peuvent pas être stockés, mais doit être généré in-situ en éliminant un électron de quelque part au cours d'une réaction, déclenchant une cascade de rupture et de création de liens.
Les chimistes peuvent fabriquer des radicaux de diverses manières, mais l'équipe de Kanazawa voulait tester sur route un oraganocatalyseur, appelé carbène N-hétérocyclique (NHC). Avec un aldéhyde comme réactif, et un ester redox fonctionnalisé comme l'autre, le NHC a déclenché leur transformation en radicaux. Des études antérieures ont laissé entendre que les deux radicaux réagiraient plus rapidement avec un alcène qu'avec l'autre.
"Le défi avec les radicaux est que, étant si instable, ils réagissent souvent avec eux-mêmes, " explique Kazunori Nagao, co-auteur de l'étude. " Ensuite, vous récupérez soit vos matériaux de départ, ou un sous-produit, au lieu de la cible. Nous avons minimisé cela ici. En réalité, la réaction s'est déroulée comme un relais - d'abord le radical alkyle ajouté à un carbone de l'alcène, puis le radical acyle ajouté à l'autre."
Le composé résultant avait une cétone et un groupe dérivé d'ester lié à deux carbones adjacents, dans un arrangement dit vicinal. Bien qu'une réaction directe entre les différents radicaux se soit également produite, donnant un produit à deux composants indésirable, au lieu de la cible à trois composants à pont alcène, c'était mineur. Par ailleurs, une large gamme de matières premières étaient compatibles avec le procédé.
"Deux points cruciaux méritent d'être mentionnés, " dit Hirohisa Ohmiya, auteur correspondant de l'étude. "D'abord, contrairement à certaines réactions, le nôtre est exempt de catalyseurs métalliques et n'a pas besoin d'une source lumineuse pour produire des radicaux, le rendant vert et polyvalent. Seconde, le NHC contrôle précisément le relais, nous pouvons donc être sélectifs dans les positions des groupes fonctionnels. Nous travaillons maintenant sur une version asymétrique pour les produits chiraux."