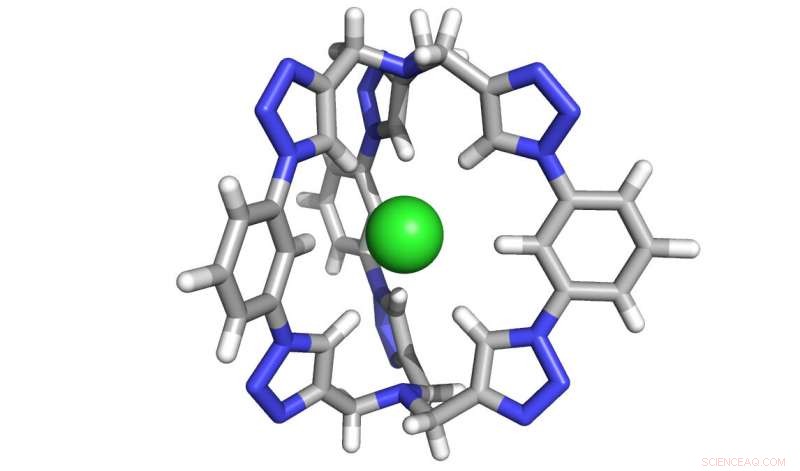
Un rendu informatique de la cage à six molécules de triazole conçue pour capturer les sels de chlorure. Crédit :Yan Liu, Université de l'Illinois à Urbana-Champaign
Des chercheurs de l'Université de l'Indiana ont créé une nouvelle molécule puissante pour l'extraction du sel d'un liquide. Le travail a le potentiel d'aider à augmenter la quantité d'eau potable sur Terre.
Construit à l'aide de liaisons chimiques jusqu'alors considérées comme trop faibles, la nouvelle molécule est environ dix milliards de fois améliorée par rapport à une structure similaire créée il y a plus de 10 ans à IU. La conception des molécules a été publiée le 23 mai dans le journal Science .
"Si vous deviez placer un millionième de gramme de cette molécule dans une tonne d'eau, 100 pour cent d'entre eux pourront encore capturer un sel, " dit Yun Liu, qui a dirigé l'étude en tant que doctorant. étudiant au labo d'Amar Flood, le professeur de chimie James F. Jackson et le professeur Luther Dana Waterman au département de chimie du Bloomington College of Arts and Sciences.
La molécule est conçue pour capturer le chlorure, qui se forme lorsque l'élément chlore s'apparie avec un autre élément pour gagner un électron. Le sel de chlorure le plus connu est le chlorure de sodium, ou du sel de table commun. D'autres sels de chlorure sont le chlorure de potassium, chlorure de calcium et chlorure d'ammonium.
En même temps que la population humaine continue de croître, l'infiltration de sel dans les systèmes d'eau douce réduit l'accès à l'eau potable à travers le monde. Aux États-Unis seulement, le US Geological Survey estime à 271 tonnes métriques de solides dissous, y compris les sels, pénètrent dans les cours d'eau douce chaque année. Les facteurs contributifs comprennent les processus chimiques impliqués dans l'extraction du pétrole, l'utilisation de sels de voirie et d'adoucisseurs d'eau, et l'altération naturelle de la roche. Il suffit d'une cuillère à café de sel pour polluer en permanence cinq gallons d'eau.
La nouvelle molécule d'extraction de sel créée à IU est composée de six "motifs" de triazole - des cycles à cinq chaînons composés d'azote, le carbone et l'hydrogène, qui forment ensemble une "cage" tridimensionnelle parfaitement formée pour piéger le chlorure. En 2008, Le laboratoire de Flood a créé une molécule bidimensionnelle, en forme de beignet plat, qui utilisait quatre triazoles. Les deux triazoles supplémentaires donnent à la nouvelle molécule sa forme tridimensionnelle, et dix milliards de fois plus d'efficacité.
La molécule est également unique car elle lie le chlorure à l'aide de liaisons carbone-hydrogène, auparavant considéré comme trop faible pour créer des interactions stables avec le chlorure par rapport à l'utilisation traditionnelle des liaisons azote-hydrogène. Malgré les attentes, les chercheurs ont découvert que l'utilisation de triazoles créait une cage si rigide qu'elle formait un vide au centre, qui attire les ions chlorure.

Yun Liu détient un modèle imprimé en 3D de la molécule de six triazoles conçue pour capturer les sels de chlorure. Crédit :Fred Zwicky, Université de l'Illinois à Urbana Champaign.
Par contre, les cages avec des liaisons azote-hydrogène sont souvent plus flexibles - et le centre de type vide nécessaire pour la capture du chlorure nécessite un apport d'énergie, abaissant leur efficacité par rapport à une cage à base de triazole.
"Si vous deviez prendre notre molécule et la comparer à d'autres cages qui utilisent des liaisons [plus fortes], nous parlons de plusieurs ordres de grandeur d'augmentation des performances, " a déclaré Flood. " Cette étude montre vraiment que la rigidité est sous-estimée dans la conception des cages moléculaires. "
La rigidité permet également à la molécule de conserver sa forme après la perte du chlorure central, par rapport à d'autres conceptions qui s'effondrent dans les mêmes circonstances en raison de leur flexibilité. Cela confère à la molécule une plus grande efficacité et polyvalence.
Le travail est également reproductible. La première molécule a mis près d'un an à être synthétisée, dit Liu, qui a été choqué de découvrir les cristaux nécessaires pour confirmer la structure unique de la molécule formée après que l'expérience ait été laissée seule dans le laboratoire pendant plusieurs mois - un événement surprenant car ce processus nécessite généralement une surveillance attentive.
La formation du cristal a représenté un moment "eureka", prouver que la conception unique de la molécule était réellement viable. Plus tard, Wei Zhao, chercheur postdoctoral au laboratoire de Flood, a pu recréer la molécule en plusieurs mois.