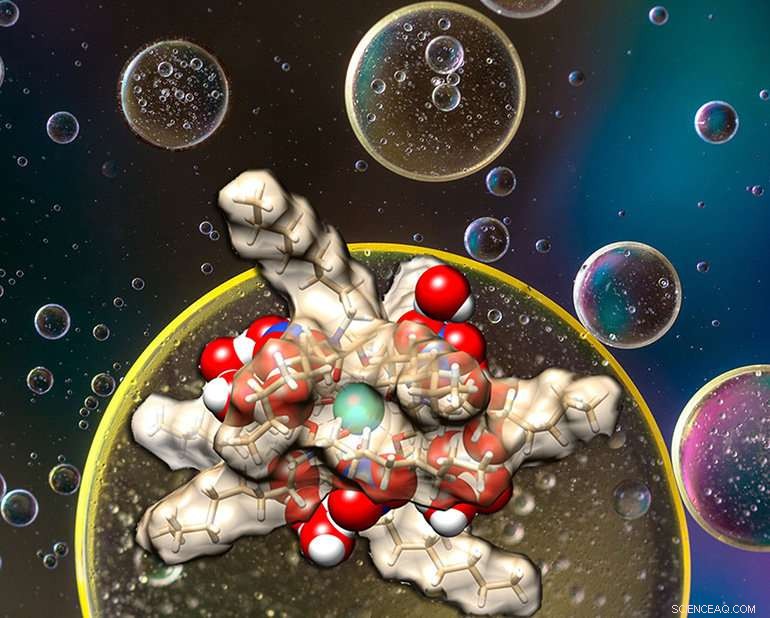
Un extractant enlève un élément d'une mer d'éléments similaires. Les chercheurs ont découvert un arrangement particulier de molécules d'eau de la sphère externe (sphères rouges et blanches) autour d'un extractant (marron). Les molécules d'eau de la sphère extérieure, qui s'enroulent autour de la sphère intérieure de l'extractant contenant des lanthanides, influencer l'efficacité de la séparation pour éliminer la cible (sphère bleue). Crédit :Département américain de l'énergie
Les éléments de lanthanide sont des éléments essentiels des produits de haute technologie d'aujourd'hui, notamment les téléviseurs à écran plat, téléphones portables, voiture électrique, et satellites. Bien que la demande pour ces éléments soit élevée, séparer les lanthanides des impuretés (autres lanthanides) est extrêmement difficile. L'industrie utilise l'extraction liquide-liquide. La cible dans l'eau glisse dans une phase huileuse à l'aide d'une molécule d'extraction. Les impuretés restent dans l'eau. Depuis des décennies, les chercheurs ont conçu de nouveaux extractants. Cependant, ils ont largement négligé les effets subtils des fines couches d'eau qui accompagnent la balade, enroulé autour de la cible. De nouvelles recherches révèlent que des réseaux particuliers de molécules d'eau affectent le fonctionnement de l'extractant.
Les résultats soulignent l'avantage de contrôler les interactions subtiles de la sphère extérieure. L'extraction liquide-liquide des lanthanides est une technologie bien développée. Pourquoi certains extractants sont extrêmement sélectifs et d'autres non n'est pas bien compris. Aussi, comment concevoir une sélectivité améliorée n'est pas bien connu. Savoir comment l'eau extraite avec l'élément cible influence la séparation est une étape essentielle vers la conception de meilleurs systèmes d'extraction. Ces systèmes peuvent obtenir les lanthanides nécessaires aux appareils de haute technologie.
La compréhension fondamentale de la reconnaissance sélective et de la séparation des ions lanthanides par des agents chélatants est d'une importance cruciale pour faire progresser les systèmes énergétiques durables. Les lanthanides sont difficiles à séparer les uns des autres en raison des similitudes de leurs propriétés physiques et chimiques. La plupart des processus de séparation tirent parti d'une petite diminution du rayon ionique qui se produit dans la série des lanthanides. Ces procédés de séparation utilisent deux liquides. Les liquides sont comme l'huile et l'eau. Ils peuvent être mélangés mais toujours séparés en différentes couches. Pendant le mélange, le liquide d'extraction extrait le complexe de lanthanide cible, entouré de couches de molécules d'eau. Le liquide d'extraction contient des bras, appelés ligands, qui attrapent le lanthanide. Pour un ligand idéal, la diminution du rayon ionique entraînerait une augmentation constante de l'extraction à travers la série. C'est-à-dire, les ligands capteraient plus de lutétium (le lanthanide avec le plus petit rayon) que le lanthane (avec le plus grand rayon). Cependant, avec le ligand diglycolamide, l'extraction des lanthanides augmente sur les lanthanides légers à moyens, mais la sélectivité reste presque constante sur les plus petits, lanthanides lourds. La collaboration entre la Colorado School of Mines et le Oak Ridge National Laboratory a permis d'élucider l'origine de la sélectivité des lanthanides grâce à des investigations complémentaires intégrant des études de distribution, calculs de mécanique quantique, et des simulations classiques de dynamique moléculaire.
Les résultats montrent une relation entre l'eau co-extraite et l'extraction des lanthanides par le ligand diglycolamide à travers la série. La découverte souligne l'importance des interactions de liaison hydrogène entre les ions nitrate de la sphère externe sur le ligand et le complexe de lanthanide et les amas d'eau dans un environnement non polaire. Sur la base des études expérimentales et de la théorie fonctionnelle de la densité, le mécanisme sous-jacent à l'absorption d'eau est lié à la surface des contre-ions nitrate disponibles pour interagir avec l'eau co-extraite. Des simulations de dynamique moléculaire élucident davantage que les ions nitrate de la sphère externe sur les ligands forment des liaisons hydrogène avec les molécules d'eau.
Dans une perspective plus large, ces résultats ont des implications importantes pour la conception de nouveaux systèmes et procédés de séparation pour les ions lanthanides trivalents, soulignant l'importance de régler les interactions entre les sphères interne et externe pour obtenir un contrôle total sur la sélectivité dans l'extraction liquide-liquide des lanthanides.