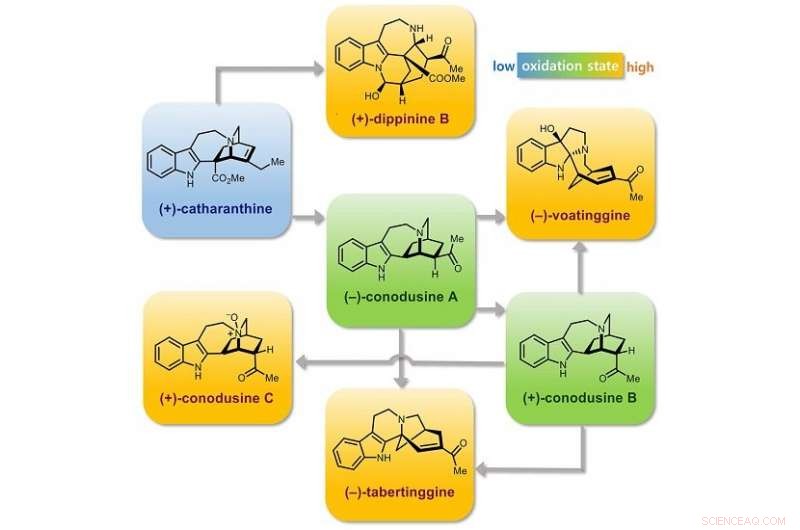
Résumé graphique. Crédit :KAIST
Les chimistes de KAIST ont synthétisé sept produits naturels différents d'iboga et de post-iboga à partir de catharanthine disponible dans le commerce en reflétant la post-modification biosynthétique de la nature du squelette de l'iboga.
Ils ont conçu une nouvelle stratégie pour biosynthétiser les produits naturels via une série de réactions d'oxydation et de réarrangement sélectives et efficaces. Cela servira de tremplin pour le développement de médicaments thérapeutiques contre le cancer et la dépendance aux narcotiques.
L'équipe de recherche, dirigé par le professeur Sunkyu Han, conceptualisé et inventé le terme alcaloïdes « Post-Iboga » pour décrire les produits naturels qui sont biosynthétiquement dérivés d'alcaloïdes de type iboga, qui sont composés de squelettes indole et/ou isoquinuclidine réarrangés.
Les alcaloïdes d'iboga ont attiré l'attention de la communauté scientifique en raison de leurs structures polycycliques intrigantes et de leurs utilisations thérapeutiques potentielles contre les toxicomanies. La nature a évolué pour ajouter des répertoires architecturaux à cette famille de métabolites secondaires en diversifiant les charpentes de l'iboga.
Des exemples notables sont les médicaments anticancéreux approuvés par la FDA, la vinblastine et la vincristine, tous deux dérivés de la dimérisation oxydative des sous-unités catharanthine et vindoline. Certes, les foyers synthétiques vers les dérivés biosynthétiques de l'iboga ont historiquement été sur ces produits naturels dimères susmentionnés.
Des études récentes d'isolement de produits naturels sur les espèces Tabernaemontana corymbosa et Ervatamia officinalis ont abouti à la découverte de divers métabolites secondaires qui sont biosynthétiquement dérivés des alcaloïdes de l'iboga. Ces récentes explosions de rapports d'isolement de produits naturels dérivés de l'iboga ont suscité de l'intérêt pour cette famille de produits naturels.
L'équipe de recherche a utilisé la (+)-catharanthine, la matière première pour la production industrielle du médicament anticancéreux Navelbine. Oxydations bien orchestrées en position C19 et la partie indole du dérivé catharanthine, suivi de réarrangements différentiels en conditions acides, ont fourni respectivement des échantillons synthétiques de voatinggine et de tabertinggine.
D'autre part, des oxydations opportunes en position C19 et en position alpha de la partie amine tertiaire du dérivé catharantine, suivi d'une transhémiminalisation, a produit le premier échantillon synthétique de produit naturel de type chippiine/dippinine, dippinine B.
Il est important de noter que les alcaloïdes de type chippiine et dippinine ont été ciblés parmi les chimistes de synthèse depuis plus de 30 ans, mais n'avaient pas succombé à la synthèse avant ce rapport.