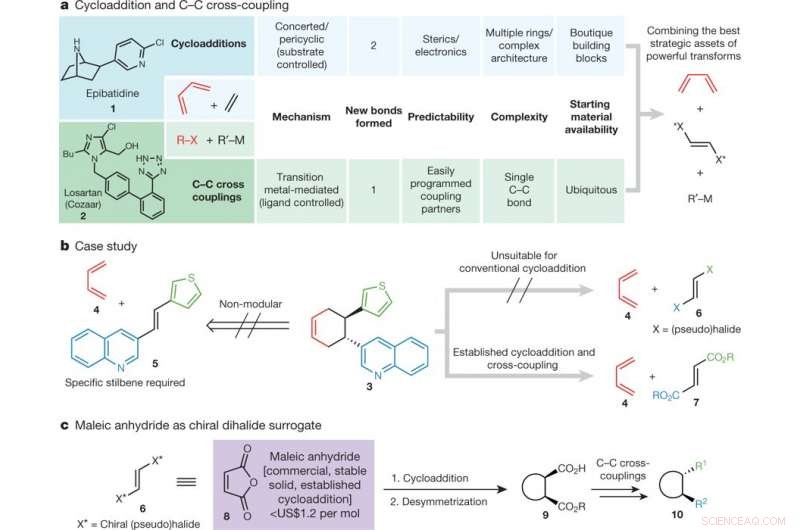
une, Comparaison de la cycloaddition et du couplage croisé C–C. Bu, butyle; R–X, électrophile; R′–M, nucléophile. b, Étude de cas :analyse rétrosynthétique du bloc de construction énantiopure 3. Ce bloc de construction pourrait en théorie être formé par une réaction de Diels-Alder, mais les structures qui seraient utilisées pour cela, 4 et 5, ne sont pas appariés électroniquement et aucune réaction ne se produirait ; de plus, la stratégie n'entraînerait aucune modularité. A la place, un hypothétique dihaloéthylène vicinal (6) pourrait être utilisé; cependant, ceci n'est pas adapté à la cycloaddition classique. 7 est un équivalent synthétique viable. c, L'anhydride maléique peut être utilisé comme substitut dihalogénure chiral disponible et modulaire. Crédit: La nature (2018). DOI :10.1038/s41586-018-0391-9
Les scientifiques de Scripps Research ont développé une nouvelle stratégie puissante pour synthétiser les squelettes moléculaires des produits chimiques utilisés dans les médicaments et autres produits importants, une technique qui offre une flexibilité et une maîtrise sans précédent de la synthèse chimique, selon un article publié le 30 juillet dans La nature .
La méthode, qui combine deux réactions chimiques utilisées pour construire des anneaux moléculaires et lier ensemble des sections de molécules complexes, pourrait accélérer la découverte de nouveaux médicaments en offrant la possibilité de construire simplement et efficacement une grande variété d'architectures moléculaires. Il promet également de fournir une option polyvalente pour synthétiser des produits naturels à partir de zéro en laboratoire.
L'équipe Scripps, dirigé par Phil Baran, Doctorat., a réuni deux manières anciennes de construire des molécules, Couplage croisé C-C et cycloaddition, fournissant une séquence élégante de réactions chimiques qui ont exploité les avantages de chaque méthode.
« Les chimistes ont longtemps dû choisir entre ces deux classes de réaction fidèles, présentant tous deux des avantages marqués, mais aussi des lacunes, " dit Baran, titulaire de la chaire Darlene Shiley en chimie à Scripps Research. "La combinaison de ces deux réactions résout cette dichotomie en tirant parti des forces des deux pour fournir une stratégie fiable et polyvalente pour la production de molécules complexes."
Accouplement croisé C-C, une méthode de formation de liaison hautement fiable et contrôlable, a longtemps été la méthode de choix dans l'industrie pharmaceutique pour synthétiser les squelettes de candidats médicaments. Cependant, le procédé est limité dans sa capacité à construire des architectures tridimensionnelles complexes, résultant en un nombre disproportionné de molécules médicamenteuses plates, une caractéristique qui présente potentiellement un obstacle à la création de nouveaux médicaments pour des cibles biologiques de plus en plus difficiles. Réactions de cycloaddition, en revanche, offrir la possibilité de construire des formes 3D très complexes en une seule étape, mais différents types de réactions de cycloaddition nécessitaient une préparation hautement personnalisée, ce qui limite leur utilité.
Le composé épibatidine, une molécule étudiée comme analgésique potentiel, est un exemple de molécule complexe qui a été synthétisée par cycloaddition. Le médicament contre la pression artérielle Cozaar, un médicament de forme beaucoup plus simple, a été découvert et est fabriqué à l'aide d'un couplage croisé C-C. Baran et son équipe ont cherché à développer un moyen de construire les squelettes de telles molécules d'une manière qui fusionne la capacité de génération de complexité de la cycloaddition avec la fiabilité et la polyvalence du couplage croisé C-C.
Pour faire ça, ils ont résolu l'énigme de choisir une réaction plutôt qu'une autre en les utilisant ensemble. Leur nouvelle stratégie surmonte un certain nombre d'obstacles pour synthétiser des molécules par étapes, en commençant par construire un échafaudage moléculaire par cycloaddition, définir sa forme 3-D, puis utiliser le couplage croisé C-C pour connecter d'autres entités moléculaires à l'échafaudage construit par cycloaddition.
L'équipe Scripps déclare avoir utilisé sa nouvelle méthode pour construire plus de 80 exemples de molécules complexes, y compris les produits naturels (dont l'épibatidine) et les composés actuellement produits à l'échelle industrielle mais avec des méthodes différentes. Dans de nombreux cas, la technique offrait des avantages en termes de moins d'étapes, un rendement plus élevé et la capacité de produire une plus grande variété de formes de certaines molécules.
Le chercheur a été financé par LEO Pharma et les National Institutes of Health (Subvention :GM-118176).
En plus de La nature papier, Baran a également écrit un article fournissant un contexte à la nouvelle technique dans Comptes de la recherche chimique .