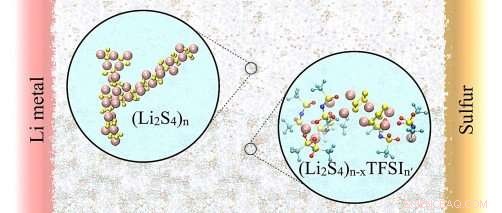
Batteries rechargeables lithium-soufre, où les électrodes sont constituées de lithium (Li) métallique et de soufre (S) séparés par un électrolyte liquide, pourrait remplacer les batteries lithium-ion si nous pouvions comprendre comment arrêter les réactions qui diminuent les performances de la batterie. Pendant le fonctionnement sur batterie, des ions polysulfure sont formés au niveau de l'électrode de soufre, mais ils peuvent se dissoudre dans l'électrolyte et éventuellement limiter les performances de la batterie. Les calculs montrent que la formation d'amas étendus (structure de gauche (Li2S4)n) se produit pour les polysulfures plus courts, ce qui limite la solubilité des ions plus courts dans le solvant pur. Moins de regroupement s'est produit lorsqu'un sel de lithium a été ajouté au solvant pour former l'électrolyte liquide (structure de droite (Li
À l'avenir, Les batteries rechargeables au lithium-soufre (Li-S) pourraient contenir plus d'énergie et coûter moins cher que les batteries lithium-ion si elles pouvaient durer plus longtemps. Un défi majeur consiste à empêcher les ions polysulfure qui doivent se former au niveau de l'électrode de soufre pendant la décharge d'être transportés à travers l'électrolyte liquide vers l'autre électrode. Ici, les chercheurs ont découvert comment la solubilité et le transport des ions polysulfure dans l'électrolyte liquide sont liés à la longueur de la chaîne de l'ion polysulfure, la tendance de l'ion à se regrouper, et la quantité de sel de lithium présent dans l'électrolyte. Il est à noter que les polysulfures de n'importe quelle longueur de chaîne ou structure dissous dans l'électrolyte liquide peuvent contribuer à de moins bonnes performances de la batterie.
L'augmentation de la durée de vie des batteries rechargeables lithium-soufre nécessite d'empêcher le transport de polysulfure entre les électrodes pendant le fonctionnement. La connaissance de la façon dont les molécules de sel et de solvant de l'électrolyte interagissent avec les polysulfures aide à comprendre leur solubilité. Les informations tirées d'études sur ces interactions pourraient aider à la conception de nouveaux électrolytes pour une durée plus longue, batteries rechargeables lithium-soufre pratiques.
La batterie lithium-soufre a une densité énergétique théorique bien supérieure à celle des batteries lithium-ion commerciales; cependant, la technologie présente une décoloration et donc une durée de vie limitée de la batterie. Dans ces batteries, des espèces de soufre actives (sous forme d'ions polysulfure dissous) migrent vers l'électrode de lithium métallique. Puis, des réactions irréversibles impliquant ces polysulfures peuvent se produire au niveau de l'électrode entraînant la perte de sa capacité à stocker des charges. Les tentatives pour protéger le métal des polysulfures n'ont été que partiellement couronnées de succès.
Les scientifiques du Joint Center for Energy Storage Research se sont concentrés sur le réglage de la composition de l'électrolyte pour contrôler la dissolution des polysulfures, mouvement, et interagir. Récemment, en utilisant des études théoriques et expérimentales combinées, les scientifiques ont découvert que la solubilité des polysulfures (Li
Les chercheurs ont également calculé et mesuré expérimentalement les taux de diffusion de l'ion lithium et d'autres espèces dans les électrolytes à différents rapports sel/solvant. Des concentrations élevées de sel pourraient contrôler favorablement la dissolution des polysulfures, mais a entraîné une mobilité réduite pour les espèces ioniques et une conductivité ionique insuffisante. Comprendre la structure et la dynamique des électrolytes lithium-soufre permet d'affiner la composition de l'électrolyte. Avec ces idées, les futurs électrolytes pourraient être conçus pour assurer un transport efficace des ions entre les électrodes, tout en supprimant la dissolution et la migration des espèces polysulfures.