
De gauche, Pei-Shan Yen '16 (doctorat), Ravindra Datta, professeur de génie chimique, et Nicholas Deveau '17 (PhD) du Worcester Polytechnic Institute (WPI) ont développé de nouvelles membranes en métal liquide en sandwich qui pourraient aider à réduire le coût de l'hydrogène pour les véhicules à pile à combustible. Crédit :Worcester Polytechnic Institute (WPI)
Alors que les voitures alimentées par des piles à combustible à hydrogène offrent des avantages évidents par rapport aux véhicules électriques qui gagnent en popularité (y compris leur autonomie plus longue, leur impact environnemental global plus faible, et le fait qu'ils peuvent être ravitaillés en quelques minutes, par rapport aux heures de charge), ils doivent encore décoller avec les consommateurs. L'une des raisons est le coût élevé et la complexité de la production, distribution, et stocker l'hydrogène pur nécessaire à leur alimentation, ce qui a entravé le déploiement des stations de ravitaillement en hydrogène.
Les ingénieurs ont depuis longtemps reconnu la puissance et la disponibilité illimitée de l'hydrogène, l'élément le plus abondant de l'univers. L'hydrogène est naturellement présent dans l'environnement, mais il est presque toujours chimiquement lié à d'autres éléments - à l'oxygène de l'eau (H2O), par exemple, ou au carbone dans le méthane (CH4). Pour obtenir de l'hydrogène pur, il doit être séparé d'une de ces molécules. La quasi-totalité de l'hydrogène produit aux États-Unis est obtenu à partir d'hydrocarbures, principalement du gaz naturel, par reformage à la vapeur, un procédé en plusieurs étapes dans lequel les hydrocarbures réagissent avec de la vapeur à haute température en présence d'un catalyseur pour produire du monoxyde de carbone, gaz carbonique, et l'hydrogène moléculaire (H2).
L'hydrogène peut alors être séparé des autres gaz par un encombrant, processus chimique en plusieurs étapes, mais le coût et la complexité de la production d'hydrogène peuvent être réduits en utilisant une membrane pour effectuer la séparation. La plupart des membranes de séparation d'hydrogène en cours de développement utilisent le métal précieux palladium, qui a une solubilité et une perméance exceptionnellement élevées à l'hydrogène (ce qui signifie que l'hydrogène se dissout facilement et se déplace à travers le métal, tandis que les autres gaz sont exclus). Mais le palladium est cher (il se vend actuellement environ 900 $ l'once) et fragile.
Pour ces raisons, les ingénieurs chimistes ont longtemps recherché des alternatives au palladium pour une utilisation dans les membranes de séparation d'hydrogène, mais si loin, aucun candidat approprié n'a émergé. Une étude pionnière menée par Ravindra Datta, professeur de génie chimique au Worcester Polytechnic Institute (WPI), peut avoir identifié l'alternative au palladium longtemps insaisissable :les métaux liquides.
Une multitude de métaux et d'alliages sont liquides aux températures de fonctionnement standard trouvées dans les systèmes de reformage à la vapeur (environ 500 degrés C), et la plupart d'entre eux sont beaucoup moins chers que le palladium. En outre, une membrane réalisée avec un film de métal liquide ne doit pas être sujette aux défauts et fissures qui peuvent rendre une membrane en palladium inutilisable.
L'étude WPI, publié dans le Journal de l'Institut américain des ingénieurs chimistes , est le premier à démontrer qu'en plus de ces avantages, les membranes en métal liquide semblent également être nettement plus efficaces que le palladium pour séparer l'hydrogène pur des autres gaz, suggérant qu'ils peuvent fournir une solution pratique et efficace au défi de fournir de l'hydrogène abordable pour les véhicules à pile à combustible. "Le récent passage aux voitures électriques est irréversible, " a déclaré Datta. La prochaine étape après les véhicules électriques, lui et d'autres croient, ce sont les véhicules à hydrogène, si le casse-tête de l'approvisionnement en hydrogène est résolu.
Comme les voitures électriques à batterie, les véhicules à pile à combustible ont des moteurs électriques. Les moteurs sont alimentés par l'électricité générée à l'intérieur de la pile à combustible lorsque l'hydrogène et l'oxygène se combinent en présence d'un catalyseur (le seul produit « déchet » est l'eau). Alors qu'ils peuvent tirer l'oxygène de l'air, les voitures doivent transporter une réserve d'hydrogène pur.
De nombreux chercheurs se sont concentrés sur la réduction du coût de cet hydrogène en fabriquant des membranes de palladium meilleures et plus minces. Certaines des membranes les plus avancées ont été produites par le professeur de génie chimique à la retraite du WPI, Yi Hua "Ed" Ma, qui, avec un financement considérable de l'industrie et du département américain de l'Énergie, a lancé un procédé pour lier le palladium à un tube en acier poreux, résultant en des couches de palladium aussi minces que 5 à 10 microns.
L'amincissement de la couche de palladium augmente le flux de la membrane, ou la vitesse à laquelle l'hydrogène pur se déplace à travers elle. "Mais si une membrane est trop fine, " Datta a dit, "il devient fragile ou il développe des défauts. Et les membranes doivent être sans défaut. Si elles développent même une fissure capillaire ou un micropore, il faut recommencer."
Des chercheurs du Worcester Polytechnic Institute (WPI) ont testé un prototype de membrane en métal liquide en sandwich avec cette configuration de laboratoire. La membrane, une fine couche de gallium prise en sandwich entre des supports céramiques poreux, séparait sélectivement l'hydrogène d'un flux de gaz mélangé plus efficacement qu'une membrane de palladium comparable. Crédit :Worcester Polytechnic Institute (WPI)/Curtis Sayers
Il y a six ans, Datta et ses étudiants ont commencé à se demander si les métaux liquides pourraient surmonter certaines des limitations du palladium, en particulier son coût et sa fragilité, tout en potentiellement, offrant une solubilité et une perméabilité supérieures à l'hydrogène. "Outre l'affinité chimique, la perméance dépend de l'ouverture d'une structure cristalline métallique, " at-il dit. " Les métaux liquides ont plus d'espace entre les atomes que les métaux solides, donc leur solubilité et leur diffusabilité devraient être plus élevées. »
Après qu'une revue de la littérature n'ait révélé aucune recherche antérieure sur ce sujet, Datta a demandé avec succès une subvention d'un million de dollars du département américain de l'Énergie pour étudier la faisabilité de l'utilisation de métaux liquides pour la séparation de l'hydrogène. lui et son équipe, les étudiants diplômés Pei-Shan Yen et Nicholas Deveau (Yen a obtenu son doctorat en 2016; Deveau a obtenu le sien en mai), ont décidé de commencer leur exploration avec le gallium, un métal non toxique qui est liquide à température ambiante.
Ils ont mené des travaux fondamentaux qui ont révélé que le gallium était un excellent candidat, car il a démontré une perméance à l'hydrogène significativement plus élevée que le palladium à des températures élevées. En réalité, des études en laboratoire et une modélisation théorique menées par l'équipe ont montré qu'un certain nombre de métaux liquides à des températures plus élevées peuvent avoir une meilleure perméabilité à l'hydrogène que le palladium.
Alors que le gallium liquide était très prometteur en tant que matériau pour la séparation de l'hydrogène, créer une membrane fonctionnelle avec le métal s'est avéré difficile, dit Datta. "Il s'avère que les métaux liquides sont très réactifs, " dit-il. " Vous ne pouvez pas placer du gallium sur un support métallique poreux, comme le professeur Ma l'a fait avec le palladium, car à des températures plus élevées, il forme rapidement des composés intermétalliques qui tuent la perméabilité. » L'équipe a découvert que le métal réagira également avec un certain nombre de matériaux céramiques couramment utilisés comme supports dans les membranes en palladium.
Par la modélisation et l'expérimentation, ils ont compilé une liste de matériaux, y compris les matériaux à base de carbone comme le graphite et le carbure de silicium, qui ne réagissent pas chimiquement avec le gallium liquide mais qui sont également mouillables par le métal liquide, ce qui signifie que le métal s'étalera pour former un film mince sur le matériau de support.
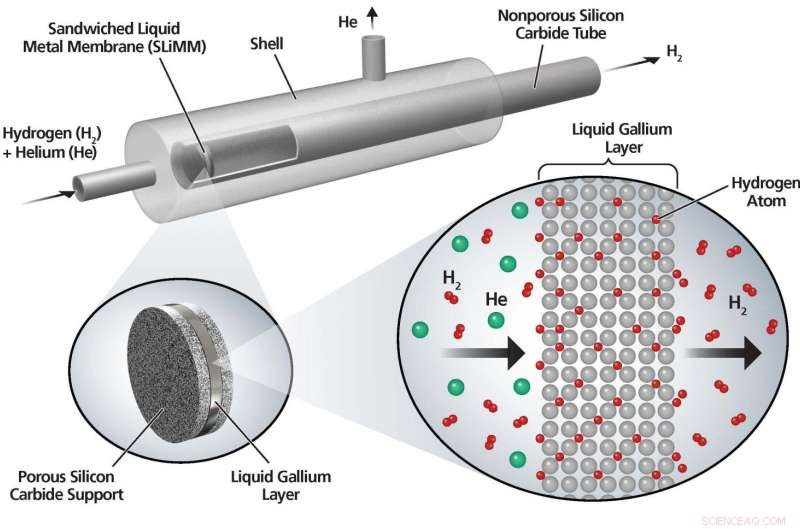
Consciente que la tension superficielle des métaux liquides était susceptible de changer en fonction des variations de température et de la composition des gaz auxquels ils étaient exposés, produisant potentiellement des fuites, ils ont décidé d'insérer le métal entre deux couches de matériau de support pour créer une membrane en métal liquide en sandwich ou SLiMM. Membrane constituée d'une fine couche (deux dixièmes de millimètre) de gallium liquide entre une couche de carbure de silicium et une couche de graphite, a été construit en laboratoire et testé pour la stabilité et la perméabilité à l'hydrogène.
La membrane a été exposée à une atmosphère d'hydrogène pendant deux semaines à des températures allant de 480 à 550 degrés C. Les résultats ont montré que le film de gallium liquide était jusqu'à 35 fois plus perméable à l'hydrogène qu'une couche comparable de palladium et que la diffusion de l'hydrogène à travers la membrane prise en sandwich était considérablement plus haute que pour une membrane de palladium typique. Le test a également montré que les membranes étaient sélectives, ne laissant passer que l'hydrogène.
"Ces tests ont confirmé nos hypothèses selon lesquelles les métaux liquides pourraient être des candidats appropriés pour les membranes de séparation d'hydrogène, " Datta a dit, « suggérant que ces matériaux pourraient être le substitut recherché depuis longtemps pour le palladium. Il y a encore une multitude de questions auxquelles il faut encore répondre, y compris si les petites membranes que nous avons construites en laboratoire peuvent être agrandies et si les membranes seront résistantes aux substances présentes dans les gaz reformés (y compris le monoxyde de carbone et le soufre) qui sont connus pour empoisonner les membranes en palladium.
"Mais en démontrant la faisabilité des membranes en métal liquide prises en sandwich, nous avons ouvert la porte à un nouveau domaine très prometteur de la recherche sur l'hydrogène énergie, " Datta a ajouté, "car il y a beaucoup d'autres métaux et alliages, au-delà du gallium, qui sont liquides à 500 degrés C. C'est un vaste champ ouvert, en termes de matériaux que vous pourriez utiliser. Aussi, cela pose une foule de questions scientifiques intéressantes."