
Les scientifiques ont développé un nouveau catalyseur recouvert de molybdène qui empêche une réaction indésirable dans certains systèmes chimiques qui divisent l'eau en hydrogène et oxygène. Crédit :Andy Freeberg/SLAC National Accelerator Laboratory
L'hydrogène est l'un des carburants propres les plus prometteurs pour une utilisation dans les voitures, maisons et génératrices portatives. Lorsqu'il est produit à partir d'eau à l'aide de ressources énergétiques renouvelables, c'est aussi un carburant durable sans empreinte carbone.
Cependant, les systèmes de séparation de l'eau nécessitent un catalyseur très efficace pour accélérer la réaction chimique qui sépare l'eau en hydrogène et oxygène, tout en empêchant les gaz de se recombiner dans l'eau. Désormais une équipe de recherche internationale, y compris des scientifiques du laboratoire national d'accélérateurs SLAC du ministère de l'Énergie, a développé un nouveau catalyseur avec un revêtement en molybdène qui empêche cette réaction de retour problématique et fonctionne bien dans des conditions de fonctionnement réalistes.
Une partie clé du développement a porté sur la compréhension du fonctionnement du revêtement de molybdène à l'aide d'expériences à la source lumineuse de rayonnement synchrotron de Stanford (SSRL) du SLAC, une installation utilisateur du DOE Office of Science. Les scientifiques ont communiqué leurs résultats le 13 avril dans Angewandte Chemie .
"Lorsque vous divisez l'eau en hydrogène et oxygène, les produits gazeux de la réaction sont facilement recombinés en eau et il est crucial d'éviter cela, " dit Angel Garcia-Esparza, auteur principal et actuellement chercheur postdoctoral à l'Ecole Normale Supérieure de Lyon. "Nous avons découvert qu'un catalyseur recouvert de molybdène est capable de produire sélectivement de l'hydrogène à partir de l'eau tout en inhibant les réactions inverses de la formation d'eau."
Les expériences ont démontré que leur stratégie de revêtement de molybdène a des applications dans les dispositifs d'électrocatalyse et de photocatalyse, ajouta Garcia-Esparza. Ce sont des dispositifs qui aident à faire avancer une réaction en utilisant l'électricité ou la lumière.
À la recherche de la stabilité
Garcia-Esparza a aidé à développer le nouveau catalyseur en tant qu'étudiant diplômé à l'Université des sciences et technologies King Abdullah (KAUST) en Arabie saoudite sous la direction de Kazuhiro Takanabe, professeur agrégé de sciences chimiques à la KAUST. Le groupe de recherche de Takanabe a exploré la stabilité, performance et fonction de nombreux éléments différents avant de choisir le molybdène comme revêtement pour un catalyseur standard à base de platine.
"Trouver un revêtement qui fonctionne bien dans l'électrolyte acide utilisé pour le fractionnement de l'eau a été un défi majeur pour mes collaborateurs, car de nombreux matériaux se dégradent rapidement dans des conditions acides, " a déclaré le co-auteur Dimosthenis Sokaras, un scientifique du SLAC.
Parmi les revêtements qu'ils ont testés, "Le molybdène était le matériau le plus performant en milieu acide, où les conditions de dégagement d'hydrogène sont favorables et faciles, " expliqua Garcia-Esparza.
Tester les performances
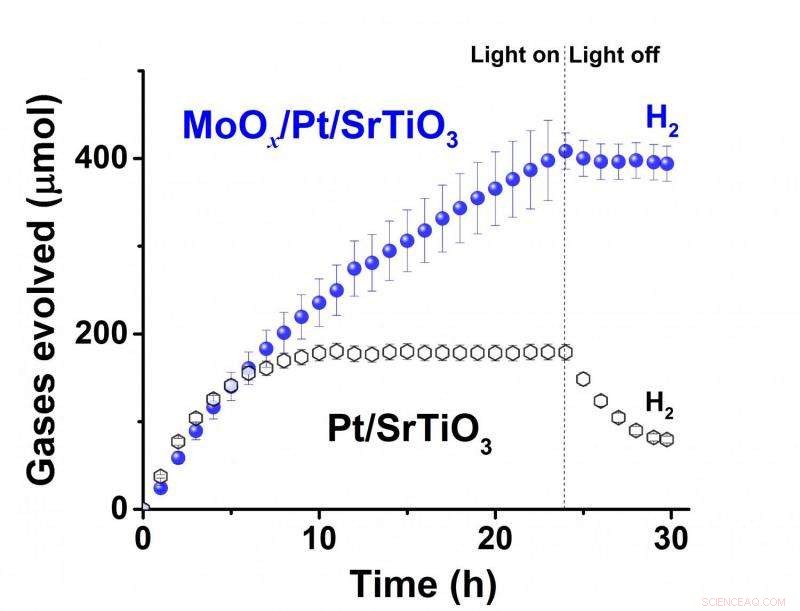
Graphique de la performance de séparation photocatalytique de l'eau d'un catalyseur Pt/SrTiO3 à 0,3 % en poids avec et sans revêtement de Mo sous irradiation UV. Le catalyseur revêtu de Mo a généré des quantités croissantes d'hydrogène gazeux pendant 24 heures avec la lumière allumée, et inhibe la reformation de l'eau lorsque la lumière est éteinte. Tandis que, le catalyseur non revêtu a augmenté la production d'hydrogène pendant seulement six heures avec la lumière allumée et le niveau a diminué lorsque la lumière était éteinte en raison de la formation d'eau. La production d'oxygène a suivi un schéma similaire mais à la moitié de la quantité d'hydrogène, puisque l'eau a deux atomes d'hydrogène pour chaque atome d'oxygène. Crédit :Angel Garcia-Esparza/KAUST
Un autre défi majeur était de trouver un moyen de mesurer les propriétés de leur catalyseur recouvert de molybdène, car ces composés de molybdène ne sont pas stables lorsqu'ils sont exposés à l'air. " Sortir le catalyseur de l'eau perturbe l'identité du matériau, " dit Garcia-Esparza. " Par conséquent, il a fallu étudier l'électrocatalyseur en conditions de travail, ce qui est difficile."
Garcia-Esparza a donc passé un été à effectuer des expériences d'électrochimie à SSRL pour caractériser le nouveau catalyseur dans des conditions opérationnelles. "L'idée était de travailler ensemble pour voir comment le catalyseur revêtu de molybdène fonctionnait et déterminer sa structure électronique lorsqu'il fonctionnait, " a déclaré Sokaras. "Nous voulions comprendre pourquoi la réaction de retour ne se produit pas."
Ils ont testé un catalyseur au platine nu, avec et sans revêtement en molybdène, lors de l'électrolyse de l'eau à SSRL, utilisant in operando la spectroscopie d'absorption des rayons X avec une cellule électrochimique sur mesure. « Chez SSRL, nous avons essentiellement pu faire de l'électrochimie tout en analysant l'échantillon avec un rayonnement synchrotron, " Garcia-Esparza a déclaré. "Les expériences réalisées au SLAC étaient la dernière pièce du puzzle pour déterminer la structure locale et l'état de l'électrocatalyseur dans les conditions opérationnelles de la production d'hydrogène."
"Nos résultats soutiennent que la couche de molybdène agit comme une membrane pour empêcher les gaz d'oxygène et d'hydrogène d'atteindre près de la surface du platine, qui empêche la formation d'eau, ", a déclaré Sokaras.
En outre, l'équipe de recherche a exploré les applications de la photocatalyse. Ils ont construit un système de fractionnement d'eau photocatalytique en utilisant soit un catalyseur standard de platine sur oxyde de strontium et de titane (Pt/SrTiO3), soit le même catalyseur recouvert de molybdène. Les deux systèmes ont été testés chez KAUST avec les lumières allumées et éteintes, c'est-à-dire avec et sans source d'énergie entraînant la réaction de séparation de l'eau.
Quand la lumière était allumée, le catalyseur standard Pt/SrTiO3 a augmenté la production d'hydrogène pendant seulement six heures parce que le système a perdu son efficacité en raison de la réaction inverse. Lorsque les lumières ont ensuite été éteintes, la quantité d'hydrogène diminuait avec le temps, vérifiant que des quantités importantes de gaz se recombinaient pour former de l'eau.
En revanche, le catalyseur revêtu de molybdène divise en continu l'eau pour générer des quantités croissantes d'hydrogène gazeux pendant 24 heures, produisant environ deux fois plus d'hydrogène gazeux que le catalyseur standard en une journée. En outre, la quantité d'hydrogène est restée stable dans l'obscurité, confirmant que le revêtement a inhibé la formation d'eau
Ces résultats sont prometteurs, mais il reste encore du travail à faire avant que le catalyseur puisse être utilisé dans un dispositif pratique. Sokaras a dit, "Je pense que nous sommes loin de parler réellement d'un appareil commercial, mais c'est certainement une énorme amélioration d'avoir ce nouveau matériau de catalyseur qui empêche la réaction en retour. Nous devons maintenant trouver un moyen de rendre le revêtement plus stable afin qu'il produise de l'hydrogène encore plus longtemps."