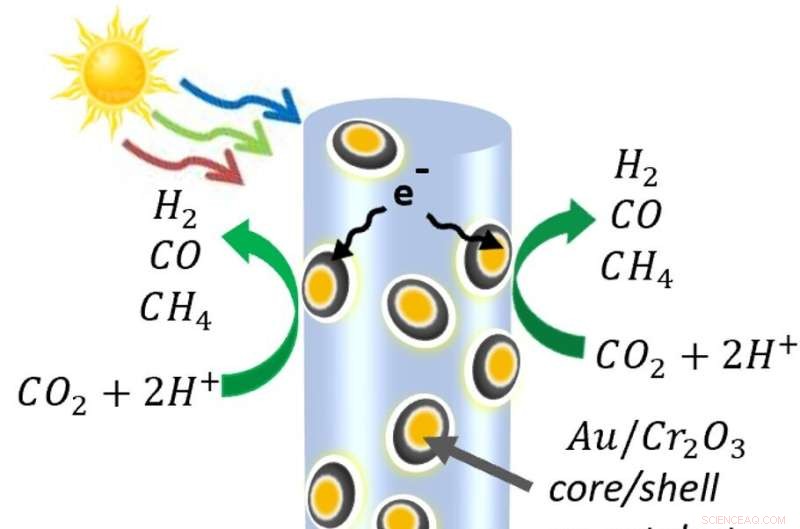
Un schéma des nanofils semi-conducteurs constitués d'indium, de gallium et d'azote - décorés de nanoparticules d'or et d'oxyde de chrome. Lorsque la lumière atteint le nanofil, elle libère des électrons et les "trous" chargés positivement que les électrons laissent derrière eux. Sur le nanofil lui-même, les trous oxydent l'eau en protons (hydrogène) et en oxygène. Pendant ce temps, certains électrons sont attirés dans les nanoparticules métalliques, où ils décomposent le dioxyde de carbone. Les molécules se recombinent en molécules de monoxyde de carbone, d'hydrogène et de méthane qui composent le gaz de synthèse. Crédit :Roksana Rashid, Université McGill.
Le gaz de synthèse à énergie solaire pourrait recycler le dioxyde de carbone en carburants et en produits chimiques utiles, a montré une équipe internationale de chercheurs.
"Si nous pouvons générer du gaz de synthèse à partir de dioxyde de carbone en utilisant uniquement l'énergie solaire, nous pouvons l'utiliser comme précurseur pour le méthanol et d'autres produits chimiques et carburants. Cela réduira considérablement le CO2 global. », a déclaré Zetian Mi, professeur de génie électrique et informatique à l'Université du Michigan, qui a dirigé l'étude publiée dans les Proceedings of the National Academy of Science .
Composé principalement d'hydrogène et de monoxyde de carbone avec un peu de méthane, le gaz de synthèse est couramment issu des énergies fossiles à l'aide de l'électricité. De plus, des produits chimiques toxiques sont souvent ajoutés pour rendre le processus plus efficace.
"Notre nouveau procédé est en fait assez simple, mais c'est excitant parce qu'il n'est pas toxique, il est durable et très rentable", a déclaré Roksana Rashid, premier auteur de l'étude, qui a réalisé les expériences en tant que doctorant en génie électrique et informatique à Université McGill au Canada.
Pour créer un processus qui utilise uniquement l'énergie solaire, le groupe de Mi a surmonté la difficulté de séparer les molécules de dioxyde de carbone, qui sont parmi les plus stables de l'univers. Pour cela, ils ont parsemé une forêt de nanofils semi-conducteurs de nanoparticules. Ces nanoparticules, constituées d'or recouvert d'oxyde de chrome, ont attiré les molécules de dioxyde de carbone et les ont pliées, affaiblissant les liaisons entre le carbone et l'oxygène.
Les nanofils de nitrure de gallium ont utilisé l'énergie lumineuse pour libérer les électrons et les espaces chargés positivement qu'ils laissent derrière eux, appelés trous. Les trous divisent les molécules d'eau, séparant les protons (hydrogène) de l'oxygène. Ensuite, au niveau des catalyseurs métalliques, les électrons séparent le dioxyde de carbone, produisant du monoxyde de carbone et aspirant parfois l'hydrogène libre pour produire du méthane. Des procédés sont en cours de développement pour séparer l'oxygène des autres gaz.
"Notre technologie met en lumière la manière de construire une production distribuée de gaz de synthèse à partir de l'air, de l'eau et de la lumière du soleil", a déclaré Baowen Zhou, co-auteur correspondant de l'étude avec Mi et ancien chercheur postdoctoral dans le laboratoire de Mi à l'Université McGill et à l'UM.
En modifiant le rapport or/oxyde de chrome dans les nanoparticules, l'équipe de Mi a pu contrôler les quantités relatives d'hydrogène et de monoxyde de carbone produites lors de la réaction. Ceci est important car le rapport hydrogène/monoxyde de carbone affecte la facilité de production d'un type de carburant ou de produit chimique.
"Ce qui est surprenant, c'est la synergie entre l'or et l'oxyde de chrome pour faire du CO2 réduction au gaz de synthèse efficace et réglable. Cela n'était pas possible avec un seul catalyseur métallique", a déclaré Mi. "Cela ouvre de nombreuses opportunités passionnantes qui n'avaient pas été envisagées auparavant."
La configuration de gaz de synthèse réglable de Mi utilise des processus de fabrication industriels standard et est évolutive. Alors que Rashid a utilisé de l'eau distillée dans cette expérience, l'eau de mer et d'autres solutions d'électrolytes devraient également fonctionner, et Mi les a utilisées dans des études connexes sur la séparation de l'eau.
"Le semi-conducteur que nous utilisons comme absorbeur de lumière est à base de silicium et de nitrure de gallium, qui sont les semi-conducteurs les plus couramment produits, et nous utilisons très peu de matériau pour le nitrure de gallium. Chaque nanofil a une épaisseur d'environ un micromètre", a déclaré Mi.
Le prochain objectif de Mi est d'augmenter l'efficacité de l'appareil, qui se situe actuellement à 0,89 %. Lorsque 10% de l'énergie lumineuse est convertie en énergie chimique, il espère que la technologie pourrait voir la technologie être adoptée pour les énergies renouvelables, similaires aux cellules solaires. Le 'méthane vert' issu de la photosynthèse artificielle pourrait recycler le CO2