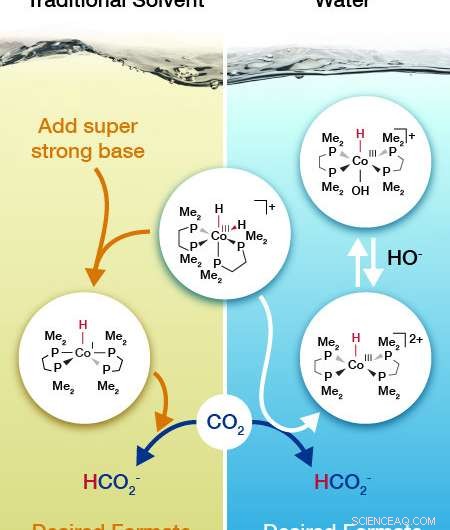
Les chercheurs en catalyse ont déterminé que le catalyseur à base de cobalt (au centre) emprunte un chemin différent pour ajouter de l'hydrogène au dioxyde de carbone selon qu'il se trouve dans l'eau ou dans un autre solvant. Crédit :Nathan Johnson
Travailler dans de bonnes conditions permet de réaliser facilement un travail. Mais et si vous pouviez passer de bon à excellent ? C'est ce que les scientifiques ont fait pour un catalyseur populaire qui entraîne la conversion du dioxyde de carbone en une matière première prometteuse connue sous le nom de formiate. Un catalyseur à base de cobalt abondant sur Terre entraîne la réaction dans un solvant avec une base super forte qui est coûteuse. Avec quelques calculs au fond de l'enveloppe, Le Dr Eric Wiedner et ses collègues du Pacific Northwest National Laboratory du DOE ont prédit que le catalyseur au cobalt pourrait prendre un chemin de réaction différent pour fonctionner dans l'eau avec du bicarbonate de sodium peu coûteux, communément appelé bicarbonate de soude. Le résultat? Le catalyseur est le catalyseur de métaux non précieux le plus performant pour la conversion du dioxyde de carbone dans l'eau.
"En utilisant des prédicteurs thermodynamiques pour concevoir des catalyseurs, nous avons évité l'approche au fusil de chasse et le temps et les coûts associés, " a déclaré Wiedner. "Nous comprenons comment contrôler la thermodynamique du catalyseur, et sont maintenant capables d'étendre nos découvertes pour concevoir de nouveaux systèmes catalytiques."
Les travaux de l'équipe montrent que l'environnement réactionnel, y compris le catalyseur, solvant, et socle, influence fortement la réaction. Dans ce cas, l'environnement détermine le déroulement de la réaction. Comprendre l'influence de l'environnement est crucial pour concevoir les meilleurs catalyseurs. Et les meilleurs catalyseurs sont nécessaires pour transformer un polluant commun en un produit chimique qui peut servir de bloc de construction pour la fabrication de carburants et de produits chimiques à base d'hydrocarbures.
Et si le dioxyde de carbone polluant pouvait être utilisé comme matière première pour des produits chimiques précieux ? La molécule serait transformée en un bloc de construction d'hydrocarbure. Comment? En ajoutant d'abord de l'hydrogène pour créer du formiate (HCOO-). Un grand défi consiste à trouver un système catalytique capable de piloter la réaction sans recourir à des produits chimiques coûteux. Une équipe de recherche du Pacific Northwest National Laboratory a conçu un système de catalyseur à base de cobalt qui fonctionne dans l'eau. Le catalyseur est le meilleur lorsqu'il s'agit de conduire la réaction dans l'eau sans compter sur des métaux précieux ou des bases coûteuses.
L'équipe a prédit comment le catalyseur réagirait avec le dioxyde de carbone en fonction de l'impact attendu du solvant sur le transfert d'hydrure (H-), dans le but de travailler dans l'eau. Le mécanisme était différent de ceux qui se produisent dans le solvant traditionnel, tétrahydrofurane. Le mécanisme résultant repose sur du bicarbonate de sodium peu coûteux au lieu d'une base forte et coûteuse.
Guidé par les prédictions, l'équipe a testé le catalyseur dans l'eau avec du dioxyde de carbone. Ils ont caractérisé les performances du catalyseur par spectroscopie de résonance magnétique nucléaire à haute pression à l'aide d'une cellule personnalisée développée et construite au PNNL. "C'est une technique rare et puissante dans la communauté de la catalyse, " a déclaré Wiedner. L'analyse de l'équipe a démontré que le catalyseur avait fonctionné comme prévu.