Les maladies auto-immunes comptent parmi les maladies chroniques les plus répandues dans le monde. Les traitements émergents pour les maladies auto-immunes se concentrent sur les « thérapies cellulaires adoptives », ou celles utilisant des cellules du corps d'un patient pour obtenir une immunosuppression. Ces cellules thérapeutiques sont reconnues par le corps du patient comme étant « le soi », limitant ainsi les effets secondaires, et sont spécifiquement conçues pour localiser l'effet thérapeutique souhaité.
Dans le traitement des maladies auto-immunes, les thérapies cellulaires adoptives actuelles se sont largement centrées sur les lymphocytes T régulateurs (Treg ), qui est définie par l’expression de la protéine 3 de la boîte Forkhead, ou Foxp3. Bien que les Tregs offrent un grand potentiel, leur utilisation à des fins thérapeutiques reste un défi majeur. En particulier, les méthodes d'administration actuelles entraînent une ingénierie inefficace des cellules T.
Tregs ne composent qu’environ 5 à 10 % des cellules mononucléées du sang périphérique en circulation. De plus, les Tregs manquent de marqueurs de surface plus spécifiques qui les différencient des autres populations de lymphocytes T. Ces obstacles rendent difficile la récolte, la purification et la culture des Tregs à des numéros thérapeutiquement pertinents. Bien qu'il existe d'autres Tregs résidant dans les tissus dans les organes non lymphoïdes tels que les muscles squelettiques et le tissu adipeux viscéral, ces Tregs sont très inaccessibles et peu nombreux.
Aujourd'hui, une équipe de recherche dirigée par Michael Mitchell, professeur agrégé de bio-ingénierie à l'École d'ingénierie et de sciences appliquées de l'Université de Pennsylvanie, a développé une plate-forme de nanoparticules lipidiques (LNP) pour délivrer l'ARN messager (ARNm) Foxp3 aux cellules T pour des applications. en auto-immunité. Leurs découvertes sont publiées dans la revue Nano Letters. .

"Les principaux défis associés à l'ingénierie cellulaire ex vivo (en dehors du corps) sont l'efficacité, la toxicité et la mise à l'échelle :nos nanoparticules lipidiques d'ARNm (LNP d'ARNm) nous permettent de surmonter tous ces problèmes", explique Mitchell. "La nouveauté de nos travaux vient de trois éléments majeurs :premièrement, l'utilisation de l'ARNm, qui permet la génération de cellules immunosuppressives transitoires ; deuxièmement, l'utilisation de LNP, qui permettent une délivrance efficace de l'ARNm et une ingénierie cellulaire efficace ; et enfin, la ingénierie ex vivo de cellules T humaines primaires pour les maladies auto-immunes, offrant le pipeline le plus direct pour la traduction clinique de cette thérapie, du banc au chevet. "
"À notre connaissance, il s'agit de l'une des premières plates-formes d'ARNm LNP à avoir été utilisée pour concevoir des cellules T destinées à des thérapies auto-immunes", poursuit-il. "D'une manière générale, cette plateforme peut être utilisée pour concevoir des thérapies cellulaires adoptives pour des maladies auto-immunes spécifiques et peut potentiellement être utilisée pour créer des pistes thérapeutiques pour les allergies, la transplantation d'organes et au-delà."
La délivrance de la protéine Foxp3 aux cellules T a été difficile car les protéines ne traversent pas facilement la membrane cellulaire. "L'ARNm code pour la protéine Foxp3, qui est un facteur de transcription qui rend les cellules T immunosuppressives plutôt qu'actives", explique le premier auteur Ajay Thatte, doctorant et boursier NSF au Mitchell Lab. "Ces lymphocytes T modifiés peuvent supprimer la fonction des lymphocytes T effecteurs, ce qui est important car l'hyperactivité des lymphocytes T est un phénotype courant dans les maladies auto-immunes."
De plus, la taille, la charge et la complexité relativement faible de l’ARNm lui permettent d’être facilement conditionné dans des systèmes d’administration efficaces tels que les LNP ionisables, qui se sont révélés être une plate-forme d’administration puissante, en particulier pour l’ARNm, comme le démontre le succès des vaccins contre la COVID-19. .
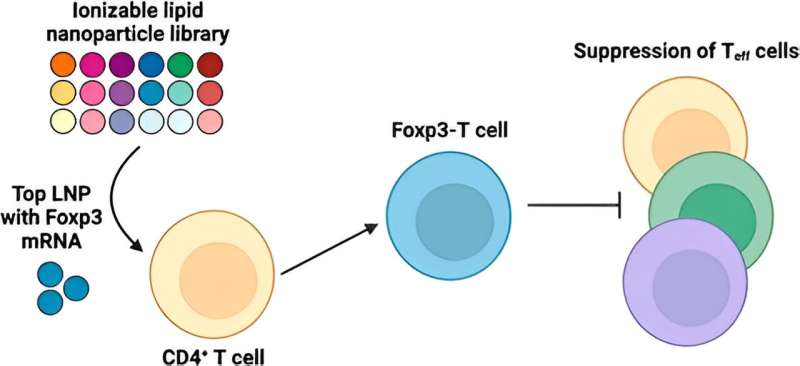
Dans la nouvelle étude, Mitchell et son équipe ont d'abord examiné une bibliothèque de 18 LNP uniques afin d'identifier une LNP la plus performante pour l'administration d'ARNm au CD4 humain + . Cellules T. Ensuite, ils ont reformulé ce LNP pour que l’ARNm de Foxp3 génère des cellules Foxp3-T, vérifiant que les cellules supprimaient efficacement la prolifération des cellules T effectrices. Les résultats démontrent le potentiel de l'utilisation des LNP d'ARNm pour concevoir des thérapies cellulaires immunosuppressives pour les maladies auto-immunes et bien plus encore.
Dans les études futures, l’équipe prévoit d’examiner l’effet suppresseur de ces cellules Foxp3-T modifiées sur d’autres cellules immunitaires telles que les macrophages et les cellules dendritiques. Ils espèrent ensuite transférer les cellules Foxp3-T modifiées dans des modèles murins de maladies auto-immunes pour tester leur efficacité et leur effet immunologique. Enfin, ils chercheront à développer des LNP ciblées pour délivrer l'ARNm de Foxp3 aux cellules T circulant dans le corps, établissant ainsi une plate-forme d'ingénierie in situ pour les thérapies contre les maladies auto-immunes.
"Bien que largement explorée dans les applications contre le cancer, l'ingénierie des cellules immunitaires en dehors du corps a été moins explorée pour les applications d'auto-immunité. De plus, il est extrêmement difficile d'atteindre une efficacité élevée et une faible toxicité pendant le processus d'ingénierie cellulaire", explique Mitchell. "Notre technologie LNP permet une ingénierie simple et efficace de cellules T à faible toxicité. Nos cellules T modifiées peuvent être utilisées dans une gamme de troubles immunitaires hyperactifs."
Plus d'informations : Ajay S. Thatte et al, Nanoparticules lipidiques d'ARNm pour l'ingénierie ex vivo de cellules T immunosuppressives pour les thérapies auto-immunes, Nano Letters (2023). DOI :10.1021/acs.nanolett.3c02573
Informations sur le journal : Lettres nano
Fourni par l'Université de Pennsylvanie