Les patients souffrant de certaines maladies chroniques doivent souvent attendre des années pour obtenir un diagnostic approprié. Par exemple, des symptômes tels que l'essoufflement peuvent être attribués à de nombreux troubles pulmonaires et cardiovasculaires, de sorte que les patients peuvent être traités pour une maladie mal diagnostiquée qui est loin d'être un diagnostic et un traitement précis.
Par conséquent, l’une des méthodes les plus prometteuses pour résoudre ce problème consiste à suivre les niveaux de composés spécifiques dans le corps au cours du développement d’une maladie spécifique. Allant dans cette direction, des scientifiques de l'Institut de chimie physique de l'Académie polonaise des sciences (Varsovie, Pologne) et de l'Université nationale de Kaohsiung à Kaohsiung (Kaohsiung, Taiwan) ont présenté leurs recherches sur le développement d'une méthode de diagnostic rapide et efficace d'un virus mortel. maladie pulmonaire.
La fibrose pulmonaire idiopathique (FPI) est une maladie chronique provoquant une fibrose pulmonaire aux conséquences mortelles, conduisant à la suffocation. Ses symptômes les plus courants sont la toux sèche et l’essoufflement, qui peuvent être associés à de multiples troubles. Ainsi, il peut souvent être diagnostiqué à tort comme étant de nombreuses maladies différentes, ce qui rend le diagnostic précis long et ardu, affectant considérablement la qualité de vie du patient.
De plus, les symptômes peuvent être retardés jusqu’à ce qu’il soit trop tard pour traiter le patient avec succès. Le développement de la FPI reste encore un mystère médical. Il existe donc un énorme besoin d’un diagnostic précoce de la FPI. La détection électrochimique des biomarqueurs IPF est l’une des solutions. Les biomarqueurs sont des composés spécifiques, par exemple des protéines, des acides nucléiques ou d'autres composés produits anormalement par l'organisme au cours du développement d'une maladie. Pour la FPI, plusieurs biomarqueurs peuvent être distingués.
L’un d’eux est la métalloprotéinase matricielle-1 (MMP-1), qui dégrade les collagènes fibrillaires dans les voies respiratoires. Malgré les propriétés chimiques bien connues de la MMP-1, la surveillance rapide de ce biomarqueur dans les fluides corporels dans le cadre de la progression de la FPI est désormais loin d'être un diagnostic de rêve.
Récemment, des chercheurs de l'Institut de chimie physique de l'Académie polonaise des sciences (IPC PAS) à Varsovie (Pologne), en collaboration avec des scientifiques du Département de génie chimique et des matériaux de l'Université nationale de Kaohsiung à Kaohsiung (Taiwan), ont ciblé des suivez l'IPF et effectuez des diagnostics rapides en concevant un nouveau chimiocapteur électrochimique pour une détermination sélective, rapide et efficace du biomarqueur de l'IPF, en particulier de la MMP-1.
Pour préparer ce chimiocapteur, les chercheurs se sont appuyés sur l'empreinte moléculaire dans des polymères, une technique basée sur le mélange d'un monomère fonctionnel, d'un agent de réticulation et d'un modèle, suivi de la génération d'une matrice polymère qui forme des cavités moléculaires en forme de (molécule modèle) correspondant une clé moléculaire qui s'insère dans le verrou polymère.
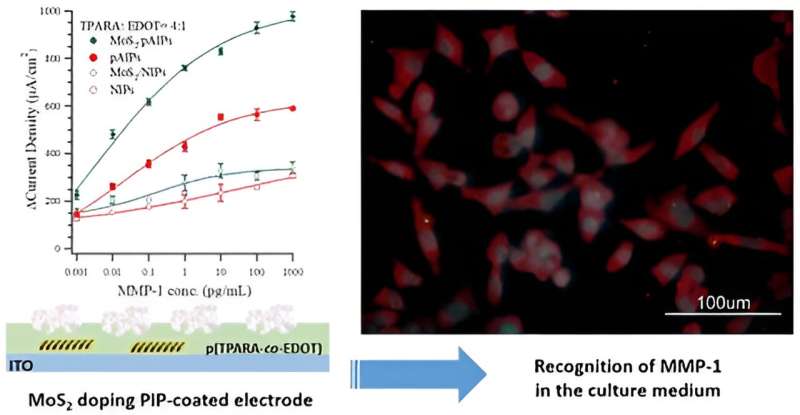
Plus précisément, ils ont modifié l'électrode transparente (une lame de verre recouverte d'oxyde d'indium-étain conducteur appelé ITO) avec un polymère à empreinte moléculaire (MIP), poly(TPARA-co-EDOT), fabriqué à partir de deux monomères, EDOT et TPARA. De plus, dopé avec un MoS2 -Matériau feuilleté 2D, le MIP a été calqué avec l'épitope peptidique du biomarqueur protéique MMP-1.
Ensuite, cette matrice a été retirée du MIP, laissant des cavités moléculaires d’une forme et d’une taille caractéristiques des molécules d’épitopes peptidiques utilisées pour l’empreinte. Puisque les cavités correspondent à ces molécules peptidiques caractéristiques, le MIP peut facilement être utilisé pour déterminer la molécule correspondante. Curieusement, doper le MIP avec MoS2 a considérablement amélioré la limite de détection de MMP-1 par rapport au MIP non dopé.
Le Dr Piyush S. Sharma affirme :"L'incorporation de nouveaux matériaux dans les chimiocapteurs électrochimiques peut améliorer leurs performances et aider à élucider leur mécanisme de détection. Dans notre recherche, le MIP modèle (épitope peptidique) a été dopé avec du MoS2 des flocons d'une taille moyenne de 0,6 à 1,5 µm lors de son dépôt sous forme de film mince sur une électrode ITO. Essentiellement, ce dopage a doublé la réponse électrochimique (au-dessus du bruit de fond) au biomarqueur protéique cible MMP-1."
La macromolécule MMP-1 possède plusieurs peptides situés sur ses bords, appelés épitopes, reconnus par le système immunitaire. Ces épitopes peuvent être utilisés avec succès comme empreinte dans les chimiocapteurs électrochimiques MIP. Puisque l'empreinte protéique ne permettrait pas leur détermination réussie, conduisant à de grandes cavités pouvant accueillir de nombreux composés moléculaires plus petits, les molécules imprimées étaient des épitopes peptidiques, beaucoup plus petits que les protéines.
De plus, en plus de leur plus petite taille, les peptides sont plus stables que les protéines dans des conditions expérimentales, notamment lors de l’utilisation d’un solvant organique lors de la formation d’un film polymère à la surface de l’électrode. Il convient de mentionner que l'utilisation de MoS2 les flocons permettent la détection du biomarqueur MMP-1 et, par conséquent, de la fibrose pulmonaire idiopathique.
"Le MoS2 Les performances des électrodes enrobées de film pAIPs dopées sont comparables à celles de la littérature récente. Enfin, l'électrode a été utilisée pour déterminer la MMP-1 dans les milieux de culture de cellules HEK293T génétiquement modifiées et, comparée à un test ELISA commercial, sa précision était élevée", remarque le professeur Włodzimierz Kutner.
Cette recherche, détaillée dans ACS Applied Nano Materials , est prometteur pour surveiller le développement de maladies chroniques et évolutives d'étiologie et de pathogenèse inconnues, y compris la fibrose pulmonaire idiopathique.
Il est encore possible de tester la détection dans des conditions perturbatrices, mais nous espérons que l’empreinte moléculaire dans les polymères attirera davantage d’attention et d’applications en biomédecine, rapprochant ainsi la société d’un diagnostic rapide et précis de nombreuses maladies difficiles. Les chercheurs espèrent que leur concept éprouvé de chimiocapteur électrochimique à empreinte moléculaire pourra également être adapté à d'autres maladies et à la médecine personnalisée.
Plus d'informations : Mei-Hwa Lee et al, MoS2 Électrodes revêtues de polymère à empreinte peptidique dopée à des nanofeuilles pour la détermination électrochimique de l'expression de protéines activées par CRISPR/dCas9, Nanomatériaux appliqués par ACS (2023). DOI :10.1021/acsanm.3c04130
Fourni par l'Académie polonaise des sciences