Le glycérol, sous-produit majeur du raffinage de la biomasse représentant environ 10 % du rendement, présente un défi important en raison de son excédent mondial. La présence de plusieurs groupes hydroxyles actifs dans le glycérol révèle un vaste potentiel pour la production de produits chimiques de grande valeur. L'acide formique (AF), un produit clé de la conversion du glycérol, est une matière première chimique organique essentielle très demandée dans des secteurs tels que les pesticides, les produits pharmaceutiques et l'énergie.
L'oxydation du glycérol en FA atténue non seulement les déchets causés par l'excédent de ressources, mais répond également aux besoins futurs des piles à combustible FA. Actuellement, la production industrielle de FA repose principalement sur du méthanol dérivé du pétrole et du gaz naturel, ce qui rend la conversion électrocatalytique du glycérol issu de la biomasse en FA très prometteuse.
Cependant, la réaction d'oxydation électrocatalytique du glycérol (RGOR) est complexe, impliquant une déshydrogénation, une adsorption/désorption et une rupture des liaisons C-C des intermédiaires de réaction, ce qui pose des défis pour l'efficacité et la sélectivité de la réaction.
Récemment, une équipe de recherche dirigée par le professeur Kai Yan de l'Université Sun Yat-sen, en Chine, utilisant une combinaison de calculs de théorie fonctionnelle de la densité (DFT) et de méthodes expérimentales, a dévoilé le rôle crucial de l'espèce active OH* dans le processus EGOR. dans la production de FA. L'analyse DFT, à partir d'une perspective thermodynamique, a étudié le mécanisme de OH* dans le processus EGOR.
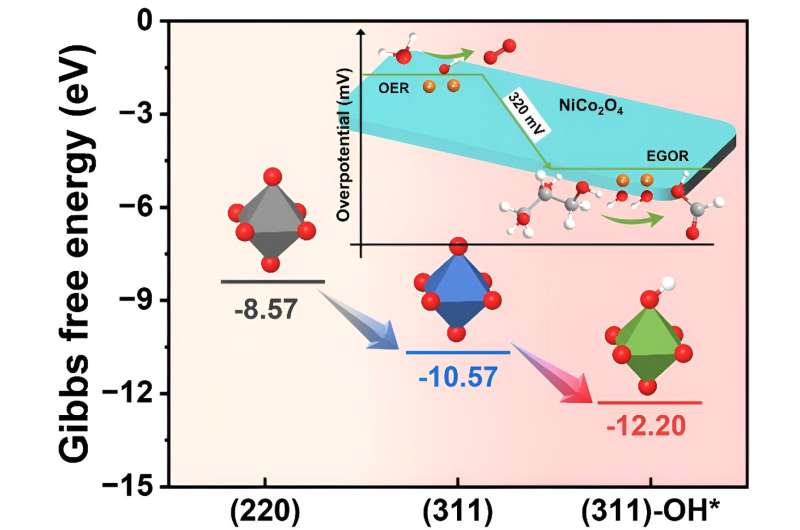
Il a été constaté que les espèces OH* de surface, en réduisant l'énergie d'adsorption du glycérol sur le NiCo2 O4 surface du catalyseur (de -12,20 à -10,57 eV), a facilité le processus EGOR et optimisé l'étape de détermination de la vitesse (RDS) en modifiant l'énergie d'adsorption des intermédiaires, passant de la déshydrogénation moins efficace de l'acide glycérique à l'étape de déshydrogénation plus efficace de glycéraldéhyde.
De plus, l'énergie d'adsorption de OH* au cours du processus EGOR était significativement inférieure à celle du processus de réaction de dégagement d'oxygène (OER) (0,66 contre 2,70 eV), indiquant l'apparition préférentielle de l'EGOR par rapport aux REL.
De plus, les performances d'un NiCo2 méticuleusement conçu O4 L’électrode dans EGOR a été étudiée par des méthodes électrochimiques. Dans un électrolyte mixte de 1 mol L -1 KOH et 0,1 mole L -1 glycérol, le potentiel d'apparition de l'électrode est tombé à 1,16 VRHE , surperformant largement les REL. Les expériences avec électrode à disque annulaire rotatif (RRDE) ont également confirmé l'apparition préférentielle d'EGOR, ce qui correspond aux résultats de l'analyse DFT.
Sur la base du mécanisme conventionnel de transfert d'électrons couplé à des protons, deux voies d'oxydation électrochimique possibles (voie d'oxydation directe et voie d'oxydation indirecte) de OH* ont été étudiées en utilisant des méthodes de potentialisation en plusieurs étapes et de résonance électronique simultanée. Les résultats expérimentaux ont démontré que les performances exceptionnelles du NiCo2 O4 L'électrode dans EGOR est étroitement liée à la génération in situ de OH* participant directement à la réaction.
Lors d'un test de stabilité de cycle à long terme de 120 h, le catalyseur a également montré un taux de conversion du glycérol efficace et stable (89 %) et une sélectivité en acide formique (70 %). Ce travail fournit des conseils et des informations précieuses pour la conception et le développement de catalyseurs efficaces et stables pour l’oxydation du glycérol. Les résultats ont été publiés dans le Chinese Journal of Catalysis. .
Plus d'informations : Yan Duan et al, Intégration de la prédiction théorique et de l'électrooxydation expérimentale du glycérol sur NiCo2 O4 nanofeuilles, Journal chinois de catalyse (2024). DOI :10.1016/S1872-2067(23)64585-1
Fourni par l'Académie chinoise des sciences