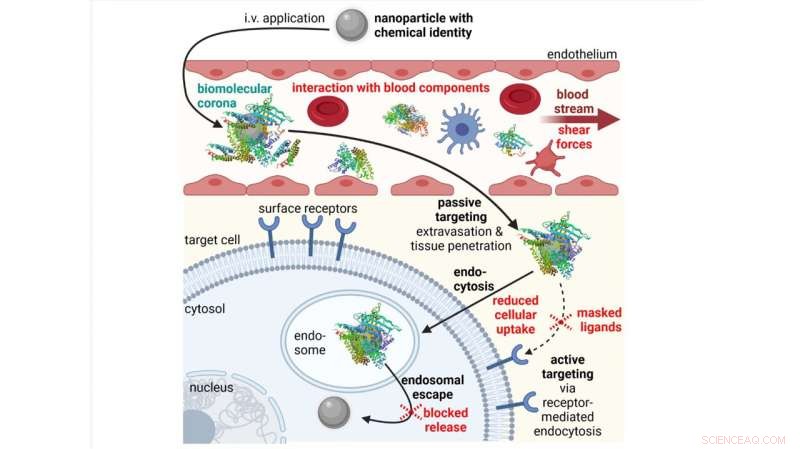
Obstacles (en rouge) dans le processus de délivrance in vivo de nanoparticules appliquées par voie intraveineuse (IV). Crédit :Simone Berger, Martin Berger, Christoph Bantz, Michael Maskos et Ernst Wagner
Les vaccins à ARN messager (ARNm) sont un excellent exemple du domaine prometteur de la nanomédecine. Mais les progrès dans la conception et l'application des nanoparticules en tant que vecteurs de délivrance efficaces pour les produits biopharmaceutiques contenant des acides nucléiques ou des protéines médicamenteuses sont, malheureusement, remarquablement lents.
Un obstacle récent à la recherche sur l'administration de médicaments est une faible corrélation observée entre in vitro (en dehors d'un organisme vivant) et in vivo (à l'intérieur d'un organisme vivant) performance. Ce problème n'était pas clair aux premiers stades, lorsque l'administration cellulaire d'un nanoporteur de médicament a été testée principalement dans une culture cellulaire standard. Avec l'émergence d'études pharmacologiques avancées in vivo sur des souris ou des patients humains, la faible fiabilité et validité des tests de culture cellulaire pour des applications thérapeutiques devient évidente.
Lorsque les nanoparticules sont appliquées par voie intraveineuse, elles se heurtent à plusieurs obstacles qui diffèrent des situations in vitro, comme lorsqu'elles rencontrent des composants sanguins. Les nanoparticules sont généralement recouvertes d'une multicouche biomoléculaire (une couronne protéique), qui modifie les propriétés physiochimiques, la pharmacocinétique et le profil de toxicité des nanoparticules.
Dans Revues de biophysique , des chercheurs allemands fournissent une caractérisation de pointe de la couronne protéique formée autour des nanoparticules et de son impact sur les propriétés physicochimiques et biologiques de ces nanoparticules.
"Lors de la prédiction des performances in vivo à partir de données in vitro, il est recommandé de combiner plusieurs méthodes de caractérisation analytique et biologique pour obtenir un aperçu plus détaillé des caractéristiques et du comportement in vivo des nanoparticules", a déclaré Simone Berger, co-auteur de Ludwig Maximilian. Université de Munich.
Le choix du biofluide (sérum, plasma ou sang total et d'origine animale) et l'établissement de protocoles standardisés sont d'une grande importance pour une préclinique plus cohérente, robuste et complète études pour dériver des relations structure-activité et in vitro/in vivo corrélations.
"Les connaissances acquises sur la formation de couronnes protéiques peuvent être exploitées pour optimiser les supports pour les applications nanomédicales", a déclaré Berger.
Des informations telles que la biodistribution in vivo et les effets hors cible ne peuvent pas être obtenues à partir d'expériences in vitro, soulignent les chercheurs. Mais de nouvelles méthodes de criblage à haut débit comme le système de codes-barres peuvent rendre in vivo enquêtes plus efficaces, économiques et éthiques.
Une certaine incertitude demeure quant à la traduisibilité des petits aux grands animaux et aux humains, mais la bioinformatique pourrait aider à identifier les modèles animaux les mieux adaptés pour certaines maladies.
"Les alternatives aux modèles animaux, telles que la technologie microfluidique" d'organe humain sur puce "ou les prédictions computationnelles, peuvent être des stratégies prometteuses pour remplacer les études animales à l'avenir", a déclaré Berger.
La nanomédecine montre "un grand potentiel pour révolutionner le paysage thérapeutique avec un large éventail d'applications comme les vaccins contre le cancer/l'immunothérapie ou le traitement des troubles génétiques", a déclaré Berger. "Avec des tests in vitro appropriés et plus prédictifs, le pipeline préclinique deviendra plus efficace, plus rapide et plus économique. Et surtout, les expérimentations animales peuvent être remplacées ou au moins réduites." Une méthode pour améliorer les tests in vitro