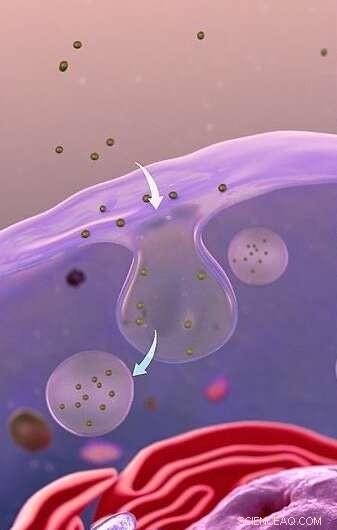
Afin d'entrer dans une cellule, les nanoparticules peuvent être englouties par la membrane entourant la cellule, formant des vésicules en forme de bulles - l'endocytose. Crédit :Adapté de www.scientificanimations.com CC BY-SA 4.0
Nos corps ont développé de formidables barrières pour se protéger contre les substances étrangères - de notre peau à nos cellules et à chaque composant des cellules, chaque partie de notre corps possède des couches protectrices. Ces défenses, bien qu'essentielles, posent un défi important aux médicaments et thérapies pharmaceutiques, tels que les vaccins, qui doivent contourner de multiples barrières pour atteindre leurs cibles.
Bien que ces obstacles soient d'une importance vitale dans la science pharmaceutique et la conception de médicaments, on ignore encore beaucoup de choses à leur sujet et sur la manière de les surmonter.
Dans une étude récente, des chercheurs de l'université Xi'an Jiaotong-Liverpool et de l'université de Nanjing en Chine, ainsi que de l'université Western Washington et Emory aux États-Unis, ont expliqué pourquoi l'administration de thérapies aux cellules peut être si difficile.
Surmonter les barrières
Avec les vaccins COVID-19, auxquels des centaines de millions d'entre nous ont été injectés, l'ARNm doit être enfermé dans des bulles de graisse protectrices - des nanoparticules lipidiques - afin qu'il puisse traverser les défenses de l'organisme et atteindre la cible visée dans nos cellules.
Certains types de cellules, telles que les cellules souches, les cellules immunitaires et les cellules nerveuses, ont des barrières particulièrement difficiles à surmonter, de sorte que la livraison de particules dans ces cellules est encore plus difficile.
Dans l'étude, publiée dans la revue ACS Nano , les chercheurs ont combiné des techniques de microscopie de pointe pour suivre en temps réel l'apport de nanoparticules, souvent utilisées pour l'administration de médicaments, dans les cellules souches.
Leurs découvertes suggèrent que, dans certains types de cellules, les nanoparticules sont « piégées » dans des vésicules en forme de bulles et sont ainsi empêchées d'atteindre leur cible.
L'équipe a utilisé leurs découvertes pour créer un modèle mathématique capable de prédire l'efficacité de l'apport de nanoparticules dans les cellules et d'aider à la conception de futures thérapies.
Le Dr Gang Ruan, auteur correspondant de l'étude, déclare :« Nous avons décomposé le processus de livraison des particules dans les cellules en étapes individuelles, afin que nous puissions visualiser chaque étape et créer une fenêtre sur les mécanismes utilisés par ces cellules pour se protéger. .
"Pour concevoir des méthodes d'administration améliorées pour les thérapies, nous avons besoin d'une compréhension quantitative de la façon dont les parties de la cellule et les nanoparticules interagissent. Comme l'a dit un grand bio-ingénieur que je connaissais, si vous deviez concevoir un avion, vous devriez analyser l'aérodynamique de chaque pièce avant de construire l'avion.
"En trouvant le goulot d'étranglement dans la livraison de nanoparticules dans les cellules, nos découvertes ouvriront la voie à des thérapies plus ciblées et innovantes qui utilisent une livraison sur mesure, potentiellement pour des patients individuels."
En livraison
Auparavant, l'imagerie de la livraison de nanoparticules dans les cellules était limitée en raison de la vitesse rapide requise et de la petite échelle. Cependant, l'équipe multidisciplinaire a pu utiliser ses différents domaines d'expertise pour créer des moyens innovants de surmonter ces obstacles. Ils ont combiné deux types d'analyses par microscopie, auparavant utilisées séparément, pour leur permettre d'étudier l'ensemble du processus de livraison.
Xuan Yang, qui partage la paternité principale de l'étude avec le Dr Xiaowei Wen, déclare :« Nous avons pu suivre le mouvement des nanoparticules pixel par pixel, en temps réel, et donc visualiser le mouvement des nanoparticules à travers barrières membranaires et à leur entrée dans chaque compartiment des cellules souches. »
Bien que le processus de livraison des nanoparticules dans ces cellules soit complexe et composé de plusieurs mécanismes, en visualisant puis en modifiant chimiquement chaque étape du processus, l'équipe a identifié l'étape critique qui empêche la livraison des nanoparticules à leurs cibles cellulaires.
Afin de pénétrer dans une cellule, les nanoparticules peuvent être englouties par la membrane entourant la cellule, formant des vésicules en forme de bulles. Dans de nombreux types de cellules, les nanoparticules s'échapperaient de ces bulles une fois à l'intérieur de la cellule. Cependant, dans certaines cellules extra-protégées, telles que les cellules souches utilisées dans cette étude, les nanoparticules semblent être piégées à l'intérieur des vésicules et sont incapables de s'échapper. Cela signifie qu'ils ne peuvent pas entrer dans la cellule et atteindre leur cible.
Les chercheurs combinent leurs observations et leurs analyses dans un modèle mathématique qui peut prédire l'efficacité et la rapidité avec lesquelles les particules passeraient par chaque étape de livraison et entreraient dans une cellule.
"Notre modèle peut être utilisé pour prédire quelle sera la concentration des nanoparticules, à un endroit particulier de la cellule, à un moment donné", explique le Dr Wen.
« La méthode générale de ce modèle peut être utilisée pour incorporer différents types de nanoparticules et de cellules afin de mieux comprendre les mécanismes de délivrance utilisés pour passer dans les cellules. Par exemple, prédire dans quelle mesure les nanoparticules lipidiques dans les vaccins COVID-19 délivreront l'ARNm dans une cellule ."
Le Dr Steven Emory, qui est également un auteur correspondant de l'étude, ajoute :"Être capable de cartographier les différents composants et fonctionnements internes qui composent les voies de livraison en temps réel permet de comprendre comment contrôler ces voies. Cela pourrait ouvrent des choses vraiment passionnantes en termes de thérapeutique.
"Nous espérons que nos nouveaux outils et notre nouvelle compréhension ont créé une base initiale pour le système, à partir de laquelle nous, et d'autres chercheurs, pouvons commencer à grimper et à explorer." Les coquilles du virus de la grippe pourraient améliorer la livraison de l'ARNm dans les cellules