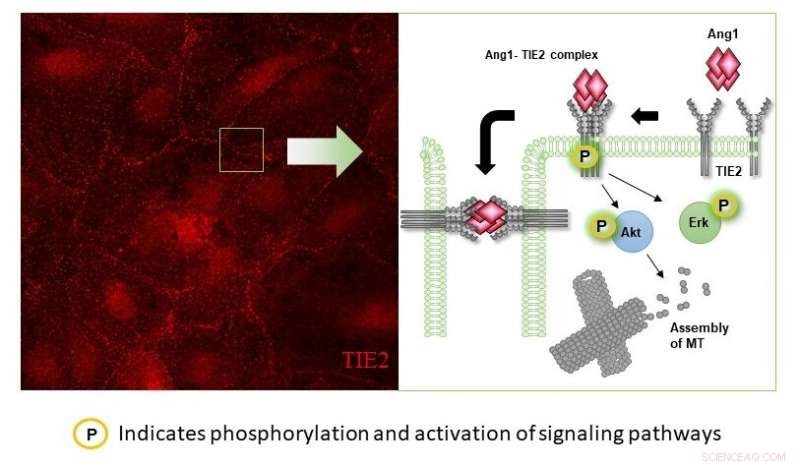
Mécanisme proposé de l'effet anti-perméabilité induit par l'angiopoéitine-1 (Ang-1) dans les cellules endothéliales microvasculaires humaines. L'image de gauche montre les cellules des vaisseaux sanguins qui sont colorées pour identifier l'emplacement de la protéine TIE2. Lorsque l'activateur Angiopoeitin-1 (Ang-1) est appliqué, Les TIE2 sont localisés près de la surface cellulaire où Ang1-Tie2 forme un pont qui maintient les cellules ensemble. Dans des expériences ultérieures, il est démontré que la liaison à Ang1 pourrait intervenir dans les changements cellulaires en augmentant la phosphorylation d'Akt ou d'Erk, ce qui aide ensuite à stabiliser les microtubules pour maintenir la structure cellulaire. Crédit :Université nationale de Singapour
Les scientifiques du NUS ont découvert un mécanisme de contrôle qui régule le trafic des cellules et des substances à travers les vaisseaux sanguins. Cet effet peut avoir un impact significatif sur les métastases cancéreuses.
Les nanoparticules sont utilisées dans diverses applications biomédicales, y compris le diagnostic et le traitement du cancer. Les nanoparticules libérant des médicaments pourraient être programmées pour délivrer des médicaments localement au site de la tumeur. Cependant, des études récentes ont montré que ces nanoparticules peuvent conduire à la formation de lacunes micrométriques dans les parois des vaisseaux sanguins, ce qui les rend "fuites". Chez les patients cancéreux, ces lacunes pourraient permettre aux cellules cancéreuses survivantes de s'échapper plus facilement de leurs sites primaires vers d'autres parties du corps.
Une équipe de recherche composée du Pr HO Han Kiat du Département de Pharmacie, NUS et le professeur David LEONG du Département de génie chimique et biomoléculaire, NUS a découvert que l'angiopoéitine-1 (un type de protéine) peut aider à combler les lacunes dans les vaisseaux sanguins causées par les nanoparticules et à réduire leur perméabilité. Cette, à son tour, contrôle le passage des substances et des molécules à travers les parois des vaisseaux sanguins. En ajustant la quantité d'angiopoéitine-1 dans le corps, les chercheurs ont découvert qu'ils peuvent limiter et inverser la « fuite » induite dans les vaisseaux sanguins causée par les nanoparticules dans les applications biomédicales.
Dans leurs expériences, l'équipe de recherche a administré des cellules cancéreuses du sein sous la peau de modèles murins, puis a introduit des nanoparticules de dioxyde de titane dans leurs vaisseaux sanguins. Ils ont établi que les nanoparticules augmentaient la fuite de cellules cancéreuses dans les vaisseaux sanguins. Cet effet de fuite peut améliorer le mouvement des cellules cancéreuses circulantes vers des tissus distants, ce qui peut entraîner la formation de nouveaux sites cancéreux secondaires auparavant inaccessibles aux cellules cancéreuses.
Suite à cela, l'équipe a découvert que l'angiopoeitine-1 agit comme un facteur de croissance pour TIE2, un régulateur de surface cellulaire naturellement présent dans nos vaisseaux sanguins. Quand il n'y a plus d'angiopoeitine-1, La protéine TIE2 est localisée et stimulée pour combler les lacunes dans les vaisseaux sanguins qui pourraient être causées par les nanoparticules. Cela réduit à son tour la perméabilité des vaisseaux sanguins et limite la quantité de cellules cancéreuses s'infiltrant dans la circulation sanguine.
Le professeur Ho a dit, "L'étude a montré que l'angiopoeitine-1 pourrait potentiellement être utilisée comme un contre-mécanisme pour limiter et inverser les fuites induites par les nanoparticules. Cela aide à diminuer l'extravasation et le transport des cellules cancéreuses vers d'autres tissus chez les patients cancéreux."