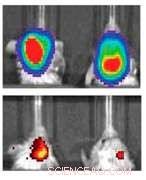
La rangée du haut indique les souris avec un glioblastome contrôlé pour la taille de la tumeur. La rangée du bas montre leur expression de MGMT, une protéine qui rend les cellules tumorales plus résistantes à la chimiothérapie. La gauche est un contrôle, tandis que la droite montre des niveaux significativement diminués de MGMT après traitement avec les nanoparticules. Crédit :Université Northwestern
Les scientifiques de Northwestern Medicine ont développé une nouvelle plate-forme de test pour évaluer, en temps réel, l'efficacité des nanomatériaux dans la régulation de l'expression des gènes. Les résultats, Publié dans Actes de l'Académie nationale des sciences , pourrait aider à faciliter les investigations précliniques et à optimiser les nanothérapies pour les cancers avant qu'elles n'atteignent les essais cliniques.
Timothée Sita, un étudiant de septième année MD/PhD dans le programme de formation des scientifiques médicaux, était le premier auteur de l'étude, qui a examiné la plate-forme dans des modèles animaux.
"C'est une avancée importante pour le domaine, " a déclaré le chercheur principal Alexander Stegh, Doctorat, professeur adjoint de neurologie et de médecine. "L'optimisation très poussée que nous voyons dans le développement de médicaments conventionnels manquait dans l'espace nanotechnologique, et nous avions très envie de changer cela. Le système que nous avons développé ici nous permet vraiment de soutenir ces efforts, et évaluer nos nanoparticules dans les modèles les plus pertinents, dans un environnement in vivo."
Tchad Mirkin, Doctorat, le professeur de chimie George B. Rathmann au Weinberg College of Arts and Sciences et professeur de médecine à la division d'hématologie/oncologie, était également un auteur correspondant de l'article.
Les scientifiques ont démontré le concept en utilisant des nanostructures appelées acides nucléiques sphériques (SNA) pour cibler un gène de facteur de résistance dans le glioblastome, un agressif, type de tumeur cérébrale incurable.
SNA, développé pour la première fois par Mirkin à Northwestern en 1996, se composent de brins denses d'ARN emballés autour d'un noyau de nanoparticules. En raison de leurs propriétés uniques, Les SNA sont capables à la fois de traverser la barrière hémato-encéphalique et d'entrer dans les cellules tumorales, où ils peuvent cibler directement l'activité des gènes qui encourage la croissance du cancer.
Bien que ces conjugués soient un outil prometteur à l'ère de la médecine de précision, les scientifiques manquaient auparavant de méthode quantitative pour évaluer comment les SNA régulaient l'activité des gènes dans les organismes vivants, qui fournirait de nouvelles perspectives sur la façon d'optimiser les thérapies.
"Nous avons vu que ces particules peuvent essentiellement cibler n'importe quel gène du cancer, mais nous ne savions pas quand ils fonctionnaient le mieux ou quels schémas posologiques utiliser, " dit Sita. " En tant que tel, les essais précliniques n'ont pas été aussi réussis qu'ils auraient pu l'être. »
Dans l'étude actuelle, les scientifiques ont montré qu'en utilisant un type d'imagerie non invasive sur les souris, ils pourraient évaluer en temps réel comment les nanoparticules affectaient les niveaux d'une protéine cible intratumorale.
« Maintenant, nous pouvons modifier ces particules – jouer avec la forme de la nanoparticule, ou combien d'ARN nous chargeons sur la particule, par exemple, puis évaluer très rapidement si ces changements sont plus efficaces ou non, " a expliqué Sita. " C'est une plate-forme pour aider à optimiser les médicaments chez la souris avant qu'ils ne soient testés sur l'homme, et faire quelque chose qui se traduira mieux à la clinique."
Bien que la méthode puisse être généralisée à l'étude des nanothérapies pour de nombreux types de cancers, l'étude a également des implications cliniques propres au glioblastome.
Les scientifiques ont développé des nanoparticules pour abattre l'O6-méthylguanine-ADN méthyltransférase (MGMT) - une protéine qui réduit l'impact de la chimiothérapie - chez les souris atteintes de glioblastome. Grâce à la plateforme d'imagerie, ils ont découvert que les souris avaient les niveaux les plus bas de la protéine entre 24 et 48 heures après avoir reçu les nanoparticules, suggérant le moment optimal pour administrer la chimiothérapie.
"Nous avons montré une réduction très significative du volume tumoral lorsque nous avons combiné ces particules avec la chimiothérapie, " a déclaré Sita. "En faisant taire ce gène qui provoque la résistance à la chimiothérapie, nous pouvons avoir une réponse beaucoup plus profonde. C'est l'angle clinique clé."