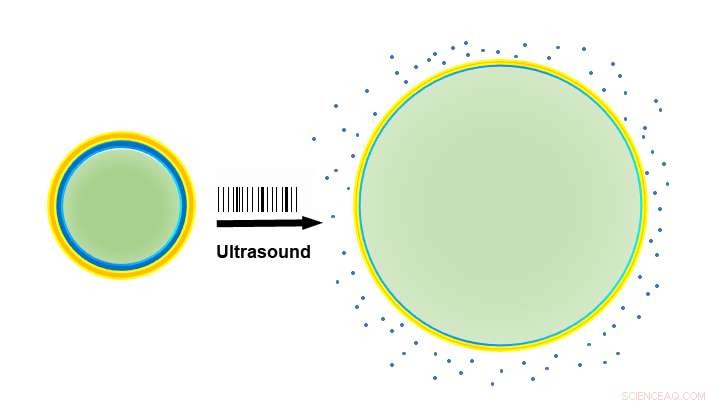
Lorsque les nanoparticules chargées de drogue (à gauche) absorbent l'énergie des ondes ultrasonores, leur centre liquide (vert) se transforme en gaz et dilate les particules (à droite), desserrant leur extérieur et libérant le médicament (bleu). Crédit :Raag Airan
Les ingénieurs biomédicaux de Johns Hopkins rapportent qu'ils ont mis au point un moyen non invasif de libérer et d'administrer des quantités concentrées d'un médicament au cerveau de rats de manière temporaire, manière localisée à l'aide d'ultrasons. La méthode « enferme » d'abord un médicament à l'intérieur de minuscules, « nanoparticules biodégradables, " active ensuite sa libération par des ondes sonores précisément ciblées, tels que ceux utilisés pour créer sans douleur et de manière non invasive des images d'organes internes.
Parce que la plupart des drogues psychoactives pourraient être délivrées de cette façon, ainsi que de nombreux autres types de médicaments, les chercheurs affirment que leur méthode a le potentiel de faire progresser de nombreuses thérapies et études de recherche à l'intérieur et à l'extérieur du cerveau.
Ils disent également que leur méthode devrait minimiser les effets secondaires d'un médicament car la libération du médicament est concentrée dans une petite zone du corps, la quantité totale de médicament administrée peut donc être beaucoup plus faible. Et parce que les composants individuels de la technologie, y compris l'utilisation de biomatériaux spécifiques, les ultrasons et les médicaments approuvés par la FDA - ont déjà été testés sur des personnes et se sont avérés sûrs, les chercheurs pensent que leur méthode pourrait être utilisée en clinique plus rapidement que d'habitude :ils espèrent lancer le processus d'approbation réglementaire d'ici un an ou deux.
"Si d'autres tests de notre méthode combinée fonctionnent chez l'homme, cela nous donnera non seulement un moyen de diriger les médicaments vers des zones spécifiques du cerveau, mais nous permettra également d'en apprendre beaucoup plus sur la fonction de chaque zone du cerveau, " dit Jordan Green, Doctorat., professeur agrégé de génie biomédical, qui est également membre du Kimmel Cancer Center et de l'Institute for Nanobiotechnology.
Les détails de la recherche sont publiés le 23 janvier dans la revue Lettres nano .
La nouvelle recherche, Vert dit, a été conçu pour faire progresser les moyens d'acheminer les médicaments au cerveau en toute sécurité, un organe délicat et difficile à traiter. Pour se protéger des agents infectieux et des gonflements pouvant être causés par le système immunitaire, par exemple, le cerveau est entouré d'une barrière moléculaire, appelée barrière hémato-encéphalique (BHE), qui tapisse la surface de chaque vaisseau sanguin alimentant le cerveau. Seules de très petites molécules médicamenteuses qui se dissolvent dans l'huile peuvent traverser la clôture, avec les gaz. À cause de ce, la plupart des médicaments développés pour traiter les troubles cérébraux répondent à ces critères mais sont dispersés dans toutes les parties du cerveau et dans le reste du corps, où ils peuvent être inutiles et indésirables.
Raag Airan, MARYLAND., Doctorat., professeur adjoint de radiologie au Stanford University Medical Center et co-auteur de l'article, dit : « Lorsque vous travaillez avec un patient qui souffre d'un trouble de stress post-traumatique, par exemple, ce serait bien de calmer la partie hyperactive du cerveau, par exemple, l'amygdale - pendant les séances de thérapie par la parole. Les technologies actuelles peuvent au mieux calmer la moitié du cerveau à la fois, ils sont donc trop non spécifiques pour être utiles dans ce contexte. »
Dans la nouvelle étude, les chercheurs se sont inspirés de l'utilisation antérieure de nanoparticules et d'ultrasons pour administrer des médicaments chimiothérapeutiques aux tumeurs sous la peau. Dans leurs dernières expériences, Le groupe de Green a conçu des nanoparticules avec une "cage" externe extensible en plastique biodégradable, dont les éléments constitutifs moléculaires aiment le pétrole d'un côté et l'eau de l'autre. Les extrémités qui aiment l'huile s'accrochent et forment une sphère extensible avec les extrémités qui aiment l'eau à l'extérieur. Les extrémités qui aiment l'huile lient le médicament à délivrer, qui dans ce cas était le propofol, un anesthésique couramment utilisé pour traiter les crises chez les personnes.
Le centre de la cage était rempli de perfluoropentane liquide. Lorsque les ondes sonores des ultrasons, délivrées de manière non invasive sur le cuir chevelu et le crâne avec des appareils approuvés par la FDA, frappent le perfluoropentane au centre des nanoparticules, le liquide se transforme en gaz, en agrandissant la cage environnante et en laissant le propofol s'échapper.
Avant de tester leur idée sur des animaux, Green et ses collègues ont affiné leur protocole d'échographie en testant des nanoparticules dans des tubes en plastique, chercher à localiser des impulsions de la bonne puissance et de la bonne fréquence pour libérer des quantités adéquates de médicament sans être assez fortes pour endommager la BHE, un effet connu des ultrasons de haute puissance.
Ils ont également testé la distribution des nanoparticules chez le rat en ajoutant un colorant fluorescent aux particules et en mesurant la quantité de colorant trouvée dans les échantillons de sang et d'organes au fil du temps. La majorité des particules se sont retrouvées dans la rate et le foie, qui sont des organes d'entretien importants dans le corps. Comme prévu, les particules n'ont pas été trouvées dans le cerveau car elles sont trop grosses pour traverser la BHE. Au lieu, les chercheurs s'appuyaient sur la propre capacité du propofol à traverser la BHE une fois libérée localement à partir des nanoparticules.
Pour voir si leur méthode pouvait apporter un soulagement médical aux animaux vivants, ils ont ensuite donné aux rats un médicament qui provoque des convulsions, puis les nanoparticules chargées de propofol. Ils ont utilisé l'IRM pour guider leur application des ultrasons au cerveau de rat et ainsi libérer le médicament des nanoparticules flottant à travers les vaisseaux sanguins infiltrés. Dès qu'ils ont appliqué les ultrasons, l'activité convulsive des rats s'est calmée.
"Ces expériences montrent l'efficacité de cette méthode pour manipuler la fonction des cellules cérébrales grâce à l'administration précise de médicaments, " dit Green. " Chez l'homme, les machines à ultrasons peuvent cibler un volume aussi petit que quelques millimètres cubes, moins d'un dix millième du cerveau."
Airane, qui faisait sa bourse et sa résidence à l'hôpital Johns Hopkins pendant l'étude, dit que l'un des plus prometteurs, les applications immédiates de la nouvelle technologie pourraient concerner la « cartographie du cerveau » requise avant de nombreuses neurochirurgies. Avant qu'un chirurgien ne coupe le cerveau pour enlever une tumeur, par exemple, il ou elle doit savoir où ne pas couper. "Actuellement, qui nécessite de garder le patient éveillé, tandis que le chirurgien expose le cerveau et le sonde avec des électrodes tout en évaluant les réponses. La méthode par ultrasons nous permettrait d'utiliser un médicament comme le propofol pour brièvement « désactiver » des zones spécifiques du cerveau, une par une, avant la chirurgie, avec rien de plus invasif qu'une piqûre d'aiguille, " il dit.
Parce que l'échographie, L'IRM et chaque composant des nanoparticules ont été approuvés pour d'autres utilisations chez l'homme, les chercheurs s'attendent à un délai court pour transmettre leur idée aux patients, mais ils reconnaissent que ses applications seront quelque peu limitées par le coût et l'accessibilité des examens IRM, du moins à court terme.
"Notre modèle actuel nécessite une imagerie en temps réel du cerveau pendant que l'échographie est appliquée, " dit Airan. " Sur la base de procédures similaires que je fais déjà, qui peut coûter jusqu'à 30 $, 000 à 50 $, 000. Mais nous travaillons sur un logiciel qui nous permettrait de synchroniser une seule image IRM avec le système de guidage par ultrasons pour réduire considérablement le coût. "
Pendant ce temps, les chercheurs pensent qu'il sera toujours cliniquement pertinent dans de nombreuses situations où les effets d'un médicament sont connus pour durer des semaines. Ils s'attendent également à ce qu'il soit largement utilisé dans la recherche sur le cerveau pour étudier et manipuler la fonction de zones spécifiques du cerveau de manière contrôlée.