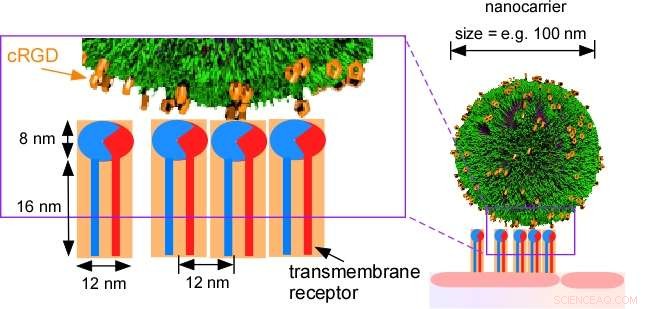
Les nanocapsules (cRGD-PICsomes) se lient à des récepteurs membranaires qui jouent un rôle important dans la formation de nouveaux vaisseaux sanguins dans les tumeurs, ce qui en fait un bon traceur de tumeur.
Des chercheurs japonais ont développé des nanocapsules adaptables qui peuvent aider au diagnostic des cellules de glioblastome, une forme hautement invasive de tumeur cérébrale.
Les polymères sont creux, synthétique, capsules de taille nanométrique. Ils ont été largement étudiés pour leur potentiel dans l'administration ciblée de médicaments dans le corps. Les PICsomes sont une nouvelle classe de polymersomes récemment développée au Japon. Ils sont fabriqués en mélangeant des groupes électrolytiques formés d'ions chargés positivement et négativement. Les PICsomes peuvent survivre dans la circulation sanguine pendant de longues périodes et peuvent être utilisés pour administrer des substances hydrosolubles aux tissus cibles.
Une étude publiée dans Science et technologie des matériaux avancés ( STAM ) rapporte que les PICsomes peuvent être adaptés pour durer plus longtemps dans la circulation sanguine et pour mieux cibler des sites spécifiques dans les tumeurs. Ces PICsomes « fonctionnalisés » ont un grand potentiel d'utilisation à la fois dans l'administration de médicaments et dans l'imagerie par résonance magnétique des tumeurs.
Le RGD cyclique (cRGD) – un peptide ou une chaîne courte d'acides aminés – est connu pour se lier spécifiquement à deux récepteurs qui jouent un rôle important dans la formation de nouveaux vaisseaux sanguins dans les tumeurs. Cela en fait un bon traceur de tumeur. Dans l'étude STAM, Des chercheurs japonais ont lié cRGD aux PICsomes. Les cRGD-PICsomes ont ensuite été injectés par voie intraveineuse à des souris inoculées – sous la peau – avec des cellules de glioblastome humain, une tumeur cérébrale très invasive. L'équipe de recherche a découvert que les cRGD-PICsomes s'accumulaient principalement dans les nouveaux vaisseaux sanguins de la tumeur et qu'ils restaient près de ces vaisseaux sanguins 24 heures plus tard.
Les chercheurs ont ensuite chargé des cRGD-PICsomes avec de l'oxyde de fer superparamagnétique (SPIO), qui est utilisé pour améliorer la visibilité des structures internes du corps en imagerie par résonance magnétique. En outre, des cellules de glioblastome ont été injectées dans le cerveau de souris et laissées croître pendant plus de deux semaines. Les cRGD-PICsomes chargés en SPIO ont ensuite été injectés par voie intraveineuse aux souris. Grâce à l'imagerie magnétique, l'équipe a réussi à suivre les PICsomes chargés dans les nouveaux vaisseaux sanguins qui se sont formés autour des glioblastomes.
Des recherches antérieures ont montré que l'imagerie magnétique peut détecter des PICsomes chargés de SPIO qui ne sont pas liés au cRGD dans les tumeurs riches en vasculaires telles que les tumeurs du côlon. Mais ils ne sont pas toujours détectables dans les glioblastomes :tumeurs cérébrales fortement protégées par la barrière hémato-encéphalique, qui empêche à la fois les substances toxiques et les médicaments d'atteindre le cerveau.
Les résultats de l'étude suggèrent que les cRGD-PICsomes chargés de SPIO pourraient être utiles pour améliorer le contraste lors de l'imagerie par résonance magnétique dans les microenvironnements tumoraux, y compris dans les nouveaux vaisseaux sanguins qui surexpriment les récepteurs transmembranaires sensibles au cRGD.
Parce que la formation de vaisseaux sanguins est intimement liée à la malignité tumorale, L'imagerie par résonance magnétique utilisant des PICsomes adaptés aux vaisseaux sanguins tumoraux cibles pourrait être un outil prometteur pour le diagnostic précis des tumeurs malignes.