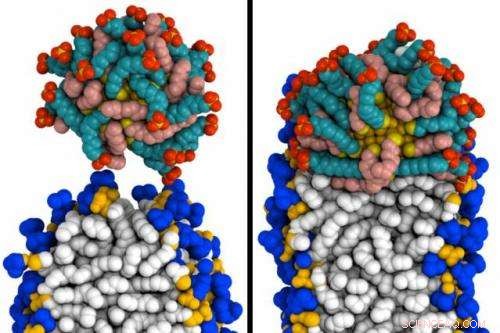
Les ingénieurs du MIT ont créé des simulations de la façon dont une nanoparticule d'or recouverte de molécules spéciales peut pénétrer dans une membrane. A gauche, la particule (en haut) entre en contact avec la membrane. A droite, il a fusionné avec la membrane. Crédit :Reid Van Lehn
Une classe spéciale de minuscules particules d'or peut facilement glisser à travers les membranes cellulaires, ce qui en fait de bons candidats pour délivrer des médicaments directement aux cellules cibles.
Une nouvelle étude des scientifiques des matériaux du MIT révèle que ces nanoparticules pénètrent dans les cellules en profitant d'une voie normalement utilisée dans la fusion vésicule-vésicule, un processus crucial qui permet la transmission du signal entre les neurones. Dans le numéro du 21 juillet de Communication Nature , les chercheurs décrivent en détail le mécanisme par lequel ces nanoparticules sont capables de fusionner avec une membrane.
Les résultats suggèrent des stratégies possibles pour la conception de nanoparticules, fabriquées à partir d'or ou d'autres matériaux, qui pourraient pénétrer encore plus facilement dans les cellules.
"Nous avons identifié un type de mécanisme qui pourrait être plus répandu qu'on ne le sait actuellement, " dit Reid Van Lehn, un étudiant diplômé du MIT en science et ingénierie des matériaux et l'un des principaux auteurs de l'article. « En identifiant cette voie pour la première fois, cela suggère également non seulement comment concevoir cette classe particulière de nanoparticules, mais que cette voie pourrait également être active dans d'autres systèmes."
L'autre auteur principal de l'article est Maria Ricci de l'École Polytechnique Fédérale de Lausanne (EPFL) en Suisse. L'équipe de recherche, dirigé par Alfredo Alexander-Katz, professeur agrégé de science et génie des matériaux, et Francesco Stellacci de l'EPFL, comprenait également des scientifiques de l'Institut de neurologie Carlos Besta en Italie et de l'Université de Durham au Royaume-Uni.
La plupart des nanoparticules pénètrent dans les cellules par endocytose, un processus qui piège les particules dans des compartiments intracellulaires, ce qui peut endommager la membrane cellulaire et provoquer une fuite du contenu cellulaire. Cependant, En 2008, Stellaci, qui était alors au MIT, et Darrell Irvine, professeur de science et génie des matériaux et de génie biologique, ont découvert qu'une classe spéciale de nanoparticules d'or recouvertes d'un mélange de molécules pouvait pénétrer dans les cellules sans aucune perturbation.
"Pourquoi cela arrivait-il, ou comment cela se passait, était un mystère complet, ", dit Van Lehn.
L'année dernière, Alexandre-Katz, Van Lehn, Stellaci, et d'autres ont découvert que les particules fusionnaient d'une manière ou d'une autre avec les membranes cellulaires et étaient absorbées dans les cellules. Dans leur nouvelle étude, ils ont créé des simulations atomistiques détaillées pour modéliser comment cela se produit, et réalisé des expériences qui ont confirmé les prédictions du modèle.
Entrée furtive
Les nanoparticules d'or utilisées pour l'administration de médicaments sont généralement recouvertes d'une fine couche de molécules qui aident à ajuster leurs propriétés chimiques. Certaines de ces molécules, ou des ligands, sont chargés négativement et hydrophiles, tandis que le reste est hydrophobe. Les chercheurs ont découvert que la capacité des particules à pénétrer dans les cellules dépend des interactions entre les ligands hydrophobes et les lipides présents dans la membrane cellulaire.
Les membranes cellulaires sont constituées d'une double couche de molécules de phospholipides, qui ont des queues lipidiques hydrophobes et des têtes hydrophiles. Les queues lipidiques se font face, tandis que les têtes hydrophiles sont tournées vers l'extérieur.
Dans leurs simulations informatiques, les chercheurs ont d'abord créé ce qu'ils appellent une "bicouche parfaite, " dans laquelle toutes les queues lipidiques restent en place à l'intérieur de la membrane. Dans ces conditions, les chercheurs ont découvert que les nanoparticules d'or ne pouvaient pas fusionner avec la membrane cellulaire.
Cependant, si la membrane modèle comprend un "défaut" - une ouverture à travers laquelle les queues lipidiques peuvent glisser - les nanoparticules commencent à entrer dans la membrane. Lorsque ces protubérances lipidiques apparaissent, les lipides et les particules s'accrochent les unes aux autres car ils sont tous les deux hydrophobes, et les particules sont englouties par la membrane sans l'endommager.
Dans de vraies membranes cellulaires, ces protubérances se produisent de manière aléatoire, en particulier près des sites où les protéines sont intégrées dans la membrane. Ils se produisent également plus souvent dans les sections courbes de la membrane, car il est plus difficile pour les têtes hydrophiles de couvrir entièrement une zone courbe qu'une zone plate, laissant des espaces pour que les queues lipidiques dépassent.
"C'est un problème d'emballage, " dit Alexander-Katz. " Il y a un espace ouvert où les queues peuvent sortir, et il y aura un contact avec l'eau. Cela rend juste 100 fois plus probable qu'une de ces protubérances sorte dans des régions très incurvées de la membrane."
Imiter la nature
Ce phénomène semble imiter un processus qui se produit naturellement dans les cellules :la fusion des vésicules avec la membrane cellulaire. Les vésicules sont de petites sphères de matériau semblable à une membrane qui transportent des marchandises telles que des neurotransmetteurs ou des hormones.
La similitude entre l'absorption des vésicules et l'entrée des nanoparticules suggère que les cellules où se produit naturellement une grande partie de la fusion des vésicules pourraient être de bonnes cibles pour l'administration de médicaments par les nanoparticules d'or. Les chercheurs prévoient d'analyser plus avant comment la composition des membranes et les protéines qu'elles contiennent influencent le processus d'absorption dans différents types de cellules. "Nous voulons vraiment comprendre toutes les contraintes et déterminer comment nous pouvons concevoir au mieux des nanoparticules pour cibler des types cellulaires particuliers, ou des régions d'une cellule, ", dit Van Lehn.
« On pourrait utiliser les résultats de cet article pour réfléchir à la manière d'exploiter ces résultats dans des véhicules de livraison de nanoparticules améliorés, par exemple, peut-être que de nouveaux ligands de surface pour les nanoparticules pourraient être conçus pour avoir une affinité améliorée à la fois pour les groupes de surface et les queues lipidiques, " dit Catherine Murphy, un professeur de chimie à l'Université de l'Illinois à Urbana-Champaign qui n'a pas participé à l'étude.
Cette histoire est republiée avec l'aimable autorisation de MIT News (web.mit.edu/newsoffice/), un site populaire qui couvre l'actualité de la recherche du MIT, innovation et enseignement.