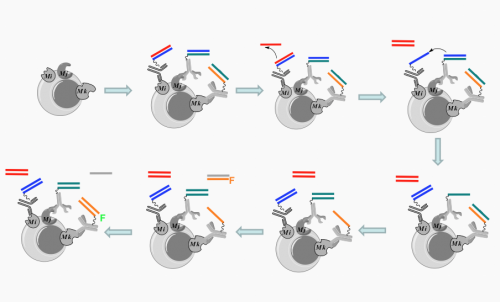
Ce graphique montre un robot moléculaire (automate) en action. Pour marquer les cellules (cercle gris) qui affichent le Mi, Mj, et les récepteurs Mk, cinq composants différents d'un robot moléculaire sont déployés. Chacun des trois premiers composants est constitué d'ADN et d'un anticorps; un anticorps se lie à chaque récepteur, rapprocher son ADN (représenté par les lignes colorées) sur la cellule. Le quatrième composant de l'ADN, représenté par la ligne rouge unique, déclenche ensuite une réaction en chaîne en éloignant le brin d'ADN rouge du premier anticorps. Cela provoque le changement de position du brin d'ADN bleu, suivi du brin d'ADN vert. Dans la dernière étape, le dernier anticorps tire un brin d'ADN fluorescent (marqué F) du cinquième composant, terminer l'action du robot. Crédit :Milan Stojanovic, Ph.D./Centre médical de l'Université Columbia
Des chercheurs du Columbia University Medical Center, travaillant avec leurs collaborateurs à l'Hôpital de Chirurgie Spéciale, ont créé une flotte de « robots » moléculaires qui peuvent se rendre sur des cellules humaines spécifiques et les marquer pour un traitement médicamenteux ou leur destruction.
Les nanorobots, une collection de molécules d'ADN, certains attachés à des anticorps ont été conçus pour rechercher un ensemble spécifique de cellules sanguines humaines et attacher une étiquette fluorescente à la surface des cellules. Les détails du système ont été publiés le 28 juillet 2013, dans l'édition en ligne de Nature Nanotechnologie .
"Cela ouvre la possibilité d'utiliser de telles molécules pour cibler, traiter, ou tuer des cellules spécifiques sans affecter les cellules saines similaires, " a déclaré le chercheur principal de l'étude, Milan Stojanovic, Doctorat, professeur agrégé de médecine et de génie biomédical au Columbia University Medical Center. « Dans notre expérience, nous avons marqué les cellules avec un marqueur fluorescent; mais nous pourrions remplacer cela par un médicament ou par une toxine pour tuer la cellule."
Bien que d'autres nanorobots à ADN aient été conçus pour administrer des médicaments aux cellules, l'avantage de la flotte de Stojanovic est sa capacité à distinguer des populations cellulaires qui ne partagent pas un seul trait distinctif.
Cellules, y compris les cellules cancéreuses, possèdent rarement un seul, caractéristique exclusive qui les distingue de toutes les autres cellules. Cela rend difficile la conception de médicaments sans effets secondaires. Les médicaments peuvent être conçus pour cibler les cellules cancéreuses avec un récepteur spécifique, mais les cellules saines avec le même récepteur seront également ciblées.
La seule façon de cibler les cellules plus précisément est d'identifier les cellules en fonction d'un ensemble de caractéristiques. « Si nous recherchons la présence de cinq, six, ou plusieurs protéines à la surface cellulaire, nous pouvons être plus sélectifs, ", a déclaré le Dr Stojanovic. Les grandes machines de tri cellulaire ont la capacité d'identifier les cellules sur la base de plusieurs protéines, mais jusqu'à maintenant, la thérapeutique moléculaire n'a pas eu cette capacité.
Comment ça fonctionne
Au lieu de construire une seule molécule complexe pour identifier plusieurs caractéristiques d'une surface cellulaire, Le Dr Stojanovic et ses collègues de Columbia ont utilisé une méthode différente, et potentiellement plus facile, approche basée sur de multiples molécules simples, qui forment ensemble un robot (ou automate, comme les auteurs préfèrent l'appeler).
Pour identifier une cellule possédant trois protéines de surface spécifiques, Le Dr Stojanovic a d'abord construit trois composants différents pour les robots moléculaires. Chaque composant consistait en un morceau d'ADN double brin attaché à un anticorps spécifique à l'une des protéines de surface. Lorsque ces composants sont ajoutés à une collection de cellules, les portions d'anticorps du robot se lient à leurs protéines respectives (sur la figure, CD45, CD3, et CD8) et travailler de concert.
Sur les cellules où les trois composants sont attachés, un robot est fonctionnel et un quatrième composant (étiqueté 0 ci-dessous) initie une réaction en chaîne parmi les brins d'ADN. Chaque composant échange un brin d'ADN avec un autre, jusqu'à la fin de l'échange, lorsque le dernier anticorps obtient un brin d'ADN marqué par fluorescence.
A la fin de la réaction en chaîne - qui prend moins de 15 minutes dans un échantillon de sang humain - seules les cellules avec les trois protéines de surface sont marquées avec le marqueur fluorescent.
« Nous avons démontré notre concept avec des cellules sanguines car leurs protéines de surface sont bien connues, mais en principe nos molécules pourraient être déployées n'importe où dans le corps, " a déclaré le Dr Stojanovic. En outre, le système peut être étendu pour en identifier quatre, cinq, ou encore plus de protéines de surface.
Maintenant, les chercheurs doivent montrer que leurs robots moléculaires fonctionnent sur un animal vivant; la prochaine étape sera des expériences sur des souris.