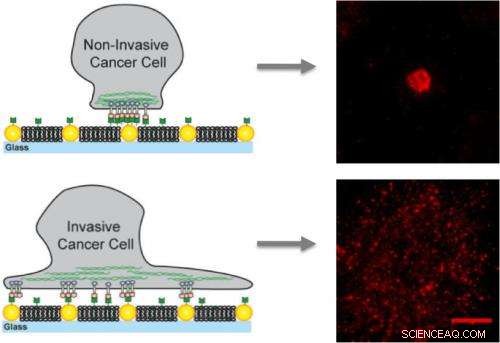
Sur des membranes artificielles incrustées de nanopoints d'or, les cellules cancéreuses non invasives se lient uniquement aux nanopoints et s'immobilisent tandis que les cellules invasives se lient à la membrane ainsi qu'aux nanopoints créant des amas mobiles qui contribuent à la métastase.
(Phys.org) — Les preuves s'accumulent que le développement et la propagation du cancer, longtemps attribué à l'expression génique et à la signalisation chimique qui ont mal tourné, implique également une composante biomécanique. Des chercheurs du Lawrence Berkeley National Laboratory (Berkeley Lab) ont ajouté à cet ensemble de preuves en démontrant que l'activité maligne d'un système protéique cellulaire critique peut provenir de ce qui sont essentiellement des embouteillages de protéines.
Utilisant une membrane artificielle unique imprégnée d'un parcours d'obstacles de nanopoints d'or, une équipe de recherche dirigée par le chimiste Jay Groves a étudié le transport du complexe de signalisation protéique EphA2/éphrine-A1 à travers les surfaces de 10 différentes lignées cellulaires de cancer épithélial du sein présentant un large éventail de caractéristiques de la maladie. Les chercheurs ont découvert que le transport de ce complexe récepteur-ligand était normal dans les lignées cellulaires plus saines, mais s'est bloqué dans les lignées cellulaires malades, le pire brouillage ayant lieu dans les cellules les plus malades.
"Il y a quelque chose sur la force avec laquelle les protéines EphA2 sont regroupées à la surface cellulaire qui est liée et peut même contribuer au comportement malin des cellules cancéreuses, " dit Groves. " Le brouillage différentiel du transport de l'EphA2 entre les différentes lignées cellulaires du cancer du sein et sa corrélation avec les caractéristiques de la maladie suggèrent que le regroupement de l'EphA2 lui-même peut contribuer aux effets pathologiques. "
Groves occupe des postes conjoints avec la division des biosciences physiques de Berkeley Lab et le département de chimie de l'UC Berkeley, et est également chercheur au Howard Hughes Medical Institute (HHMI). Il est l'auteur correspondant d'un article décrivant cette recherche dans la revue Lettres nano intitulé "Les réseaux d'obstacles à l'échelle nanométrique entravent le transport des grappes EphA2/éphrine-A1 dans les lignées cellulaires cancéreuses". Les co-auteurs de cet article étaient Theobald Lohmuller et Qian Xu.
EphA2 appartient à une famille d'enzymes qui sont des régulateurs clés des processus cellulaires. Ephrin-A1 est une protéine de signalisation qui se lie à EphA2. Les complexes d'EphA2/ephrin-A1 se rassembleront en grappes qui seront ensuite transportées à travers la surface cellulaire. La surexpression d'EphA2 a été liée à un certain nombre de cancers humains, mais est particulièrement important dans le cancer du sein.
"Environ 40 % de toutes les patientes atteintes d'un cancer du sein présentent une surexpression d'EphA2 qui est corrélée aux métastases tumorales, par conséquent, beaucoup d'efforts ont été consacrés au développement de thérapies ciblant l'EphA2, " dit Groves. " Cependant, ce qui ne va pas précisément avec EphA2 qui contribue au comportement pathologique des cellules reste incertain car EphA2 n'est généralement pas muté dans les cellules cancéreuses."
Groves est une autorité de premier plan dans le domaine émergent de la mécanobiologie, qui cherche à comprendre comment les cellules ressentent et réagissent aux forces mécaniques. Pour rechercher un éventuel facteur mécanique dans le lien entre EphA2 et le cancer du sein, Groves a utilisé une technique que son groupe a développée dans laquelle des membranes artificielles constituées d'une bicouche fluide de molécules lipidiques sont incrustées de réseaux fixes de nanopoints d'or. Cela permet aux chercheurs de contrôler l'espacement ou le transport des protéines et autres molécules cellulaires placées sur les membranes.
Pour cette étude, Groves et ses collègues ont utilisé des réseaux de nanopoints d'or pour présenter des obstacles définis au mouvement et à l'assemblage des clusters EphA2/ephrin-A1. Les ligands éphrine-A1 pourraient se lier à la membrane, ce qui a permis aux clusters d'être mobiles, ou aux nanopoints, qui a immobilisé les grappes, ou aux deux. Les chercheurs ont travaillé avec des lignées de cellules cancéreuses du sein qui ont des niveaux similaires d'expression d'EphA2 et comprenaient MDA-MB-231, une lignée hautement invasive et tumorigène, et MCF10A, une lignée relativement bénigne et non tumorigène.
"Lorsque nous voyons des cellules qui ont les mêmes niveaux d'EphA2 mais que le MDA-MB-231 est bloqué alors que le MCF10A ne l'est pas, alors nous pouvons dire que c'est quelque chose au-delà des chiffres d'EphA2 qui compte, quelque chose sur la façon dont EphA2 est branché dans le reste de la cellule qui est mal lié, " dit Groves. "Nos observations suggèrent que le cytosquelette est le coupable et que les médicaments modulant le cytosquelette pourraient également moduler thérapeutiquement le clustering EphA2, réduisant ainsi le comportement pathologique.