Des scientifiques de l'Institut Laue-Langevin ont montré que la charge des nanoparticules d'or, identifié par les grandes sociétés pharmaceutiques comme un agent d'administration de médicaments du futur pour le traitement du cancer, affecte la façon dont ils interagissent avec la paroi extérieure protectrice de notre cellule. Ces informations cruciales, Publié dans Langmuir , fournir une première étape dans la conception efficace de nanoparticules sûres pour les applications biomédicales et les pratiques et procédures pour leur manipulation sécurisée dans une variété d'autres produits de consommation.
L'utilisation croissante des nanoparticules, de minuscules flocons de matière, 1 millionième de la taille d'un grain de sable, dans une large gamme de produits commerciaux, comme des vêtements, récipients de stockage de nourriture, médicaments, produits de beauté, pneus, appareils électroniques et optiques, est controversé. Nanoparticules communes, comme l'or, argent et cuivre, pénétrer facilement les membranes organiques, (parois cellulaires, ...) créant des impacts potentiellement importants sur la santé humaine et l'environnement. Cependant, il y a un domaine où leur toxicité pourrait s'avérer utile et même sauver des vies.
Un défi majeur de la médecine moderne est de trouver des agents d'administration capables de cibler et de pénétrer les cellules pour transporter les médicaments directement à l'intérieur du tissu infecté. La recherche du bon véhicule a ouvert un nouveau champ de recherche, « nanomédecine », où les nanoparticules pourraient être programmées pour cibler les cellules cancéreuses par exemple, réduisant ou même éliminant le besoin de chirurgie.
De toutes les nanoparticules disponibles pour la science médicale, un en particulier est devenu un centre de recherche parmi les grandes sociétés pharmaceutiques – l'or. AstraZeneca a annoncé l'année dernière un nouveau projet de recherche pour étudier une nouvelle nanomédecine, CYT-6091, à base de nanoparticules d'or.
Les nanoparticules d'or sont des vecteurs particulièrement efficaces car :
Cependant, à l'heure actuelle, nous ne comprenons pas en détail les mécanismes d'interaction entre les nanoparticules et les défenses externes de notre cellule – la membrane cellulaire. Sans cela, il est impossible de déterminer à quel point ils sont dangereux et si leur capacité à pénétrer et à détruire les cellules peut jamais être exploitée à de bonnes fins, comme dans la lutte contre le cancer.
Une chose que l'on sait, c'est qu'il existe un ensemble complexe de paramètres qui influencent cette interaction, y compris la forme de la nanoparticule, Taille, composition et charge. Mais une étude systématique qui montre comment l'interaction dépend de ces paramètres au niveau moléculaire a jusqu'à présent fait défaut.
Pour commencer à régler ce problème, une équipe de recherche de l'Institut Laue-Langevin (ILL), l'Université de l'Illinois et l'Australian Nuclear Science and Technology Organization ont utilisé les neutrons de l'ILL et des instruments de diffusion de neutrons de renommée mondiale pour enquêter, au niveau moléculaire, les changements physiques subis par nos parois cellulaires lorsqu'elles entrent en contact avec des nanoparticules d'or de charges différentes.
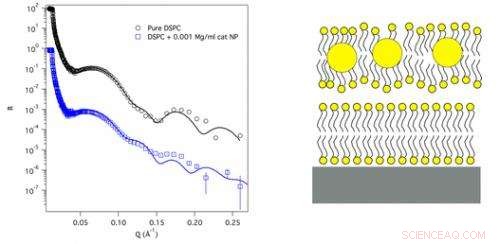
Des nanoparticules d'or de 2 nm de diamètre avaient des groupes cationiques (chargés positivement) ou anioniques (chargés négativement) ajoutés à leur surface. Pour imiter la membrane cellulaire, l'équipe de recherche a utilisé deux doubles couches de molécules de lipides gras maintenues à 20-30 l'une sur l'autre qui, ensemble, ont produit les propriétés dynamiques observées dans les membranes cellulaires. Les scientifiques ont ensuite appliqué des techniques de réflectométrie neutronique à l'ILL pour modéliser avec précision l'interaction nanoparticule - membrane cellulaire à une fraction de l'échelle nanométrique.
Ce qu'ils ont découvert, c'est que la charge de surface des nanoparticules joue en effet un rôle important dans la détermination de leur interaction avec les membranes de nos cellules. Les nanoparticules cationiques traversent directement la membrane lipidique et s'incrustent profondément dans la bicouche flottante, déstabilisant suffisamment la structure membranaire entière pour détruire complètement la cellule à des concentrations plus élevées. En revanche, les nanoparticules anioniques ne pénètrent pas du tout dans la membrane lipidique. Plutôt, à des concentrations données, ils empêchent la décomposition de la membrane en l'aidant à résister à des conditions extrêmes, comme un pH élevé, cela le déstabiliserait normalement de manière significative.