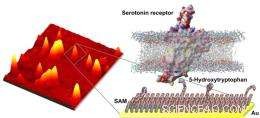
Pêche aux molécules. (À gauche) Image de microscopie à force atomique d'une surface modifiée par un précurseur de sérotonine avec des nanovésicules contenant des récepteurs de sérotonine capturés. (À droite) Illustration des structures moléculaires de la chimie de surface et des différences de taille relative entre l'« appât » (5-hydroxytryptophane) et les récepteurs de la sérotonine associés à la membrane capturés sélectivement par ces surfaces.
(PhysOrg.com) -- La nouvelle technique, dans lequel des molécules sont utilisées comme appât pour capturer et étudier de grosses biomolécules, pourrait conduire à une nouvelle génération de médicaments psychiatriques.
Des chercheurs de l'UCLA et leurs collaborateurs ont développé une méthode qui pourrait ouvrir la porte à des investigations sur la fonction de la moitié de toutes les protéines du corps humain.
L'équipe de recherche a démontré un contrôle à l'échelle nanométrique sur des molécules, permettant l'étude précise des interactions entre protéines et petites molécules. Leur nouvelle technique, dans lequel des molécules sont utilisées comme appât pour capturer et étudier de grosses biomolécules, pourrait conduire à une nouvelle génération de médicaments psychiatriques.
Dans un article publié le mois dernier dans la revue ACS Chimie Neurosciences , une équipe interdisciplinaire de chercheurs de l'UCLA et de la Pennsylvania State University (PSU) rend compte de leur enquête sur les interactions entre les grandes biomolécules, qui comprennent l'ADN et les protéines, et de petites molécules, qui comprennent des hormones et des neurotransmetteurs tels que la sérotonine.
L'équipe de recherche, dirigé par Anne Andrews, professeur de psychiatrie et chercheur au Semel Institute for Neuroscience and Human Behavior de l'UCLA et au California NanoSystems Institute (CNSI) de l'UCLA, étudie ces interactions pour identifier une nouvelle génération de cibles, ou des molécules clés qui correspondent à des maladies ou conditions spécifiques.
Les interactions entre les grandes biomolécules et les petites molécules sont omniprésentes dans la nature; ils sont la méthode de communication à l'intérieur et entre les cellules. Mais ces interactions se sont avérées difficiles à isoler en laboratoire. Une meilleure compréhension de ces interactions est vitale pour le développement de nouveaux médicaments pour les troubles psychiatriques, disent les chercheurs.
"Actuellement, on sait peu de choses sur les cibles qui s'appliquent à des maladies spécifiques, " a déclaré Andrews. " Les sociétés pharmaceutiques sont très douées pour concevoir des médicaments une fois qu'elles ont une cible à poursuivre; mon groupe travaille à leur fournir des objectifs."
Jusqu'à ce point, Le développement de médicaments pour les troubles psychiatriques tels que la dépression a été un processus d'essais et d'erreurs dans lequel les sociétés pharmaceutiques raffinent de nouveaux médicaments sur la base de quelques médicaments existants qui ont été découverts accidentellement. Andrews a déclaré qu'elle espérait que les recherches de son équipe conduiront à des traitements plus efficaces, parce que les médicaments contre la dépression actuels ne fonctionnent que pour 30 à 50 pour cent de la population.
Le contrôle à l'échelle nanométrique est la clé des conclusions de l'équipe UCLA-Penn State. Leur percée capitalise sur les travaux du groupe de recherche du co-auteur Paul Weiss sur la structuration des monocouches auto-assemblées (SAM), couches simples de molécules qui s'orientent sur des surfaces planes. Weiss, un éminent professeur de chimie et de biochimie qui détient la chaire Fred Kavli de l'UCLA en sciences des nanosystèmes, et d'autres ont découvert que les SAM ne forment pas réellement des surfaces parfaites. Ils contiennent des défauts, qui peut à son tour être utilisé pour isoler des molécules uniques.
"Actuellement, nous sommes capables d'espacer les défauts sur une surface. Nous utilisons ensuite ces défauts pour contrôler le placement et l'environnement des molécules fonctionnelles individuelles, " dit Weiss, qui est également directeur de la CNSI.
Même l'espacement est important car l'équipe UCLA-Penn State a placé de la sérotonine, une petite molécule, dans les défauts pour servir d'appât pour capturer et étudier de grosses molécules. Si les défauts ne sont pas très espacés, il n'y a pas assez d'espace entre les molécules de sérotonine pour que chacune capture une grosse molécule.
Les interactions entre grandes biomolécules et petites molécules se sont avérées notoirement difficiles à étudier à l'aide de méthodes antérieures. Lorsque la canne à pêche SAM appâtée avec de la sérotonine capture une grosse molécule, l'équipe de recherche est en mesure d'étudier les interactions de manière à reproduire les interactions naturelles des molécules.