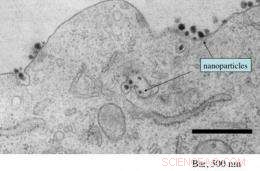
Cette micrographie électronique montre la présence de nombreuses nanoparticules ciblées contenant des siRNA à la fois entrant et à l'intérieur d'une cellule tumorale. Crédit :Caltech/Swaroop Mishra
Une équipe de chercheurs et de cliniciens dirigée par le California Institute of Technology (Caltech) a publié la première preuve qu'une nanoparticule ciblée - utilisée comme thérapeutique expérimentale et injectée directement dans la circulation sanguine d'un patient - peut pénétrer dans les tumeurs, délivrer de petits ARN interférents double brin (siARN), et désactiver un gène cancéreux important à l'aide d'un mécanisme appelé ARN interférence (ARNi). De plus, l'équipe a fourni la première démonstration que ce nouveau type de thérapie, infusé dans la circulation sanguine, peut se frayer un chemin vers les tumeurs humaines d'une manière dose-dépendante - c'est-à-dire, un nombre plus élevé de nanoparticules envoyées dans le corps entraîne un nombre plus élevé de nanoparticules dans les cellules tumorales.
Ces résultats, publié dans l'édition en ligne anticipée du 21 mars de la revue La nature , démontrer la faisabilité d'utiliser à la fois des nanoparticules et des thérapies basées sur l'ARNi chez les patients, et ouvrir la porte à de futures thérapies « changeantes » qui s'attaquent au cancer et à d'autres maladies au niveau génétique, dit Mark Davis, le professeur Warren et Katharine Schlinger de génie chimique à Caltech, et le chef de l'équipe de recherche.
La découverte de l'interférence ARN, le mécanisme par lequel les doubles brins d'ARN font taire les gènes, a valu aux chercheurs Andrew Fire et Craig Mello le prix Nobel 2006 de physiologie ou médecine. Les scientifiques ont signalé pour la première fois la découverte de ce nouveau mécanisme chez les vers en 1998 La nature papier. Depuis, le potentiel de ce type d'inhibition génique pour conduire à de nouvelles thérapies pour des maladies comme le cancer a été fortement vanté.
"L'ARNi est une nouvelle façon d'arrêter la production de protéines, ", explique Davis. Qu'est-ce qui en fait un outil potentiellement puissant, il ajoute, est le fait que sa cible n'est pas une protéine. Les zones vulnérables d'une protéine peuvent être cachées dans ses replis tridimensionnels, ce qui rend difficile pour de nombreux agents thérapeutiques de les atteindre. En revanche, L'interférence ARN cible l'ARN messager (ARNm) qui code les informations nécessaires à la fabrication d'une protéine en premier lieu.
"En principe, " dit Davis, « Cela signifie que chaque protéine est maintenant médicamenteuse car son inhibition est accomplie en détruisant l'ARNm. Et nous pouvons rechercher les ARNm d'une manière très conçue compte tenu de toutes les données génomiques qui sont et deviendront disponibles. »
Toujours, il y a eu de nombreux obstacles potentiels à l'application de la technologie ARNi comme thérapie chez l'homme. L'un des plus problématiques a été de trouver un moyen de transporter la thérapeutique, qui sont constitués de siARN fragiles, dans les cellules tumorales après injection directe dans la circulation sanguine. Davis, cependant, avait une solution. Avant même la découverte de l'ARNi, lui et son équipe avaient commencé à travailler sur des moyens de fournir des acides nucléiques dans les cellules via une administration systémique. Ils ont finalement créé un système à quatre composants, doté d'un polymère unique, qui peut s'auto-assembler en un nanoparticule contenant des siARN. Le système d'administration de siRNA est en cours de développement clinique par Calando Pharmaceuticals, Inc., une société de nanobiotechnologie basée à Pasadena.
"Ces nanoparticules sont capables d'amener les siARN vers le site ciblé dans le corps, " dit Davis. Une fois qu'ils ont atteint leur objectif, dans ce cas, les cellules cancéreuses dans les tumeurs - les nanoparticules pénètrent dans les cellules et libèrent les siARN.
Les résultats scientifiques décrits dans le La nature sont issus d'un essai clinique de phase I de ces nanoparticules qui a commencé à traiter des patients en mai 2008. Les essais de phase I sont, par définition, essais de sécurité ; l'idée est de voir si et à quel niveau le médicament ou autre thérapie devient nocif ou toxique. Ces essais peuvent également fournir une preuve de concept scientifique sur l'homme, ce qui est exactement ce qui est rapporté dans l'article de Nature.
Cette nanoparticule ciblée utilisée dans l'étude et présentée dans ce schéma est constituée d'un polymère unique et peut se frayer un chemin vers les cellules tumorales humaines de manière dose-dépendante. Crédit :Caltech/Derek Bartlett
En utilisant une nouvelle technique développée à Caltech, l'équipe a pu détecter et imager des nanoparticules à l'intérieur des cellules biopsiées des tumeurs de plusieurs des participants à l'essai. En outre, Davis et ses collègues ont pu montrer que plus la dose de nanoparticules administrée au patient est élevée, plus le nombre de particules trouvées à l'intérieur des cellules tumorales est élevé, le premier exemple de ce type de réponse dose-dépendante utilisant des nanoparticules ciblées.
Encore mieux, Davis dit, les preuves ont montré que les siARN avaient fait leur travail. Dans les cellules tumorales analysées par les chercheurs, l'ARNm codant pour la protéine de croissance cellulaire ribonucléotide réductase avait été dégradé. Cette dégradation, à son tour, conduit à une perte de la protéine.
Plus précisément, les fragments d'ARNm trouvés avaient exactement la longueur et la séquence qu'ils devraient avoir s'ils avaient été clivés à l'endroit ciblé par le siARN, note Davis. "C'est la première fois que quelqu'un trouve un fragment d'ARN provenant des cellules d'un patient montrant que l'ARNm a été coupé exactement à la bonne base via le mécanisme ARNi, " dit-il. " Cela prouve que le mécanisme de l'ARNi peut se produire en utilisant le siARN chez un humain. "
"Il existe de nombreuses cibles cancéreuses qui peuvent être efficacement bloquées en laboratoire à l'aide d'ARNsi, mais les bloquer dans la clinique a été insaisissable, " dit Antoni Ribas, professeur agrégé de médecine et de chirurgie au Jonsson Comprehensive Cancer Center de l'UCLA. "C'est parce que bon nombre de ces cibles ne peuvent pas être bloquées par des médicaments anticancéreux de conception traditionnelle. Cette recherche fournit la première preuve que ce qui fonctionne en laboratoire pourrait aider les patients à l'avenir par la livraison spécifique de siARN à l'aide de nanoparticules ciblées. Nous pouvons commencer à penser à cibler les non-ciblables."
"Bien que ces données soient très précoces et que des recherches supplémentaires soient nécessaires, il s'agit d'une étude prometteuse d'un nouvel agent anticancéreux, et nous sommes fiers de notre contribution au développement clinique initial de siRNA pour le traitement du cancer, " dit Anthony Tolcher, directeur de la recherche clinique à South Texas Accelerated Research Therapeutics (START).
« Les données prometteuses des essais cliniques valident nos années de recherche à City of Hope sur la ribonucléotide réductase comme cible de nouvelles thérapies géniques contre le cancer, " ajoute le coauteur Yun Yen, directeur associé pour la recherche translationnelle à City of Hope. "Nous voyons pour la première fois l'utilité du siRNA comme thérapie anticancéreuse et comment la nanotechnologie peut cibler spécifiquement les cellules cancéreuses."
L'essai de phase I, parrainé par Calando Pharmaceuticals, se déroule au START et au Jonsson Comprehensive Cancer Center de l'UCLA, et les résultats cliniques de l'essai seront présentés ultérieurement. "Tout au moins, nous avons prouvé que le mécanisme de l'ARNi peut être utilisé chez l'homme à des fins thérapeutiques et que l'administration ciblée de siARN permet une administration systémique, ", dit Davis. "C'est une période très excitante."